Clear Sky Science · ar
البيانات البلورية لإنزيم دوليشيلفوسفات مانووز (من Pyrococcus furiosus) تشير إلى أن الإنزيم قد يقلب منتجه الجليكوليبيدي
كيف تحافظ الميكروبات المحبة للحرارة على طلاء خلاياها
تنجو العديد من الميكروبات التي تزدهر في بيئات شديدة الغليان بفضل غلاف سكري واقي على سطح خليةها. يتطلب بناء هذا الغلاف جزيئات خاصة من الدهن–السكر التي يجب تصنيعها على جانب واحد من غشاء الخلية ثم نقلها إلى الجانب الآخر. تفكك هذه الدراسة أحد الإنزيمات المصنعة لمثل هذه الجزيئات من ميكروب محب للحرارة وتقترح أنه، بشكل لافت، قد يساعد نفس البروتين أيضاً في قلب منتجه عبر الغشاء — أي أداء مهمتين في آنٍ واحد.
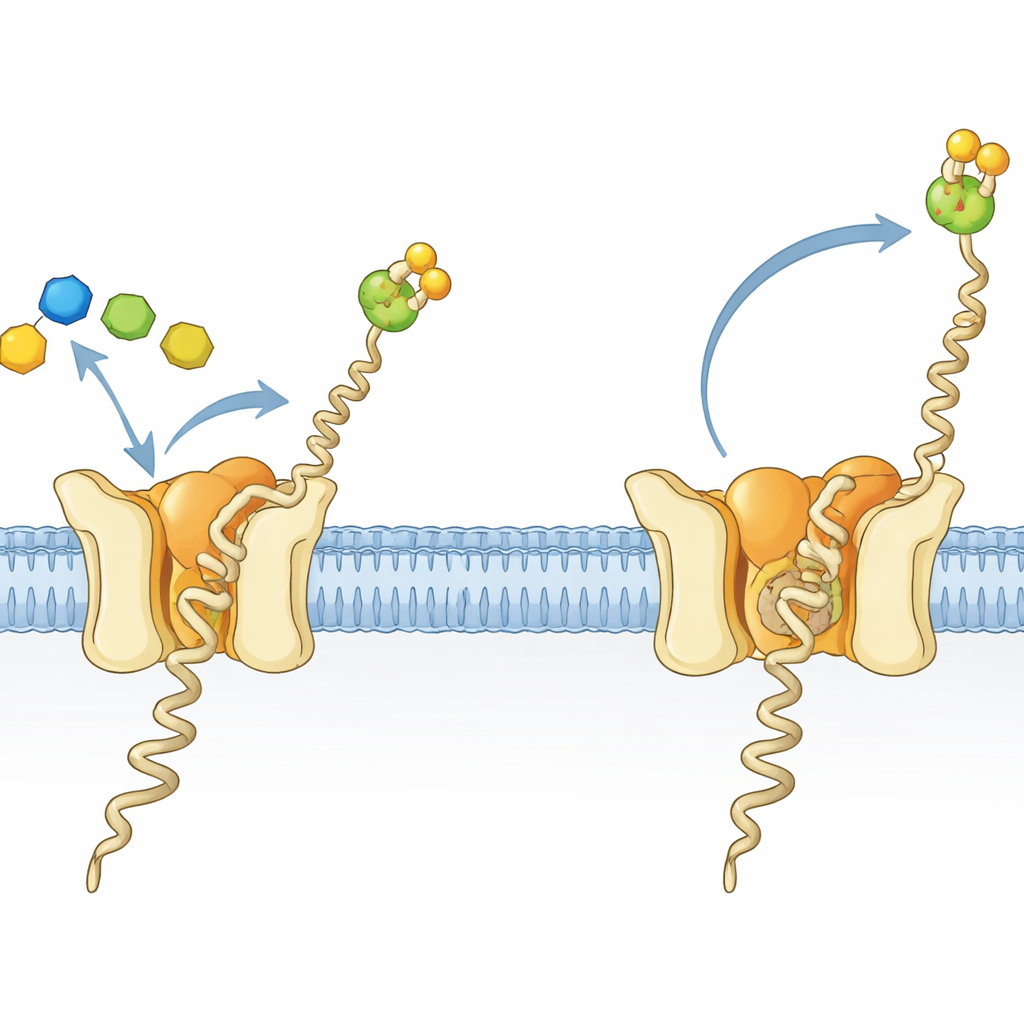
مصنع صغير لجزيء دهني–سكري حيوي
تزين الخلايا في جميع مجالات الحياة العديد من البروتينات بسلاسل من السكريات، وهي عملية ضرورية للطي الصحيح والاستقرار والتواصل بين الخلايا. في العسجيات والحقيقيات، يعد جزيء دهني–سكري أساسي لهذه الزينة هو دوليشيلفوسفات مانووز (Dol-P-Man). يتكون من ذيل دهني طويل مُثبت في الغشاء ورأس فوسفات–سكري يبرز إلى الوسط المائي. يصنع Dol-P-Man بواسطة إنزيم دوليشيلفوسفات مانووز سينثاز (DPMS)، الذي ينقل سكر المانووز من مانح قابل للذوبان إلى ليبيد مُثبّت في الغشاء. في العسجية شديدة التحمل للحرارة Pyrococcus furiosus، يكون DPMS بروتيناً ذو سلسلة واحدة، يُسمى النوع-III من DPMS، ذو جزء حفازي قابل للذوبان مربوط بقسم عابر للغشاء مكوّن من أربع حلزونات دورها كان غير واضح.
التقاط الإنزيم أثناء العمل
بلَّور الباحثون DPMS من P. furiosus مع ركائزه وتتبعوا التفاعل بواسطة البلورية بالأشعة السينية. البنية الجديدة، مجتمعة مع ثلاث تراكيب سابقة، تلتقط سلسلة لقطات تحيط بلحظة نقل السكر. في حالة واحدة، يكون جزيء المانح (GDP-مانوز) ومُستقبل شبيه بـDol-P مربوطين بتشكيل هندسي دقيق يضع الكربون التفاعلي للمانوز مباشرة أمام مجموعة الفوسفات على Dol-P — ترتيب «قبل النقل» مثالي. تعمل حلقات على الإنزيم كأبواب أمامية وخلفية: تغلق لتثبت المانح وأيون المعدن في مكانه، ثم تعيد ترتيبها لفتح مسار لدخول Dol-P ولمغادرة GDP المستهلك بعد تمرير السكر. هذه التفاصيل توضح كيف يضمن الإنزيم نقل السكر بكفاءة ودقة على سطح الغشاء.
منتج مقلوب مخبأ داخل الغشاء
أكثر ما كان مفاجئاً وجود حالة ثانية متميزة رُصدت في نفس البلورات. هنا، جزيء Dol-P-Man المكتمل ليس في الموقع الفعال بل محتبس أعمق داخل القسم العابر للغشاء من البروتين، في وضعية «مقلوبة». رأسه الفوسفات–السكري يجلس في جيب قطبي بين زوجين من الحلزونات (TMD1 وTMD2)، بينما يمتد الذيل الدهني على طول أخدود تشكله الحلزونات. يبدو أن حمض أميني رئيسي، فينيل ألانين، يعمل كبوابة يمكن أن تسد أو تفتح الوصول إلى هذا الجيب. جودة كثافة الإلكترون وطريقة تعبئة البروتين في البلورة تدلان على أن هذا Dol-P-Man المقلوب ليس تحريفاً ناتجاً عن اتصالات البلورة، بل حالة حقيقية ومأهولة جيداً يمكن للإنزيم تبنيها.
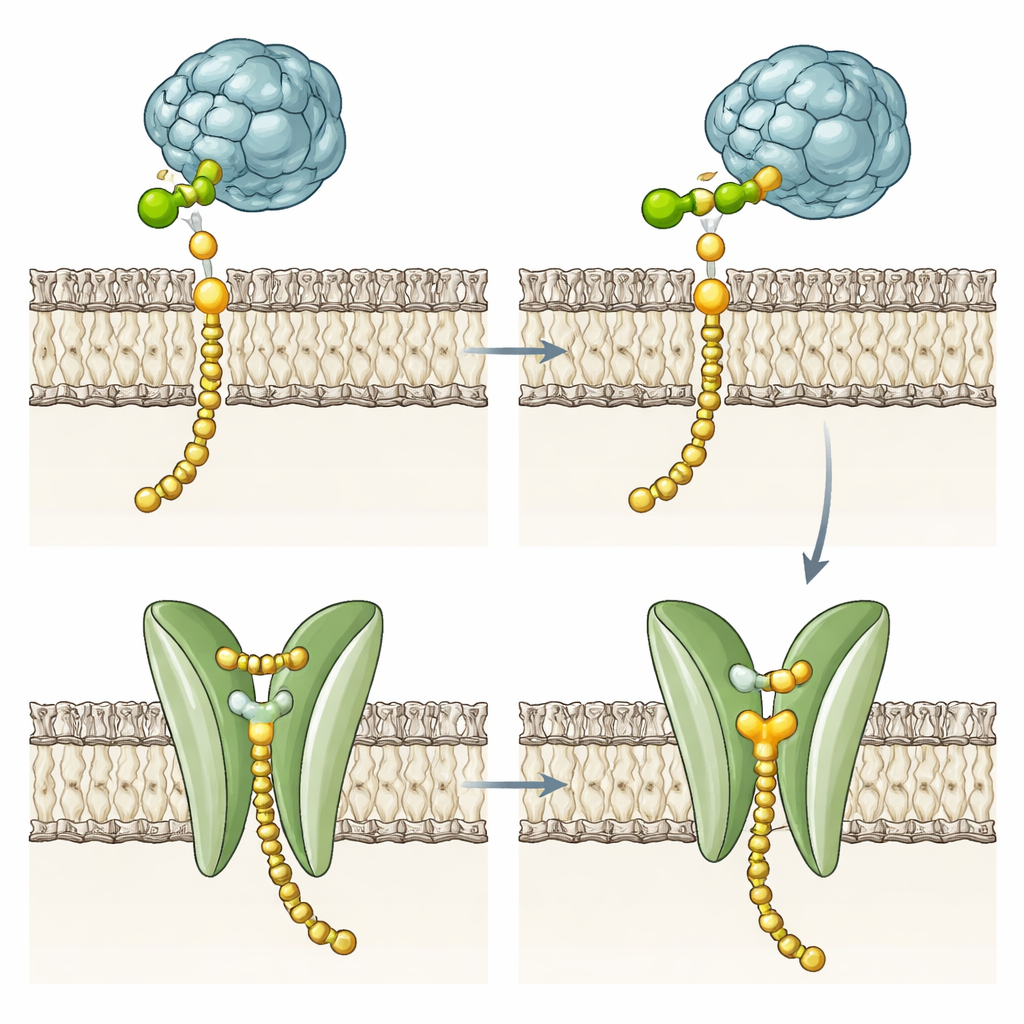
إنزيمات طفيرية توحي بمهمة ثانية
لاختبار ما إذا كان القسم العابر للغشاء مطلوباً لكيمياء نقل السكر، صمم الفريق متغيرات متعددة. حذفوا معظم الحلزونات أو كلها، استبدلوها بقسم غشائي مختلف من DPMS الفطري، أو عدّلوا بقايا الجيب الرئيسية وبوابة الفينيل ألانين. اللافت أن هذه الطفرات استمرت في صنع Dol-P-Man بمعدلات مشابهة للإنزيم السليم، رغم أن بعضاً منها كان أقل استقراراً قليلاً في الغشاء. يظهر هذا أن الكيمياء الجوهرية تقيم في المنطقة الحفازة القابلة للذوبان وأن حزمة الحلزونات الأربع غير مطلوبة لإلحاق المانووز بـDol-P. بدل ذلك، يقترح جيبها القطبي المحفوط والأخدود وباقي البوابة دوراً متخصصاً في التعامل مع المنتج النهائي، لا سيما في العسجيات شديدة التحمل للحرارة التي تجعل أغشيتها الصلبة قلب الدهون التلقائي مكلفاً من الناحية الطاقية.
لماذا يهم وجود إنزيم ذو غرض مزدوج
بجمع الأدلة البنيوية والطفرية، يقترح المؤلفون أن النوع-III من DPMS هو بروتين «متعدد الوظائف» (moonlighting). يصنع أولاً Dol-P-Man على الوجه الداخلي لغشاء البلازما العسجِي؛ ثم قد يساعد نطاقه العابر للغشاء في قلب الجزيء الدهني–السكري بحيث يظهر الرأس على السطح الخلوي الخارجي، جاهزاً ليستخدمه إنزيمات أخرى تبني الغلاف السكري للخلية. يبدو أن التطور فضّل هذا التصميم المخلوقي خصوصاً في العسجيات المحبة للحرارة الشديدة، حيث قد يقلل تقريب موقع التصنيع إلى أخدود مخصص للقلب من الهدر والأضرار الحرارية. رغم أن هذا العمل لم يثبت نشاط القلب مباشرة بعد، إلا أنه يقدم نموذجاً بنيوياً ملموساً لكيفية قدرة إنزيم على كل من إنشاء وإعادة تموضع وسيط دهني حيوي عبر حاجز غشائي قاسٍ.
الاستشهاد: Gandini, R., Keskitalo, M.M., Reichenbach, T. et al. Crystallographic data for Pyrococcus furiosus dolichylphosphate mannose synthase suggest that the enzyme could flip its glycolipid product. Sci Rep 16, 9076 (2026). https://doi.org/10.1038/s41598-026-44343-5
الكلمات المفتاحية: دوليشيلفوسفات مانووز, قلباء الدهون (lipid flippase), العسجيات (archaea), جليكوزلة البروتينات, إنزيمات الغشاء