Clear Sky Science · ar
تنظّم PGE2 التحلل الحديدي وتكوّن العظم في خلايا MC3T3-E1 عبر NOS2
لماذا يؤثر تقويم الأسنان على عظامك
تقويم الأسنان والملفات الشفافة يفعلان أكثر من مجرد تحريك الأسنان—فهما يطالبان العظم المحيط بكل سن بإعادة تشكيل نفسه. هذا العمل البيولوجي البطيء في البناء هو أحد الأسباب التي تجعل علاج التقويم يستغرق سنوات أحيانًا. تبحث هذه الدراسة داخل خلايا تكوّن العظم لتفهم كيف قد يؤثر إشارة التهابية شائعة، البروستاجلاندين E2، على تسريع الحركة وفي الوقت نفسه إضعاف العظم الجديد بهدوء، ما يفتح آفاقًا لاحقة لطرق تجعل علاج التقويم أسرع وأكثر ثباتًا.
الإشارات التي تُطلق عند دفع الأسنان
عندما يطبق أخصائي التقويم قوة على سن، يتعرّض الرباط والعظم حول الجذر لإصابة خاضعة للرقابة. تُطلق الخلايا في هذه المنطقة رُسلاً كيميائية، من بينها البروستاجلاندين E2، التي تساعد في تنسيق كيفية تحلّل العظم من جهة وإعادة بنائه من الجهة المقابلة. ركّز المؤلفون على خلايا بناء العظم المعروفة بالاستيوبلاستات، مستخدمين سطر خلايا فأر قياسي كنموذج. أرادوا معرفة كيف يشكّل البروستاجلاندين E2 نتيجتين رئيسيتين داخل هذه الخلايا: قدرتها على بناء عظم مُمكّن بالتكلّس وميلها للخضوع لشكل جديد من الموت الخلوي المعتمد على الحديد يُسمى التحلل الحديدي.
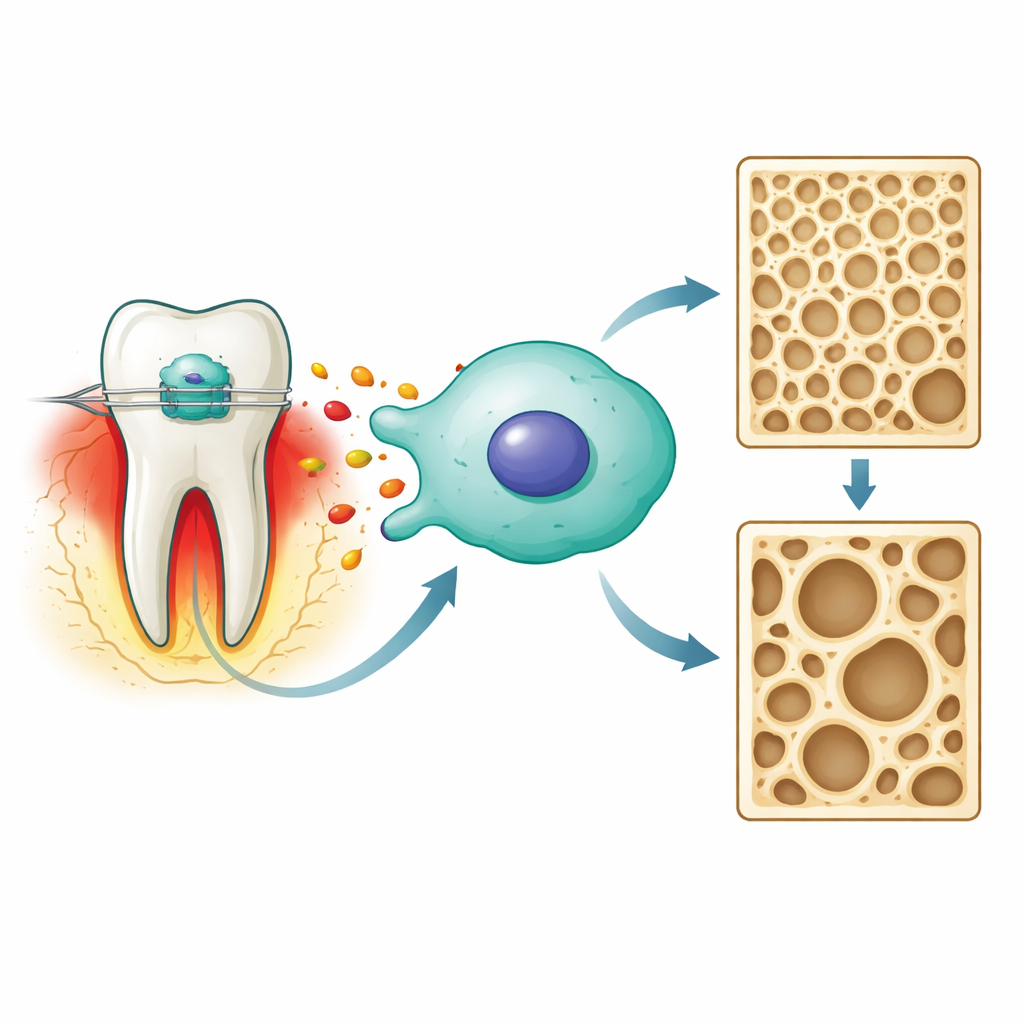
مسار ضغط يتركّز حول إنزيم واحد
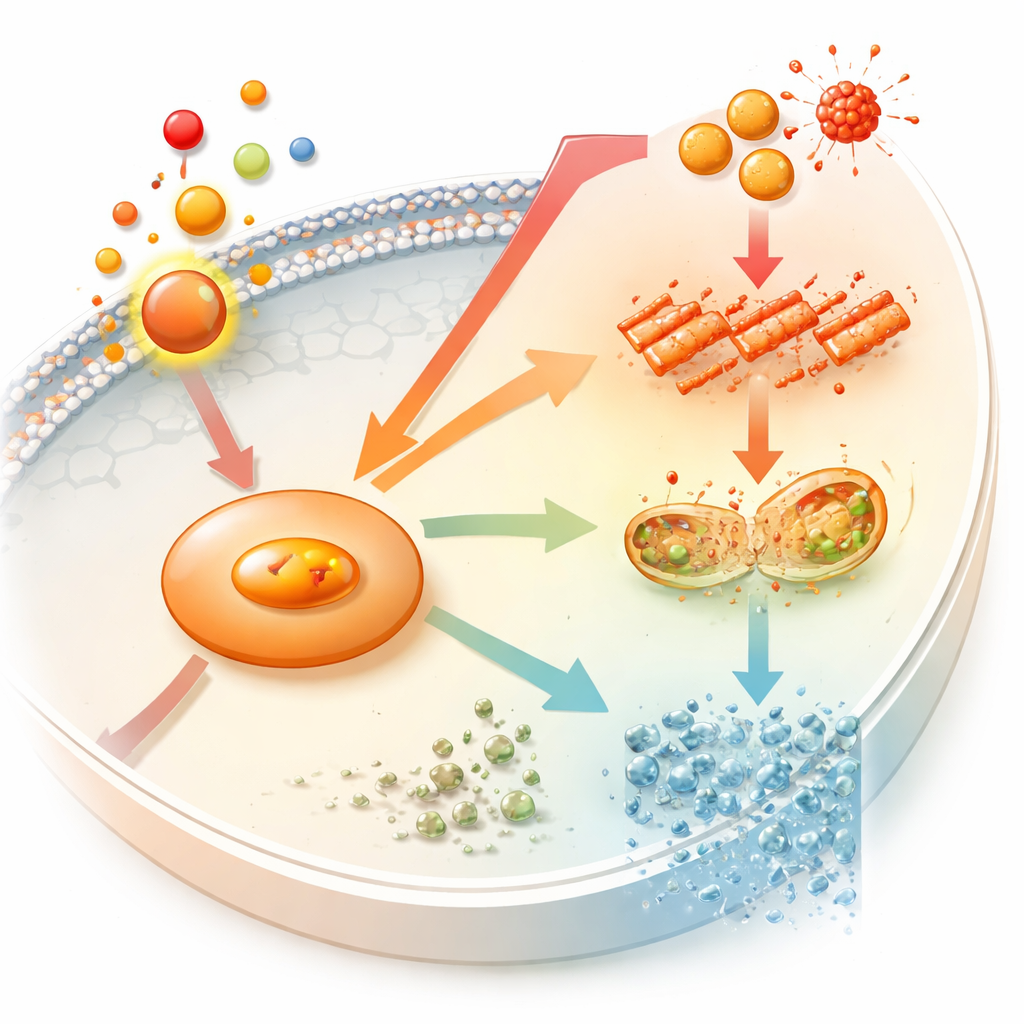
باستخدام بيانات جينية من جرذان خضعت لتحريك الأسنان، بحث الفريق أولاً عن جزيئات مرتبطة كلّها بقوة التقويم وبالتحلل الحديدي. برز مرشح واحد، إنزيم يُدعى سينثاز أكسيد النيتريك 2 (NOS2)، كمحور مركزي. في البِرشَة، أحدث تعريض خلايا شبيهة بالاستيوبلاستات لجرعة ذات صلة سريريًا من البروستاجلاندين E2 حالة من الالتهاب «المعقم»—دون جراثيم، فقط ضغط ميكانيكي. تحت هذه الإشارة ارتفعت مستويات NOS2، كما ارتفعت مؤشرات الإجهاد وجزيئات الأكسدة الضارة، بينما انخفضت البروتينات الواقية المضادة للأكسدة وتلك المسؤولة عن التعامل مع الحديد. معًا، تشكّل هذه التغيرات علامات بدايات التحلل الحديدي داخل الخلية.
عندما تتوقف خلايا بناء العظم عن العمل
نفس علاج البروستاجلاندين E2 جعل الخلايا أقل أداءً في وظائفها كبنائين للعظم. انخفضت العلامات التقليدية لتكوّن العظم، وأظهرت اختبارات تُظهر المعادن الشبيهة بالعظم المبكرة وإنزيمًا رئيسيًا هو الفوسفاتاز القلوي تلوينًا أضعف وترسيبًا معدنيًا أقل. عندما أضاف الباحثون فيروستاتين-1، دواء معروف بقدرته على حجب التحلل الحديدي، تراجعت كثير من هذه الأذية: هدأ الإجهاد التأكسدي، خفت إشارات التحلل الحديدي، وعادت النشاطات العظمية إلى الارتفاع. وهذا يشير إلى أن الإشارة الالتهابية تعيق تكوّن العظم جزئيًا عن طريق دفع الخلايا نحو التحلل الحديدي، على الأقل في هذا النموذج.
تغيير مستوى NOS2 كأنه مفتاح
ليروا ما إذا كان NOS2 مجرد مراقب أم محرك نشط، خصّص الفريق تعديلًا وراثيًا لرفع مستوياته أو خفضها. إن تقليل NOS2 في الخلايا المعالجة بالبروستاجلاندين خفّض علامات التحلل الحديدي، قلّل الضرر التأكسدي، وأعاد السلوك البنّاء للعظم إلى مستويات قريبة من الطبيعية. أما الإفراط في التعبير عن NOS2 فكان له التأثير المعاكس: زدّد الإجهاد وكبت خصائص بناء العظم أكثر. اللافت أن رفع NOS2 بمفرده—دون إضافة البروستاجلاندين E2—كان كافيًا لإطلاق تغيرات شبيهة بالتحلل الحديدي وتراجع التكوّن العظمي. هذا يبيّن أن NOS2 لا يقتصر على الاستجابة للالتهاب؛ بل يمكنه بنفسه دفع الاستيوبلاستات بعيدًا عن تشكيل عظم معياري متماسك.
ماذا يعني هذا لتقويم الأسنان في المستقبل
معًا ترسم هذه التجارب محورًا جديدًا في بيولوجيا العظم أثناء حركة الأسنان: يرفع البروستاجلاندين E2 مستوى NOS2، ويسهم NOS2 في تلف تأكسدي والتحلل الحديدي، وتتناقص قدرة الخلايا على بناء العظم. بالنسبة للمرضى، لا يعني هذا أن التقويم غير آمن، لكنه يوضح سبب كون العلاج توازنًا دقيقًا بين تحريك الأسنان بسرعة والحفاظ على عظم قوي حولها. على المدى الطويل، قد تساعد أدوية أو مواد تضبط نشاط NOS2 أو تحمي الاستيوبلاستات من التحلل الحديدي أطباء التقويم على تقصير مدة العلاج مع الحفاظ على جودة واستقرار العظم الداعم، أو حتى تحسينهما.
الاستشهاد: Sun, M., Yang, Y., Pang, L. et al. PGE2 regulates ferroptosis and osteogenesis of MC3T3-E1 cells via NOS2. Sci Rep 16, 8893 (2026). https://doi.org/10.1038/s41598-026-43001-0
الكلمات المفتاحية: تحريك الأسنان التقويمي, إعادة تشكيل العظم, التحلل الحديدي, سينثاز أكسيد النيتريك, وظيفة الخلية البانية للعظم