Clear Sky Science · ar
مركبات الزجاج الحيوي/الكيتوزان المحملة بالتينوكسيكام لهندسة أنسجة العظام: توصيف مختبري، إطلاق دواء مستمر، ونشاط مضاد للميكروبات
شفاء العظام المكسورة بمواد أذكى
عندما يتعرض العظم لضرر كبير، يحتاج الأطباء في كثير من الأحيان إلى أكثر من صفائح ومسامير معدنية. عليهم تهدئة الألم والتورم، ومحاربة الجراثيم المحتملة، وتحفيز نمو عظم جديد. تستكشف هذه الدراسة مادة ذكية واحدة تحاول القيام بكل ذلك دفعة واحدة: سقالة صغيرة شبيهة بالعظم تُطلق ببطء دواءً مضادًا للالتهاب بينما ترتبط بإحكام بالهيكل العظمي وتمنع نمو البكتيريا الضارة.
نوع جديد من رقعة العظم
ركز الباحثون على مشكلة عنيدة في جراحة العظام: العيوب العظمية الكبيرة التي تكون مؤلمة، وملتهبة، ومعرضة للعدوى. تنتقل المسكنات والمضادات الحيوية التقليدية في جميع أنحاء الجسم وقد لا تصل إلى مستويات مرتفعة بما يكفي في موقع الإصابة حيث الحاجة ماسة. سعى الفريق إلى بناء «رقعة عظمية» موضعية يمكن وضعها مباشرة في المنطقة المصابة، تدعم الأنسجة النامية، وتوفر الدواء بشكل ثابت على مدى أسابيع، كل ذلك مع كونها لطيفة على الجسم.
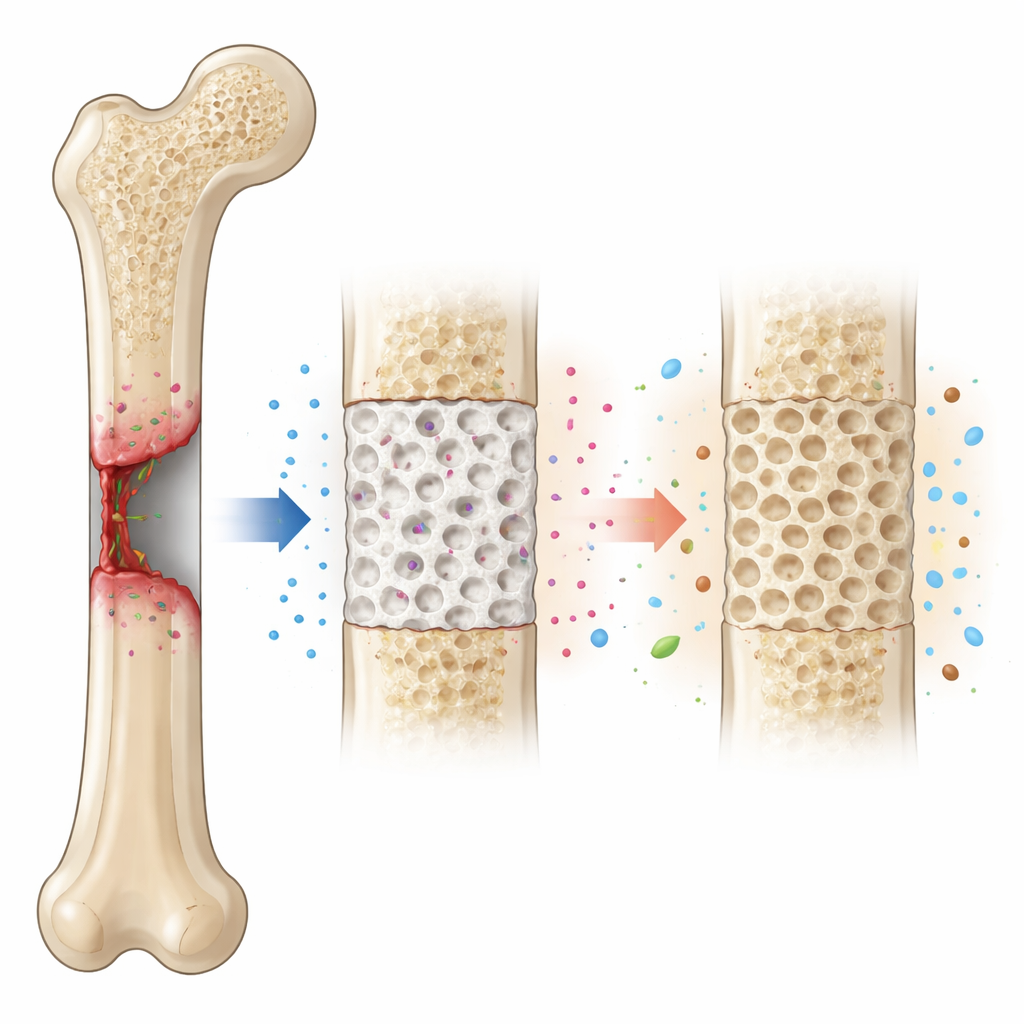
مزج الزجاج والسكر الطبيعي ومسكن الألم
المادة التي صمموها تجمع بين ثلاثة مكونات رئيسية. الأول هو الزجاج الحيوي، نوع خاص من الزجاج معروف بقدرته على الارتباط بقوة بالعظم من خلال تشكيل طبقة معدنية رقيقة مشابهة لبلورات العظم الطبيعية. الثاني هو الكيتوزان، مادة قابلة للتحلل مشتقة من قشور القشريات يمكنها تشكيل هياكل مرنة مسامية ولها خصائص خفيفة لمكافحة الجراثيم. الثالث هو التينوكسيكام، دواء شائع يُستخدم لتقليل الألم والالتهاب. باستخدام مسار كيميائي يُعرف بعملية السول-جيل، أدرج الفريق كميات مختلفة من التينوكسيكام (1 و2 و3 بالمئة بالوزن) في مزيج من الزجاج الحيوي والكيتوزان، ثم ضغطوا المساحيق الناتجة إلى أقراص صغيرة.
اختبار سلوك رقعة العظم داخل الجسم
لمحاكاة ما يحدث داخل الإنسان، تم نقع الأقراص لأكثر من شهر في سائل يحاكي بلازما الدم البشرية. استُخدمت أدوات متقدمة لمراقبة كيفية تغير أسطحها. أظهرت التحليلات الطيفية وقياسات الأشعة السينية أن جميع العينات نمت بسرعة طبقة من الهيدروكسيأباتيت، نفس المعدن الذي يشكّل جزءًا كبيرًا من العظم الطبيعي. أصبحت هذه الطبقة أكثر انتظامًا ووفرة مع مرور الوقت، لا سيما في العينة ذات التحميل الدوائي الأعلى. كشفت صور المجهر الإلكتروني عن سطح مسامي للغاية مليء بفتحات مترابطة. هذه المسامية حاسمة: فهي تسمح للسوائل الجسدية والمغذيات وخلايا تكوين العظم بأن تتغلغل وتتثبت، مما يساعد الزرعة على الاندماج مع النسيج الحي.
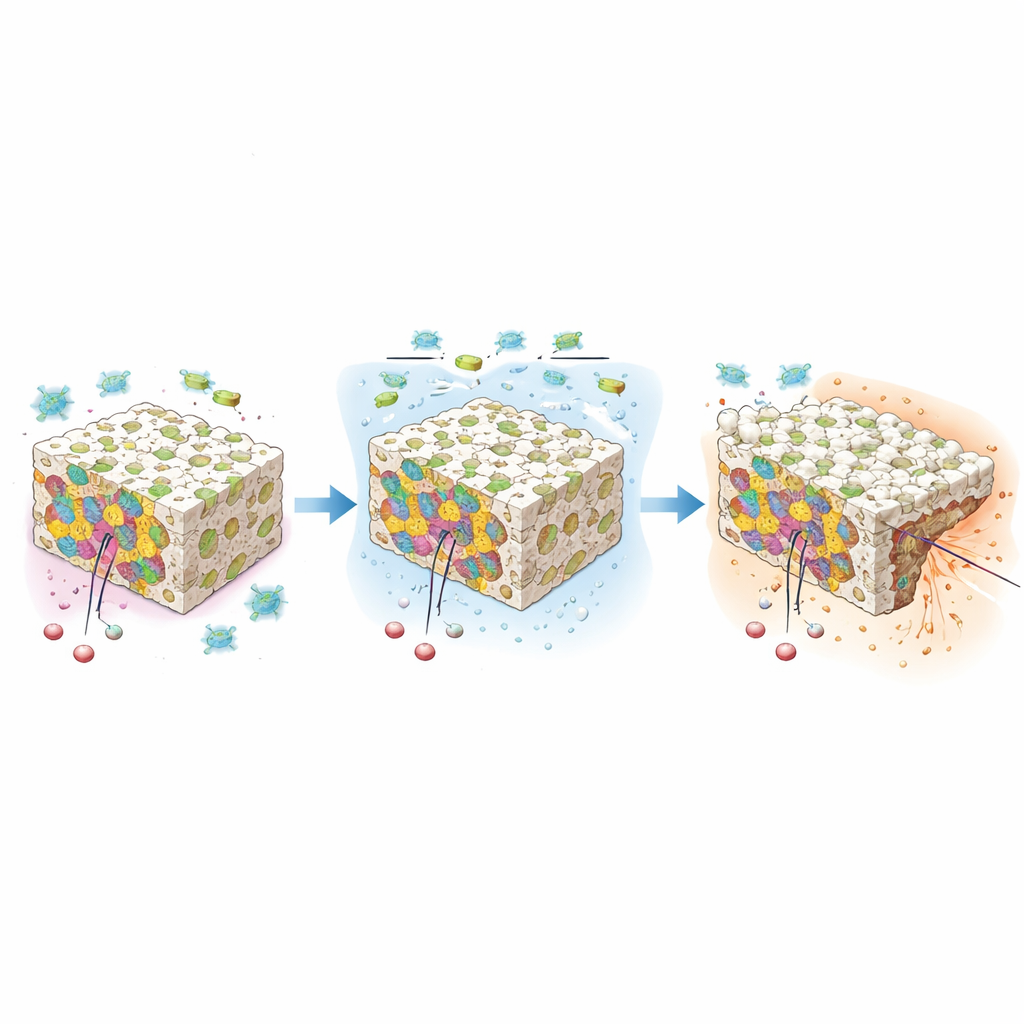
دواء بطيء ومستمر ودفاع مدمج ضد الجراثيم
تتبع العلماء أيضًا كيفية خروج التينوكسيكام من الأقراص على مدى 33 يومًا. أصدرت النسخ الثلاثة الدواء في ثلاث مراحل: اندفاع أولي أسرع، وفترة وسطى من الإخراج المستقر، وذيل أبطأ. بشكل عام، تبع الإطلاق سلوكًا قريبًا من النظام الصفري، مما يعني أن الدواء خرج بمعدل شبه ثابت — وهو مثالي للحفاظ على تحكم ثابت في الألم والالتهاب دون تقلبات كبيرة. أفرجت العينة ذات التحميل الأعلى عن أكبر كمية إجمالية مع الحفاظ على التحكم. بالتوازي، ضغط الفريق المواد إلى أقراص صغيرة ووضعها على أطباق مزروعة بالبكتيريا. أنتجت المركبات مناطق تثبت خالية واضحة ضد سلالات موجبة وسالبة الجرام على حد سواء، بما في ذلك Staphylococcus aureus وEscherichia coli. أظهرت العينة التي تحتوي على أكبر كمية من التينوكسيكام أقوى تأثير مضاد للبكتيريا بشكل عام.
ما الذي قد يعنيه هذا لإصلاح العظام في المستقبل
تشير النتائج مجتمعة إلى أن هذه المركبات من الزجاج الحيوي–الكيتوزان المحملة بالتينوكسيكام يمكنها أداء ثلاث وظائف في وقت واحد: فهي ترتبط بالعظم عبر نمو طبقة معدنية طبيعية، وتوفر مصدرًا موضعيًا طويل الأمد لتخفيف الألم والالتهاب، وتساعد في كبح البكتيريا الضارة حول منطقة الإصابة. وعلى الرغم من أن العمل أُجري في اختبارات مخبرية وليس على المرضى، فإنه يشير إلى إمكانات زرعات عظمية مستقبلية لا تعمل كمباعدات سلبية فحسب، بل كشركاء نشطين في الشفاء — تدعم نمو العظم الجديد بينما توصل الدواء بهدوء إلى المكان الذي يحتاجه أكثر.
الاستشهاد: El-khooly, M.S., Elkelish, A., Abdel-Aal, A.A. et al. Tenoxicam-loaded bioglass/chitosan composites for bone tissue engineering: in vitro characterization, sustained drug release, and antimicrobial activity. Sci Rep 16, 8258 (2026). https://doi.org/10.1038/s41598-026-42389-z
الكلمات المفتاحية: هندسة أنسجة العظام, هيكل مطلق للأدوية, مركب زجاج حيوي كيتوزان, توصيل التينوكسيكام, مادة حيوية مضادة للبكتيريا