Clear Sky Science · ar
يقلل GV1001 من تاو 4R المرضي والعجز الوظيفي في نماذج ذات صلة بالشلل فوق النووي التقدمي
لماذا يهم هذا الناس والعائلات
الشلل فوق النووي التقدمي (PSP) هو اضطراب دماغي نادر ولكنه مدمر يجرد المصابين من التوازن والحركة والوضوح الذهني خلال سنوات قليلة فقط. لا توجد حالياً أدوية تثبط تقدم المرض. تبحث هذه الدراسة في جزيء دوائي صغير يسمى GV1001، طوّر أصلاً لعلاج السرطان، وتبيّن أنه يمكن أن يخفف مشاكل الحركة ويقلل التغيرات الخلوية المرتبطة بالمرض في نماذج مختبرية للـ PSP. تشير النتائج إلى نهج جديد لمهاجمة مجموعة من الأمراض التي تقودها شكل ضار من بروتين تاو.
مساعد المرور في الدماغ عندما يختل عمله
تشارك بروتينات تاو في العديد من أمراض الدماغ؛ فتاو عادة يساعد على استقرار “المسارات” الداخلية التي تتحرك عبرها المواد داخل الخلايا العصبية. في الـ PSP، يتراكم شكل معين يسمى 4R تاو في مناطق عميقة من الدماغ، وخاصة في منتصف الدماغ، حيث يعطل بنية الخلية ويضر الوصلات وينتهي به المطاف إلى موت الخلايا. يصاب الأشخاص بالتيبس والسقوط ومشاكل حركة العين وصعوبات في التفكير، وغالباً ما يتدهور وضعهم بسرعة خلال خمس إلى ثماني سنوات. على عكس مرض الزهايمر، يهيمن في PSP شكل 4R من تاو، مما يجعله هدفاً مهماً للعلاجات المصممة خصيصاً لاضطرابات تاو المرتبطة بالحركة.
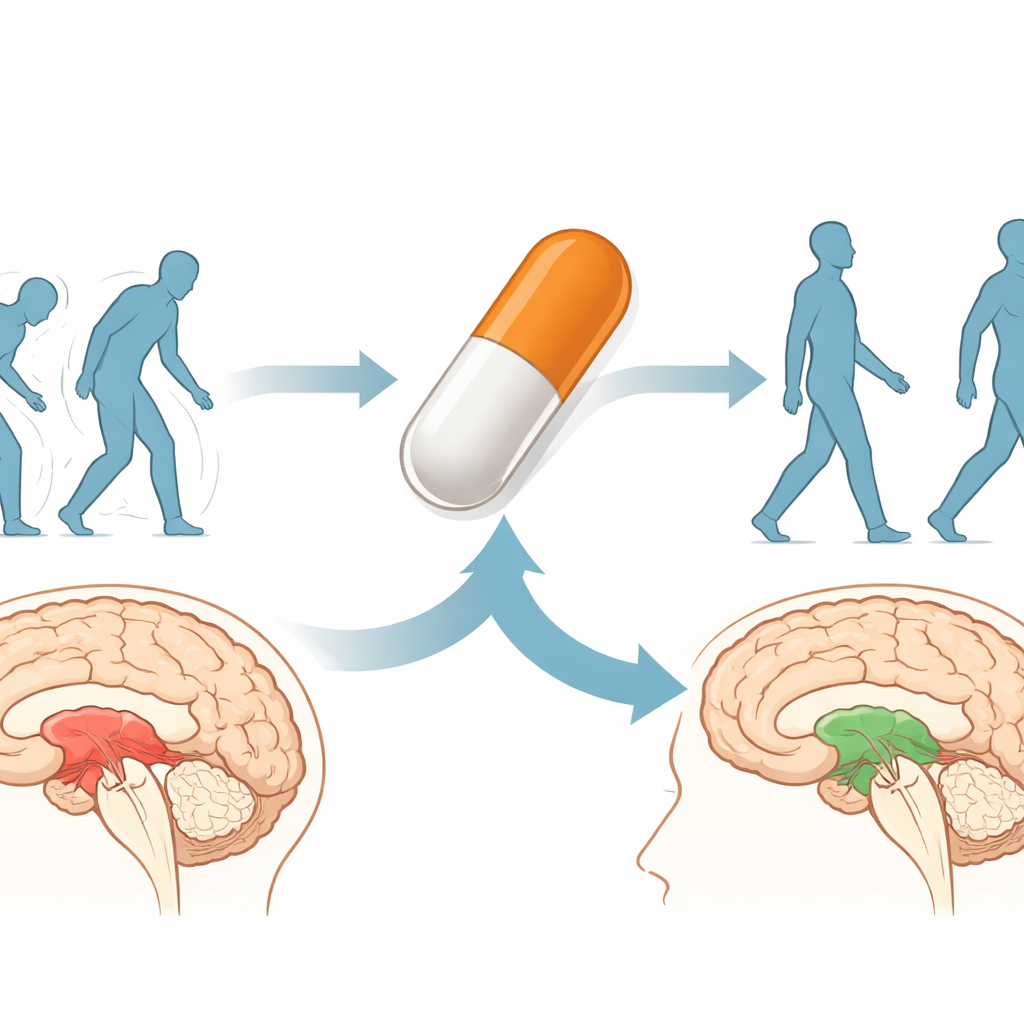
مرشح دوائي للسرطان يجد دوراً جديداً
GV1001 هو ببتيد قصير مشتق من التيلوميراز البشري، إنزيم نشط في العديد من السرطانات. تم اختباره بالفعل في أورام عدة ومؤخراً في حالات مثل تضخم البروستات ومرض الزهايمر، مع سجل أمان عامٍ جيد. أظهرت أعمال سابقة أن GV1001 يمكنه حماية الخلايا الدماغية من التلف التأكسدي، ودعم الميتوكوندريا المنتجة للطاقة، وتخفيف الاستجابات الالتهابية في الدماغ. تدرس الدراسة الحالية ما إذا كانت هذه التأثيرات الوقائية العامة، إلى جانب أي تأثيرات جديدة، قد تجعل GV1001 مفيداً للاضطرابات التي يكون فيها تاو 4R هو الفاعل الرئيسي، مثل PSP.
اختبار الحركة والذاكرة والتغيرات الدماغية في الفئران
استخدم الباحثون فأراً معدل وراثياً خصيصاً لإنتاج تاو بشري مماثل للشكل 4R القابل للتجمع، مما يؤدي بمرور الوقت إلى مشاكل في الحركة والذاكرة. بدءاً من عمر سبعة أشهر، تلقّت هذه الفئران GV1001 تحت الجلد ثلاث مرات أسبوعياً لمدة نحو خمسة أشهر. مقارنة بالحيوانات غير المعالجة، بقيت الفئران المعالجة بـ GV1001 لفترات أطول على قضيب دوار، مشَت لمسافات أطول وبسرعات أكبر في ساحة مفتوحة، وأظهرت تمييزاً أفضل للأجسام الجديدة، مما يوحي بتحسن المهارات الحركية والذاكرة. عند فحص الأدمغة، وجد الباحثون تجمعات أقل لتاو وعدداً أقل من العلامات الكيميائية المرتبطة بـ «تاو المفرط النشاط» في مناطق متعددة، بما في ذلك القشرة والحُصين والمادة السوداء، وهي مناطق مهمة للحركة والمعرفة.
نظرة داخل الخلايا الدماغية وتهدئة الالتهاب العصبي
بعيداً عن تاو نفسه، تتميز PSP والأمراض ذات الصلة بفقدان المشابك—نقاط التواصل بين الخلايا العصبية—وفرط تنشيط الخلايا الداعمة المسماة النجمات والخلايا البلعمية الصغيرة، التي تحفز الالتهاب المزمن. في الفئران المعالجة، عادت مستويات بروتينات المشبك الرئيسية نحو الوضع الطبيعي، ما يوحي بأن GV1001 يساعد في الحفاظ على الوصلات العصبية. انخفضت مؤشرات تنشيط النجمات والخلايا البلعمية الصغيرة، سواء في أدمغة الفئران أو في خطوط خلايا بشرية حُفِّزت لتقليد الالتهاب. كما قلل الدواء مستويات TSPO، وهو بروتين يستخدم في تصوير الدماغ لتتبع الالتهاب، ما يفتح الاحتمال بأن التصوير مستقبلاً قد يراقب تأثير GV1001 لدى المرضى.
استهداف مباشر لشكل تاو 4R الضار
لاختبار ما إذا كان GV1001 يؤثر على تاو 4R بشكل أكثر خصوصية، أنشأ الفريق نموذج خلايا قائم على الإنسان للـ PSP عن طريق تمايز خلايا شبيهة بالعصب البشري وتعريضها لأنوناسين، سم نباتي يضر الميتوكوندريا ويزيد من تاو 4R. كما هو متوقع، زاد annonacin بشكل حاد كمية تاو 4R دون تغيير إجمالي تاو. عند إضافة GV1001 بعد بدء هذا الضرر، عادت مستويات تاو 4R الزائدة ونسبة تاو 4R إلى إجمالي تاو نحو الوضع الطبيعي، بينما بقي إجمالي التاو دون تغير كبير. شوهدت تخفيضات انتقائية مماثلة في تاو 4R في أدمغة الفئران المعالجة. تشير هذه النتائج إلى أن GV1001 يفعل أكثر من حماية الخلايا عموماً—فهُو يبدو أنه يخفض تحديداً شكل التاو الأكثر ارتباطاً بـ PSP.
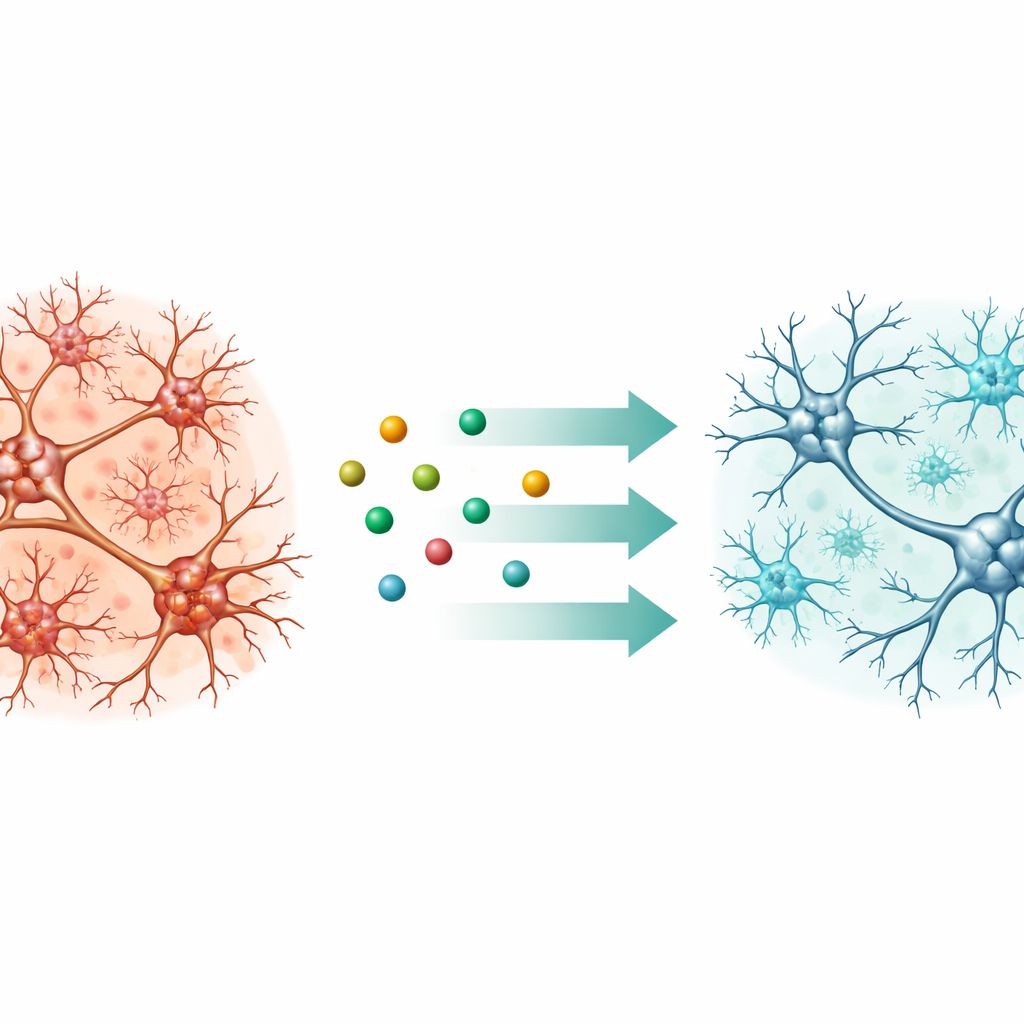
ماذا يمكن أن يعني هذا للعلاجات المستقبلية
تُظهر النتائج مجتمعة أن GV1001 يمكن أن يحسن الحركة والذاكرة، ويقلل تغيرات تاو السامة، ويحافظ على المشابك، ويخفف الالتهاب الدماغي في نماذج تحاكي جوانب رئيسية من PSP وأمراض أخرى يقودها تاو 4R. أشارت اختبارات سريرية مبكرة لدى أشخاص مصابين بالـ PSP بالفعل إلى تباطؤ في تدهور الأعراض وتحمل جيد، رغم الحاجة إلى دراسات أكبر وأطول بكثير. بالنسبة للمرضى والعائلات، تمنح هذه الدراسة تفاؤلاً حذراً بأن دواءً صُمم أصلاً للسرطان قد يعاد توظيفه لإبطاء مسار مرض دماغي سريع التقدم عن طريق استهداف الشذوذ البروتيني الجوهري فيه.
الاستشهاد: Jang, KB., Kang, D.M., Lee, MH. et al. GV1001 reduces pathological 4R tau and functional deficits in models relevant to progressive supranuclear palsy. Sci Rep 16, 8638 (2026). https://doi.org/10.1038/s41598-026-42195-7
الكلمات المفتاحية: الشلل فوق النووي التقدمي, بروتين تاو, اعتلال تاو 4R, الالتهاب العصبي, GV1001