Clear Sky Science · ar
تصوير التقدّم الخبيث: اختبار مناعي فلوري مكاني يعتمد على CD109 يحدد تحول سرطان الغدة الدرقية الحليمي إلى السرطان الخلوي الجاري داخل بيئة الورم
لماذا تهمنا هذه الدراسة عن سرطان الغدة الدرقية
يعد السرطان الخلوي الجاري في الغدة الدرقية أحد أكثر الأورام البشرية فتكاً، حيث يحوّل غالباً ورماً درقياً كان قابلًا للشفاء إلى مرض قاتل سريعاً. ومع ذلك، لا يفهم الأطباء تمامًا كيف يمكن لسرطان حليمي شائع وبطيء النمو أن يتحوّل فجأة إلى هذا الشكل العدواني. تتتبع هذه الدراسة ذلك التحوّل مباشرة داخل ورم المريض، مستخدمة تقنية تصوير جديدة لمراقبة كيف تتغير الخلايا السرطانية وجوارها البيئي خطوة بخطوة. يقدم العمل صورة أكثر تفصيلاً عن كيفية تأثير البيئة المحلية للورم في دفع الخلايا نحو حالة أكثر فتكاً، مما يلمّح إلى طرق جديدة لإبطاء أو منع هذا الانتقال.
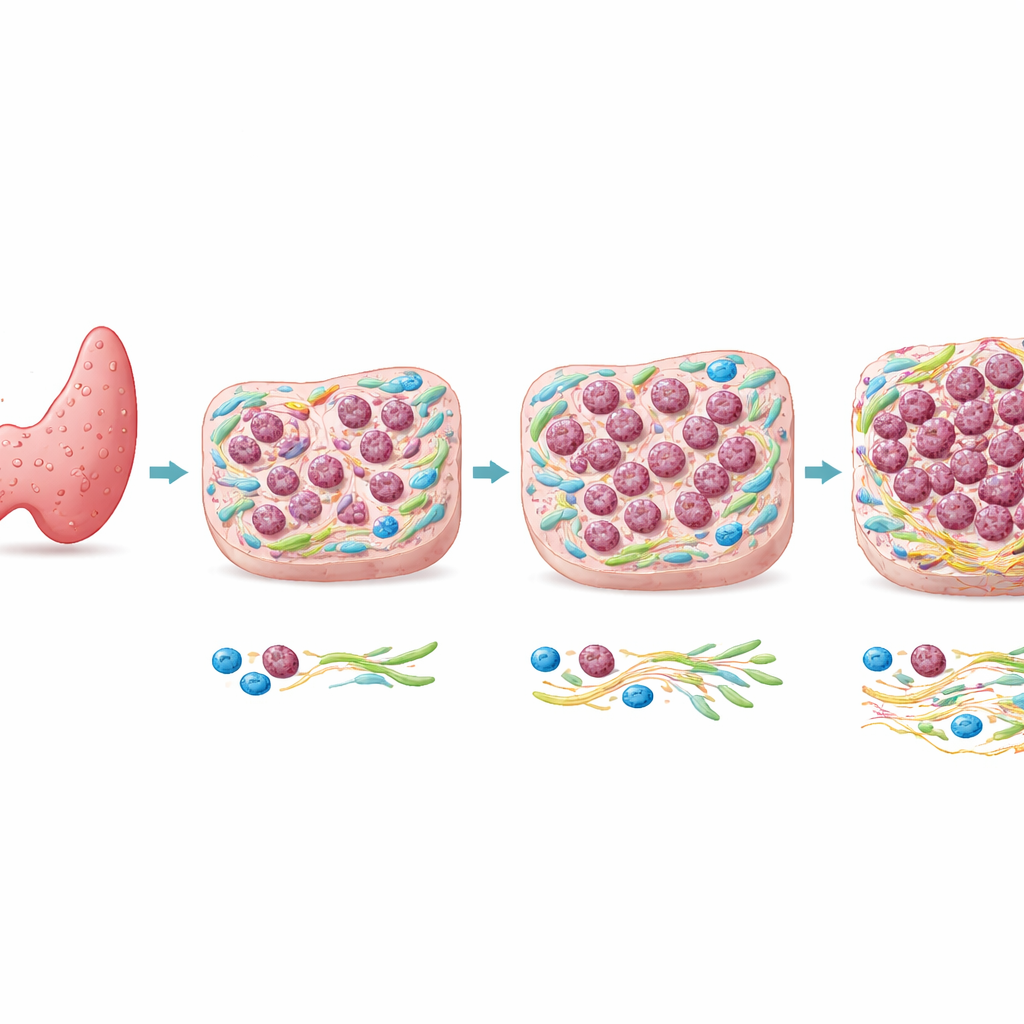
من ورم شائع إلى قاتل نادر
غالبية سرطانات الغدة الدرقية هي سرطانات حليمية، والتي تنمو عمومًا ببطء وتتمتع بنتائج جيدة. أما السرطان الخلوي الجاري، فهو نادر لكنه غالبًا ما يكون قاتلاً خلال أشهر. أظهرت الدراسات الجينية أن السرطان الخلوي الجاري والمنطقة الحليمية القريبة في نفس المريض غالبًا ما يشتركان في العديد من الطفرات الجينية نفسها، بما في ذلك تغييرات في جينات سرطان معروفة. تشير هذه الشبه إلى أن الجينات وحدها قد لا تفسر لماذا تصبح بعض مناطق الورم فقط خلوية جارية. لذلك ركّز المؤلفون على ما يحدث في المشهد النسيجي حول الخلايا—أي بيئة الورم الدقيقة—ليروا ما إذا كانت الظروف الموضعية تسهم في دفع هذا التحول الخطر.
طريقة جديدة لرسم خرائط السرطان في موضعه
طور الفريق اختبار تلوين مناعي فلوري مكاني (SPI)، وهو نوع من المجاهر متعددة الألوان التي تقيس سطوع بروتينات محددة في مربعات صغيرة محددة عبر مقطع نسيجي. ركّزوا هذه الطريقة على CD109، وهو بروتين سطحي حدّدوه كعلامة للسلوك الخبيث في نسيج الغدة الدرقية، وعلى CK8/18، وهو بروتين يميز خلايا الورم الحليمة الاعتيادية. من خلال حساب نسبة CD109 إلى CK8/18 في مئات المناطق الصغيرة، أنشأوا خرائط ملونة تفصل بوضوح مناطق الحليمي عن مناطق الخلوي الجاري وكشف، والأهم من ذلك، مناطق وسطية حيث تتداخل العلامتان. بدلاً من حدود حادة، بدا الانتقال من السرطان الحليمي إلى الخلوي الجاري كاستمرارية تدريجية ومرقطة.
خمس مناطق على طول مسار التغير
لفهم هذه الاستمرارية بشكل أفضل، قسّم الباحثون النسيج إلى خمس مناطق، من حليمي نقي إلى خلوي جاري متطور تمامًا. ثم فحصوا العديد من البروتينات الإضافية التي تعكس هوية الخلايا والنمو والحركة والأنسجة الداعمة. عبر هذه المناطق، تراجعت السمات الظهارية الكلاسيكية مثل E-cadherin وCK8/18 بشكل مطرد، في حين ارتفعت العلامات المرتبطة بحركية الخلية وتغير الشكل مثل الفيمينتين. كما ارتفعت البروتينات المشيرة إلى انقسام خلوي سريع في المناطق الأكثر خلوية. في الوقت نفسه، أصبحت الخلايا الداعمة المحيطة—الليفيات المرتبطة بالسرطان—والخلايا المناعية، وخصوصًا بعضالبلعمات، أكثر عددًا وأكثر نشاطًا، وزادت البروتينات التي تنتجها.
عندما يصبح هيكل الورم عدائيًا
حدث تغيير لافت في هيكلية الورم، أي المصفوفة خارج الخلية. في المناطق الخلوية، رسّبت خلايا شبيهة بالليف مزيدًا من أنواع الكولاجين III وVI وبروتين مصفوفة يُسمى TGFBI، وكانت هذه الألياف أسمك وأكثر تشابكًا وموجهة في اتجاهات متعددة بدلًا من خطوط سلسة وموازية. من المحتمل أن تجعل هذه الشبكة المعاد ترتيبها النسيج أكثر صلابة ميكانيكيًا. في هذه المناطق الأكثر صلابة، كان بروتين إشارة حساس للضغط يُدعى YAP أكثر نشاطًا في كل من الخلايا السرطانية والخلايا الداعمة. أظهرت نفس المناطق أيضًا المزيد من علامات تلف الحمض النووي وشكل من أشكال موت الخلايا الالتهابي، مع إطلاق بروتينات S100 التي يمكن أن تعمل كإشارات خطر وتزيد الالتهاب في البيئة. يقترح المؤلفون أن هذا المزيج من الضغط، وموت الخلايا، والالتهاب المزمن يفضّل بقاء وانتشار الخلايا السرطانية المتحولة التي تتحمل الإجهاد وتخضع لما يشبه انتقالًا ظهاريًا-متسامًا.
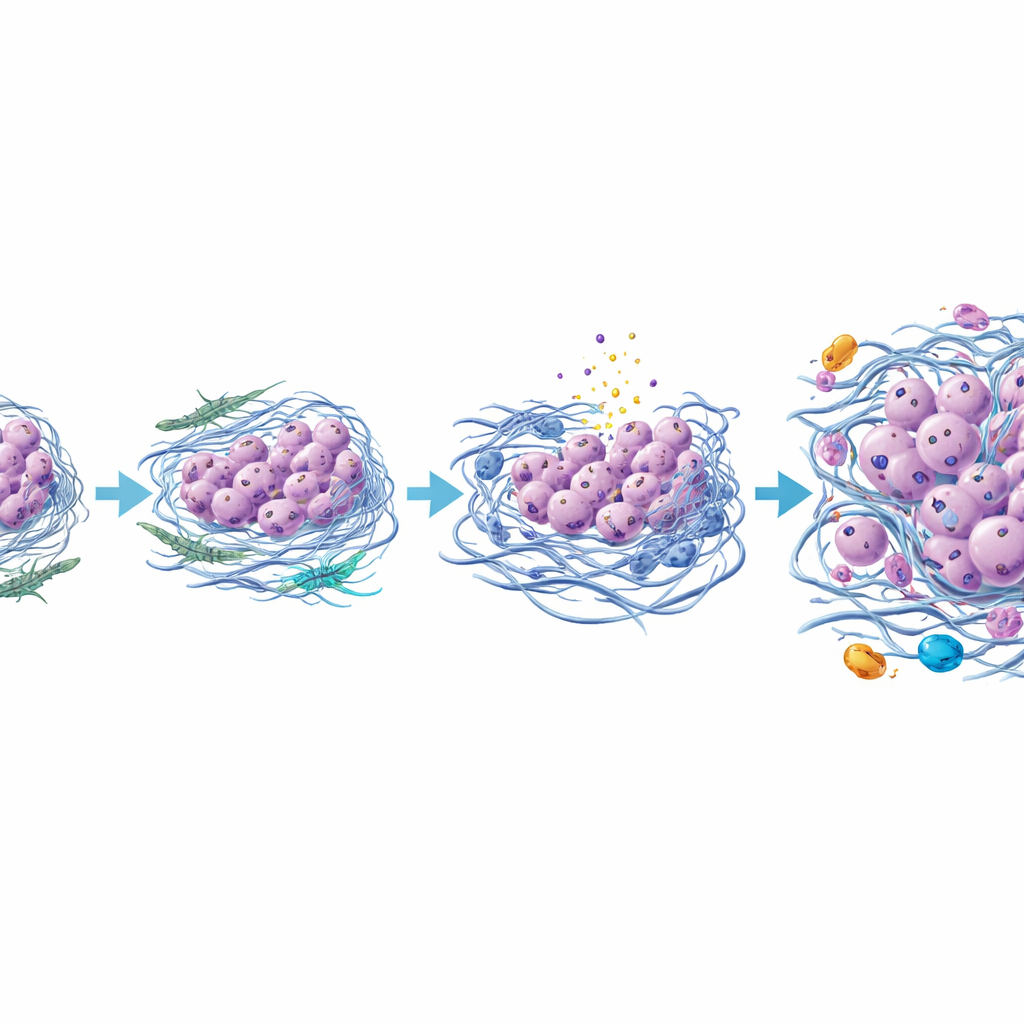
صورة جديدة لكيفية تحول ورم درقي إلى قاتل
عند تجميع هذه النتائج، تشير الدراسة إلى أن السرطان الخلوي الجاري في الدرقية يظهر ليس فقط نتيجة طفرات جينية إضافية بل من خلال إعادة تشكيل الحي المحيط بالورم. بينما تتفاعل خلايا الورم الحليمية والخلايا الداعمة القريبة، يتطور بعض الليفاويات إلى نوع أكثر عدوانية يثخّن ويصلب المصفوفة المحيطة، يضغط الخلايا الضعيفة لتموت، ويستدعي خلايا مناعية ملتهبة. الخلايا السرطانية الناجية والأكثر تحملًا تدريجيًا تفقد خصائصها الدرقية الأصلية وتتبنى هوية أكثر حركة وغزوًا، مشكلةً في النهاية ورمًا خلويًا جاريًا. وعلى الرغم من أن هذا العمل يستند إلى حالة واحدة مدروسة جيدًا ويحتاج إلى تأكيد في مزيد من المرضى، إلا أنه يقدم أداة تصوير قوية ونموذجًا مفصلاً يمكن أن يساعد استهداف الخلايا الداعمة للورم أو المصفوفة أو الإشارات الالتهابية في منع أو تأخير أحد أكثر التحولات المرعبة في سرطان الغدة الدرقية.
الاستشهاد: Cohen, T., Suzuki, K., Matsuda, K. et al. Visualizing malignant progression: in situ CD109-based spatial immunofluorescence assay delineates papillary to anaplastic thyroid carcinoma transformation within the tumor microenvironment. Sci Rep 16, 8682 (2026). https://doi.org/10.1038/s41598-026-41927-z
الكلمات المفتاحية: سرطان الغدة الدرقية الخلوي الجاري, سرطان الغدة الدرقية الحليمي, بيئة الورم الدقيقة, صلابة مصفوفة خارج الخلية, التلوين المناعي الفرّاغي المكاني