Clear Sky Science · ar
تحليل الحويصلات خارج الخلوية المشتقة من خلايا الظهارة القصبية باستخدام تقنيات التدفق الخلوي التقليدية، التصويرية والنانوية
لماذا تهم الفقاعات الصغيرة في الرئتين
تغطي خلايا بطانة الرئتين سطح المسالك الهوائية وتدير تواصلاً مستمراً مع الجهاز المناعي، خصوصاً عند استنشاق الغبار أو التلوث أو الجراثيم. جزء كبير من هذا "الحوار" يتم عبر فقاعات مجهرية تُسمى الحويصلات خارج الخلوية—حزم من الدهون والبروتينات تُفرَزها الخلايا. يمكن أن تفاقم هذه الحويصلات أو تخفف من أمراض الرئة، وربما تخدم مستقبلاً كإشارات إنذار مبكّرة لحالات مثل الربو، ومرض الانسداد الرئوي المزمن (COPD)، والتليف. تستكشف هذه الدراسة أفضل الطرق لقياس هذه الجسيمات المراوغة باستخدام أنواع مختلفة من الأجهزة الليزرية المتقدمة، بهدف جعل هذه القياسات عملية للبحث والاختبارات السريرية المستقبلية.
رسائل غير مرئية من خلايا المسالك الهوائية
الحويصلات خارج الخلوية (EVs) هي حزم صغيرة مغلفة بغشاء تفرزها تقريباً جميع الخلايا في سوائل مثل الدم والبول والغشاء السائل الرقيق المبطن للمسالك الهوائية. ارتبطت الحويصلات الناتجة من خلايا الظهارة القصبية البشرية—الخلايا التي تبطن القصبات الهوائية—بعمليات رئوية متعددة: فهي قد تؤثر على تطوّر الحساسية، تساعد في محاربة عدوى الرئة، تشكّل بنية المسالك الهوائية في مرض الانسداد الرئوي المزمن، وحتى تحد من تندب نسيج الرئة. وبحملها لقطع من البروتينات والدهون والمادة الوراثية من خلاياها الأصلية، يمكن أن تعمل الحويصلات كبصمات للحالة الصحية للرئة أو المرض، وقد تُستخدم لاحقاً كعلاجات بحد ذاتها. والتحدي أنها صغيرة للغاية، ومتباينة جداً، ومتواجدة بكميات منخفضة، مما يصعّب رؤيتها واحتسابها بدقة.
التخطي عن الاختبارات البطيئة والمجزأة
تقليدياً، اعتمد العلماء على عدة طرق منفصلة لدراسة الحويصلات. تُستخدم الطرد المركزي فائق السرعة أو فصل الحجم لعزلها؛ يقيس تحليل تتبع الجسيمات النانوية كيفية حركتها لتقدير الحجم والعدد؛ وتوفر الميكروسكوبات الإلكترونية صوراً مفصّلة. ومع أن هذه الطرق قوية، فهي بطيئة، وتستهلك وقتاً وجهداً، وليست مثالية للاستخدام الروتيني أو السريري. والأهم أنها ضعيفة في تحديد البروتينات المحددة على كل حويصلة. يوفر التدفق الخلوي—التقنية المستخدمة على نطاق واسع لتحليل الدم والخلايا المناعية—بديلاً أكثر سلاسة. يمرر التدفق الخلوي الجسيمات واحدة تلو الأخرى أمام الليزرات، فيقيس تشتت الضوء (المتعلق بالحجم) والفلورة (من الأصباغ أو الأجسام المضادة). تعد تصاميم الأجهزة الحديثة بدفع حدود التدفق الخلوي إلى مقياس أصغر الحويصلات، مما يفتح إمكانية أن تقوم آلة واحدة بقياس الحجم والعدد وتصنيف الحويصلات في تشغيل واحد.
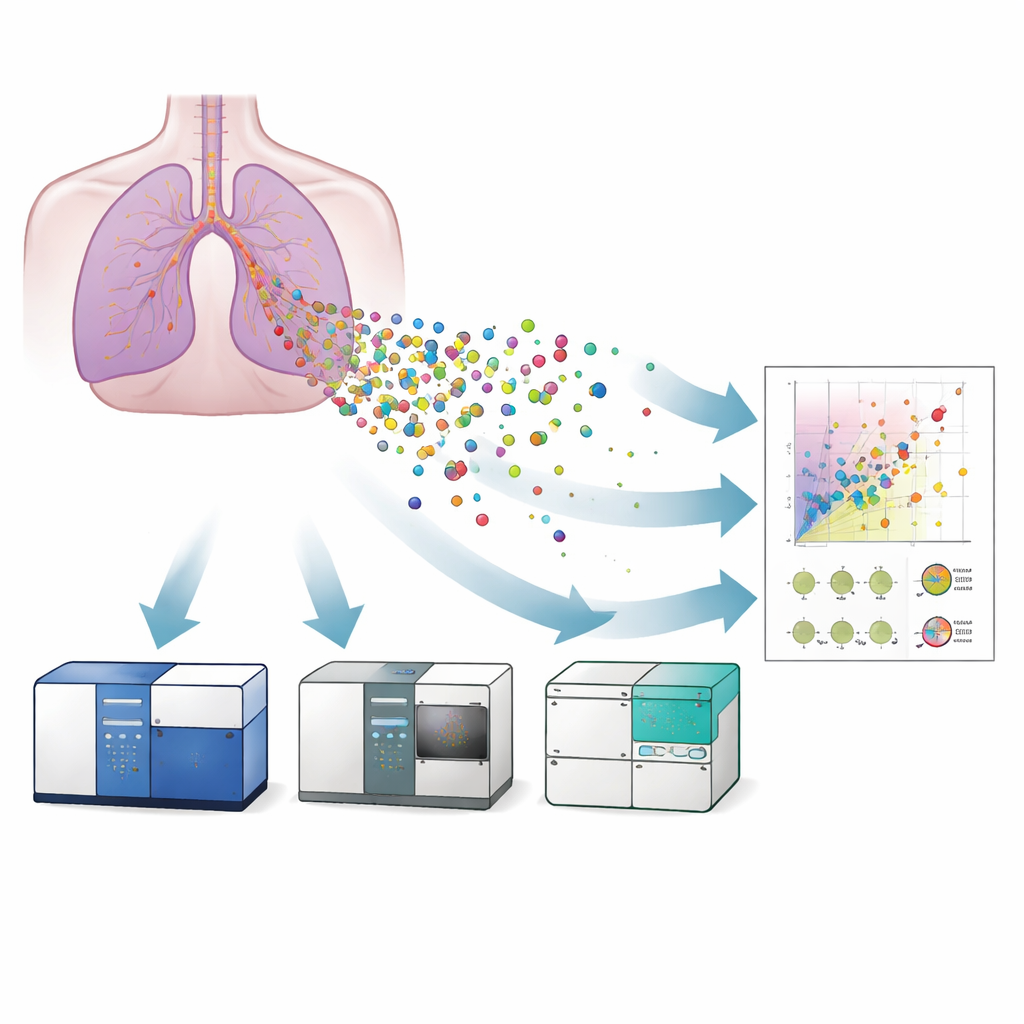
ثلاث آلات، هدف واحد
قارن الباحثون ثلاث نكهات من أجهزة التدفق الخلوي لدراسة الحويصلات المفرزة من نموذج مختبري لظهارة القصبات البشرية: جهاز تدفق خلوي تقليدي، جهاز تدفق خلوي تصويري، وجهاز تدفق خلوي بمقاييس نانوية. أولاً، أكدوا وجود الحويصلات وشكلها النموذجي باستخدام الميكروسكوب الإلكتروني والميكروسكوب فائق الدقة، الذي أظهر أيضاً أن الحويصلات تحمل بروتينات سطحية معروفة بالتتراسبانينز (CD9, CD63, CD81)—وهي علامات معيارية لتحديد EVs. ثم استخدموا خرزات مرجعية ومعايير ليبوزوم معايرة لتحويل إشارات الضوء في كل جهاز إلى أحجام تقريبية للحويصلات. استطاع جهاز التدفق الخلوي النانوي اكتشاف حويصلات صغيرة تصل إلى نحو 40 نانومتراً، والجهاز التصويري حتى نحو 55 نانومتراً، بينما كافح الجهاز التقليدي تحت نحو 120 نانومتراً. وهذا يعني أن الأنظمة الأكثر حساسية فقط هي القادرة على رصد أصغر الحويصلات بالكامل، والتي قد تكون الأكثر أهمية طبياً.
وضع علامات وعدّ الحويصلات
للتأكد من أنهم يقيسون حويصلات سليمة ونشطة بيولوجياً وليس حطاماً، استخدم الفريق صبغة تسمى calcein-AM. لا تتوهج هذه الصبغة إلا بعد عبورها غشاء سليم ومعالجتها بواسطة إنزيمات داخل الحويصلة. ضبطوا تركيز الصبغة بعناية بحيث تميّز الحويصلات بقوة مع تقليل الإشارة الخلفية، واستقروا على تركيز أعطى استجابات واضحة وخطية عبر تخفيفات العينات. ثم جمعوا الكالسيين مع أجسام مضادة فلورية ترتبط بالتتراسبانينز على سطح الحويصلة، مما مكن الأجهزة من فصل الحويصلات التي تحمل تركيبات مختلفة من هذه العلامات. كما قيّم الفريق حساسية كل جهاز تجاه هذه الوسوم الفلورية—كم عدد جزيئات الأجسام المضادة التي يجب أن تكون موجودة على الحويصلة حتى يمكن اكتشافها بثقة. عادة ما قدم التدفق الخلوي التصويري حدود كشف أدنى من الجهاز التقليدي، ما يجعله أنسب للجسيمات التي تحمل فقط عدداً قليلاً من بروتينات العلامة.
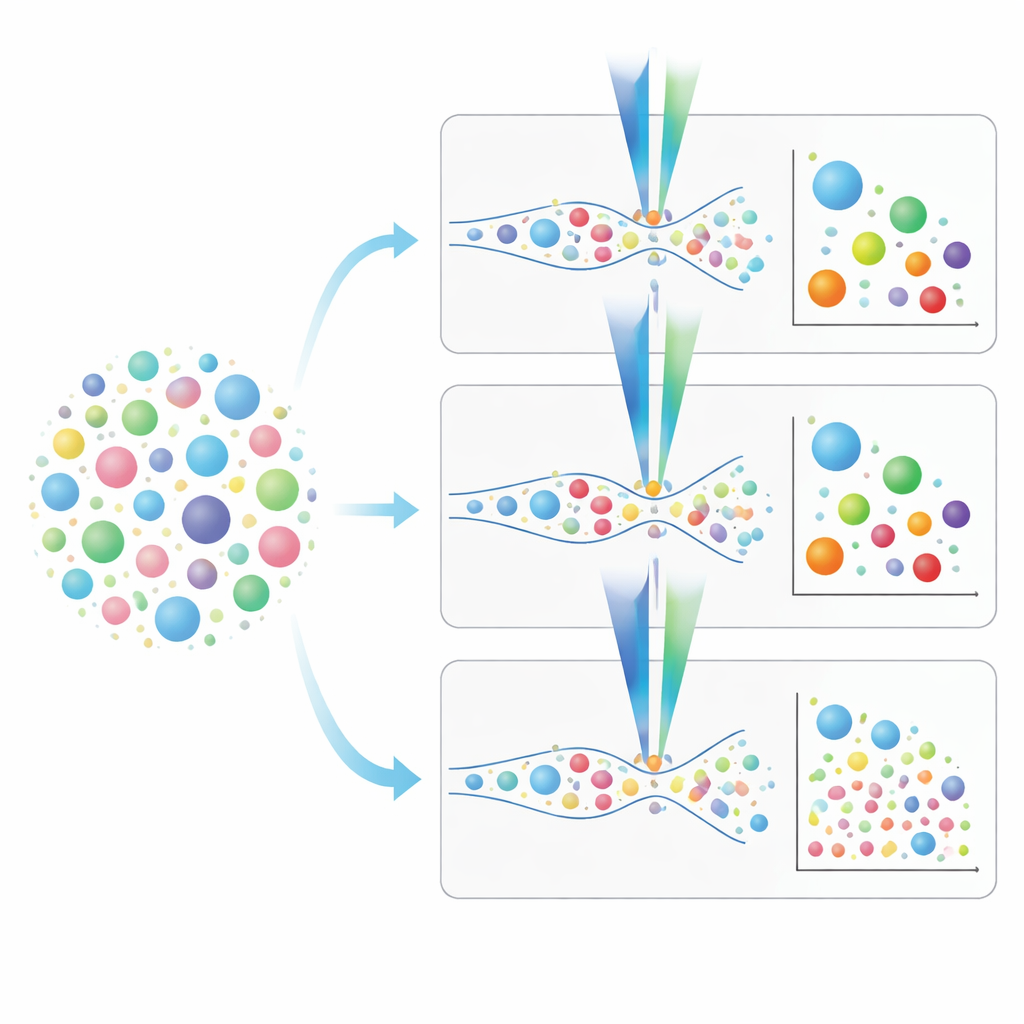
اختيار الأداة المناسبة لدراسات حويصلات الرئة
من هذا المقارنة المباشرة يبرز تصور عملي. أجهزة التدفق الخلوي التقليدية أسرع ويمكنها تحليل العينات دون عزل مسبق، لكنها تفوّت العديد من أصغر الحويصلات التي قد تحمل إشارات مرضية حاسمة. تتيح أجهزة التدفق الخلوي التصويرية والنانوية، رغم أنها أبطأ وفي حالة الجهاز النانوي تتطلب غالباً تنظيفاً مسبقاً للعينات، رؤية أحجام أصغر بكثير ودعم "بصمة" أغنى لعلامات سطح الحويصلة. يوضح المؤلفون استراتيجيات خطوة بخطوة للتلوين والمعايرة، ويؤكدون على أهمية معرفة حد اكتشاف كل وسم فلوري، ويعرضون كيف يتجنبون إشارات مضللة من أصباغ تؤشر أيضاً إلى شظايا أو جزيئات غير حويصلية. بعبارة بسيطة، يقدمون خارطة طريق للباحثين لاختيار الجهاز والبروتوكول الأنسب لأسئلتهم حول EVs الرئوية، مما يقرب المجال من استخدام هؤلاء الرسل المجهرية كأدوات عملية في فهم وتشخيص ومعالجة أمراض الجهاز التنفسي في المستقبل.
الاستشهاد: Hopkins, G., Browne, W., Tucis, D. et al. Bronchial epithelial cell-derived extracellular vesicle analysis using conventional, imaging, and nanoscale flow cytometry technologies. Sci Rep 16, 11162 (2026). https://doi.org/10.1038/s41598-026-41848-x
الكلمات المفتاحية: الحويصلات خارج الخلوية, ظهارة الرئة, التدفق الخلوي, أمراض الجهاز التنفسي, تحليل العلامات الحيوية