Clear Sky Science · ar
تقييم كمي خارج الجسم لدرجة الحرارة المستهدفة ومدة الاستئصال لتحسين بروتوكولات استئصال بالميكروويف باستخدام قياس الحرارة بالرنين المغناطيسي
مراقبة علاجات الأورام في الوقت الحقيقي
عندما يحرق الأطباء أورام الكبد بالحرارة، يرغبون في رؤية الأجزاء الدقيقة من العضو التي تُدمر أثناء الإجراء نفسه. يوفر التصوير بالرنين المغناطيسي طريقة لـ"رؤية الحرارة" داخل الجسم أثناء انتشارها. تستكشف هذه الدراسة مدى ارتفاع درجة الحرارة والمدة التي يمكن للأطباء تسخين نسيج الكبد فيها بأمان أثناء الاستئصال بالموجات الدقيقة مع الحصول في الوقت نفسه على خرائط درجة حرارة واضحة وموثوقة عبر الرنين المغناطيسي — وهي خطوة مهمة نحو علاجات سرطانية أكثر دقة وأقل توغلاً.
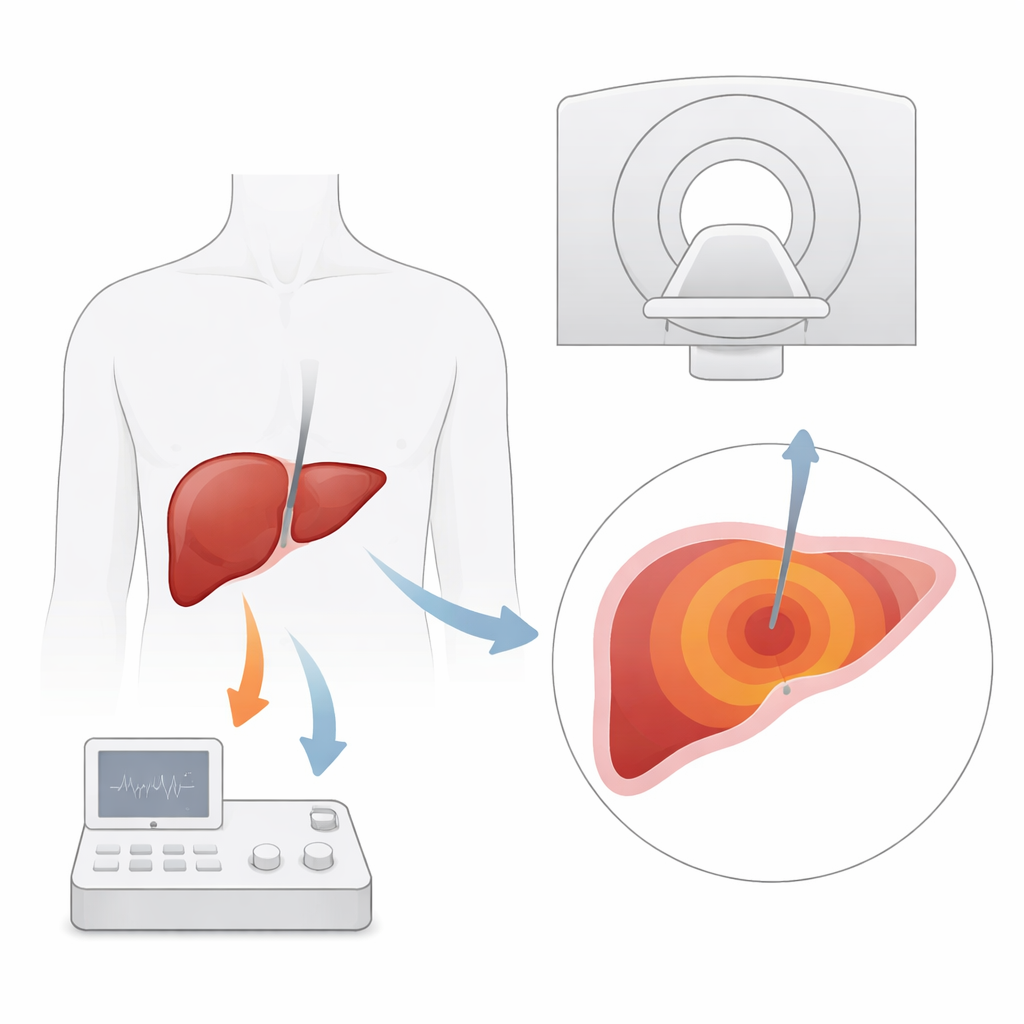
لماذا تحتاج علاجات الكبد الحرارية إلى رؤية أفضل
يستخدم الاستئصال بالموجات الدقيقة إبرة رفيعة لتوصيل طاقة تطهو وتقتل نسيج الورم داخل الكبد. يكون ذلك مهماً بشكل خاص للمرضى المصابين بسرطان الكبد أو النقائل الذين لا يمكنهم الخضوع للجراحة. تُوجّه أدوات التصوير التقليدية مثل الموجات فوق الصوتية والأشعة المقطعية مكان وضع الإبرة، لكنها تواجه صعوبة في إظهار الأورام الصغيرة بوضوح أو تتبع مدى انتشار الحرارة أثناء العلاج. يبرز الرنين المغناطيسي لأنه لا يكتفي بإظهار الأنسجة الرخوة بتفصيل عالٍ، بل يمكنه أيضاً قياس تغيرات الحرارة باستخدام خاصية جزيئات الماء. من الناحية النظرية، يسمح ذلك للأطباء بمراقبة خريطة حرارية للكبد في الوقت الحقيقي والتأكد من أن الورم بأكمله، بالإضافة إلى هامش آمن، قد دُمر.
متى تُعمي الحرارة النظر
عملياً، يمكن أن تصبح خرائط درجة الحرارة بالرنين المغناطيسي غير موثوقة عندما يسخن النسيج كثيراً. عند درجات حرارة عالية، يغلي الماء في النسيج مُشكِّلاً جيوب غازية صغيرة تُشوّه المجال المغناطيسي. تظهر هذه التشويهات كقراءات درجة حرارة خاطئة وأشكال غريبة على الخريطة، مما يصعّب معرفة أين تنتهي منطقة الاستئصال الحقيقية. افترض الباحثون أن استخدام درجات حرارة مستهدفة أقل قليلاً قد يعطي خرائط رنين مغناطيسي أنظف وأكثر موثوقية، حتى لو أدى ذلك إلى مناطق معالجة أصغر. كان هدفهم العثور على تراكيب من درجة الحرارة المستهدفة ومدة التسخين التي توازن بشكل أمثل بين وضوح الصورة وكفاية تدمير النسيج.
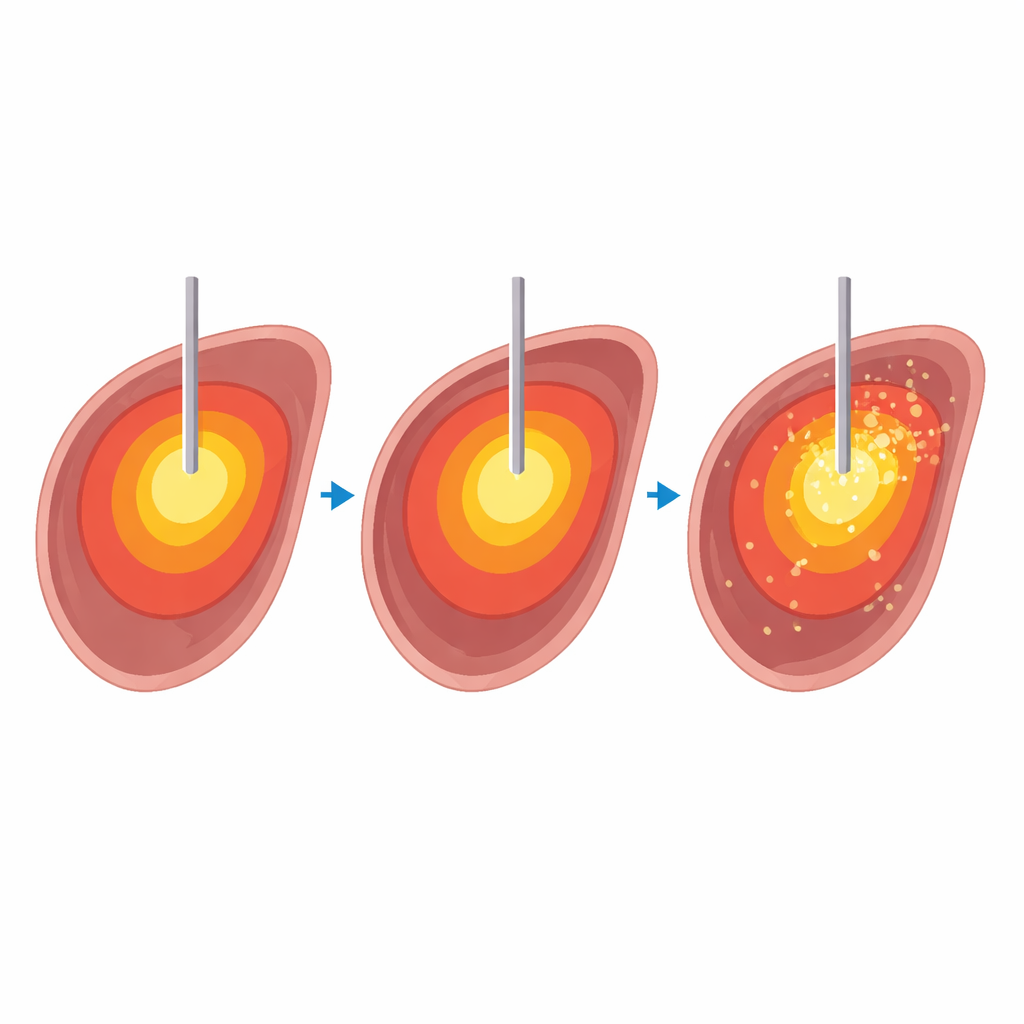
اختبار إعدادات الحرارة في أكباد حيوانية متبرع بها
لاستقصاء ذلك بأمان ودقة، نفّذ الفريق 32 استئصالاً بالموجات الدقيقة في عشرة أكباد بقرية أُزيلت بعد الذبح بفترة قصيرة. داخل ماسح رنين مغناطيسي بقوة 1.5 تسلا، سخّنوا نسيج الكبد إلى أربع درجات حرارة مستهدفة — 60 و80 و100 و120 درجة مئوية — لفترات زمنية مختلفة بين 5 و15 دقيقة. خلال كل استئصال، أنتج تسلسل رنين مغناطيسي سريع خرائط ثلاثية الأبعاد للحرارة و"الجرعة الحرارية" كل بضع ثوانٍ. بعد التسخين، قُطعت الأكباد على طول مسار الإبرة، وقِيسَت مساحات النسيج الميت المرئية وقورنت بالمساحات المتوقعة حسب خرائط الرنين المغناطيسي. قيّم اثنان من أخصائيي الأشعة جودة خرائط الرنين المغناطيسي على مقياس من خمس نقاط، مع مراعاة مدى استدارة وانتظام المنطقة المسخنة ومدى تداخل التشويهات الناتجة عن الغاز والإبرة.
حروق أبرد، خرائط أوضح
أظهرت التجارب تقايضاً واضحاً. أدت درجات الحرارة الأعلى إلى مناطق أكبر من النسيج الميت، كما يُتوقع، لكن خرائط درجة الحرارة بالرنين المغناطيسي تدهورت بشكل ملحوظ فوق 100 درجة. عند هذه الإعدادات الأكثر حرارة، أصبحت أشكال الاستئصال أكثر انتظاماً، وتسببت تشويهات الغاز في قراءات تظهر انخفاضاً في درجات الحرارة أو حتى قيماً سالبة بالقرب من الإبرة. بالمقابل، كانت خرائط الرنين المغناطيسي عند 60 و80 درجة أكثر سلاسة ودائرية ومواءمة أفضل مع أحجام الآفة الحقيقية الظاهرة في شرائح النسيج. أكدت التحليلات الإحصائية توافقاً قوياً بين المساحات المشتقة من الرنين المغناطيسي والنخر الفعلي عند درجات الحرارة الأدنى، مع تضعف الارتباطات أو اختفائها عند درجات الحرارة الأعلى. عوضت زيادة مدة التسخين جزئياً انخفاض درجة الحرارة من حيث الضرر الإجمالي، لكنها لم تستطع مطابقة أكبر الآفات الملاحظة عند 120 درجة بشكل كامل.
استراتيجية من خطوتين لاستئصال أكثر أماناً وذكاءً
استناداً إلى هذه النتائج، يقترح المؤلفون حل وسط عملي للعلاجات المستقبلية الموجهة بالرنين المغناطيسي. قدّم طور تسخين أولي عند نحو 80 درجة مئوية لمدة 15 دقيقة توازناً جيداً: كانت جودة الصورة عالية، وكانت منطقة الاستئصال كبيرة إلى حد معقول، وأظهرت دراسات النسيج موتاً خلوياً فعالاً. للحالات التي تتطلب مناطق معالجة أكبر، يقترحون نهجاً من خطوتين: ابدأ بمرحلة ذات درجة حرارة أقل لرسم خريطة حرارية واضحة والتحقق من التغطية، ثم، بمجرد أن تبدو الموضعية والهواشي مُرضية، زدّ درجة الحرارة في مرحلة ثانية لتوسيع المنطقة الميتة، مع قبول أن خريطة الحرارة ستكون أقل موثوقية أثناء هذه الزيادة النهائية.
ماذا يعني هذا لرعاية المرضى المستقبلية
بالنسبة لغير المتخصص، الرسالة الأساسية هي أن "خفض الحرارة قليلاً" يمكن أن يجعل بالفعل العلاجات الحرارية للسرطان أكثر أماناً ودقة — على الأقل في إعدادات المختبر المُتحكَّم بها. أعطت درجات الحرارة المستهدفة الأدنى خرائط حرارة بالرنين المغناطيسي أوضح بكثير، مما سَهّل رؤية المكان الذي دُمر فيه النسيج فعلياً. الجانب السلبي هو أن الحروق الأبرد تنتج آفات أصغر، لذلك قد يحتاج الأطباء إلى علاجات أطول أو متعددة الخطوات لتغطية أورام كبيرة. ونظراً لأن هذا البحث أُجري في أكباد حيوانية غير حية دون تدفق دم أو حركة تنفس، فهناك حاجة إلى مزيد من العمل على المرضى. ومع ذلك، تشير الدراسة إلى بروتوكولات علاجية تستخدم الرنين المغناطيسي ليس فقط لتوجيه الإبرة، بل لمراقبة وضبط الحرق في الوقت الحقيقي، مما قد يحسّن النتائج للأشخاص المصابين بأورام الكبد.
الاستشهاد: Nardone, L., Tan, A.S.M., Bour, P. et al. Quantitative ex vivo assessment of target temperature and ablation duration for protocol optimization of microwave ablation procedures with mr thermometry. Sci Rep 16, 8153 (2026). https://doi.org/10.1038/s41598-026-41656-3
الكلمات المفتاحية: الاستئصال بالموجات الدقيقة, قياس حرارة بالرنين المغناطيسي, سرطان الكبد, الاستئصال الحراري, العلاج الموجَّه بالصور