Clear Sky Science · ar
لا يُعدل DUSP29 تداخلات الورم الميلانيني–خلية العضلة في نموذج زراعة مشتركة للعضلات الهيكلية
لماذا تهم مقاومة العضلات لانتشار السرطان
عندما ينتشر السرطان في الجسم، فإنه غالبًا ما يستقر في أماكن مثل الرئتين أو الكبد أو العظام. ومن الغريب أن عضلاتنا الهيكلية — التي تشكل معًا حوالي نصف وزن الجسم — نادرًا ما تكون موطنًا لهذه البؤر الخطيرة. لقد أثار هذا اللغز اهتمام الأطباء والعلماء لأكثر من قرن. تبحث الدراسة الملخّصة هنا سؤالًا محددًا داخل ذلك اللغز الأكبر: هل خلايا العضلات نفسها، وبروتين غني في العضلات يُدعى DUSP29، يكبحان الخلايا السرطانية مباشرةً، أم أن حماية العضلات تعود لسبب مختلف تمامًا؟
مكان هبوط نادر للخلايا السرطانية المتجولة
يُشاهد الأطباء عددًا أقل بكثير من حالات الانبثاث في العضلات الهيكلية مقارنةً بالعديد من الأعضاء الأخرى، حتى لدى أشخاص انتشر لديهم السرطان على نطاق واسع. إحدى الأفكار أن خلايا العضلات تخلق بيئة غير مرحبة بالخلايا الورمية القادمة، ربما بإرسال إشارات كيميائية أو إجبار الخلايا السرطانية على تغيير سلوكها. أشارت أعمال سابقة في الفئران إلى أنه عندما تنمو خلايا سرطان الجلد (الميلانوما) بجوار خلايا عضلية غير ناضجة، فإنها تفقد بعض صبغتها وحتى تبدأ في التشابه مع نسيج العضلة. وبناءً على ذلك، توجه المؤلفون إلى بروتين محدد، DUSP29، الموجود بمستويات أعلى بكثير في العضلات مقارنةً بمواقف أخرى وينتمي إلى عائلة من الإنزيمات المعروفة بالتحكم في مسارات النمو والبقاء التي تختطفها السرطانات في كثير من الأحيان.
اختبار لقاءات العضلة–الورم في طبق مخبري
لفحص هذه الأفكار، بنى الباحثون نموذجًا مختبريًا مسيطرًا باستخدام سطرين خلويين فأريين معروفين جيدًا: خلايا ميلانوما (B16F10) وخلايا مسبقة للعضلات، أو الخلايا العضلية الوليدة (C2C12). مزجوا هذين النوعين من الخلايا في أطباق مشتركة بنِسب مختلفة، بدءًا من أعداد متساوية إلى حالات تفوق فيها الخلايا العضلية الخلايا الورمية بشكل كبير. في بعض التجارب لامست الخلايا بعضها البعض مباشرة؛ وفي أخرى، عُمّرت خلايا الميلانوما في وسط النمو السائل المأخوذ من مزارع الخلايا العضلية فقط، ما يلتقط أي عوامل ذائبة أفرزتها خلايا العضلات. على مدى عدة أيام، قاس الفريق عدد الخلايا الحية والمنقسمة باستخدام اختبار قياسي يغير لونه، وفحصوا علامات الموت المبرمج للخلايا باستخدام قياس التدفق الخلوي، وهي تقنية تميّز بين الخلايا الحية والميتة والآخذة في الموت.
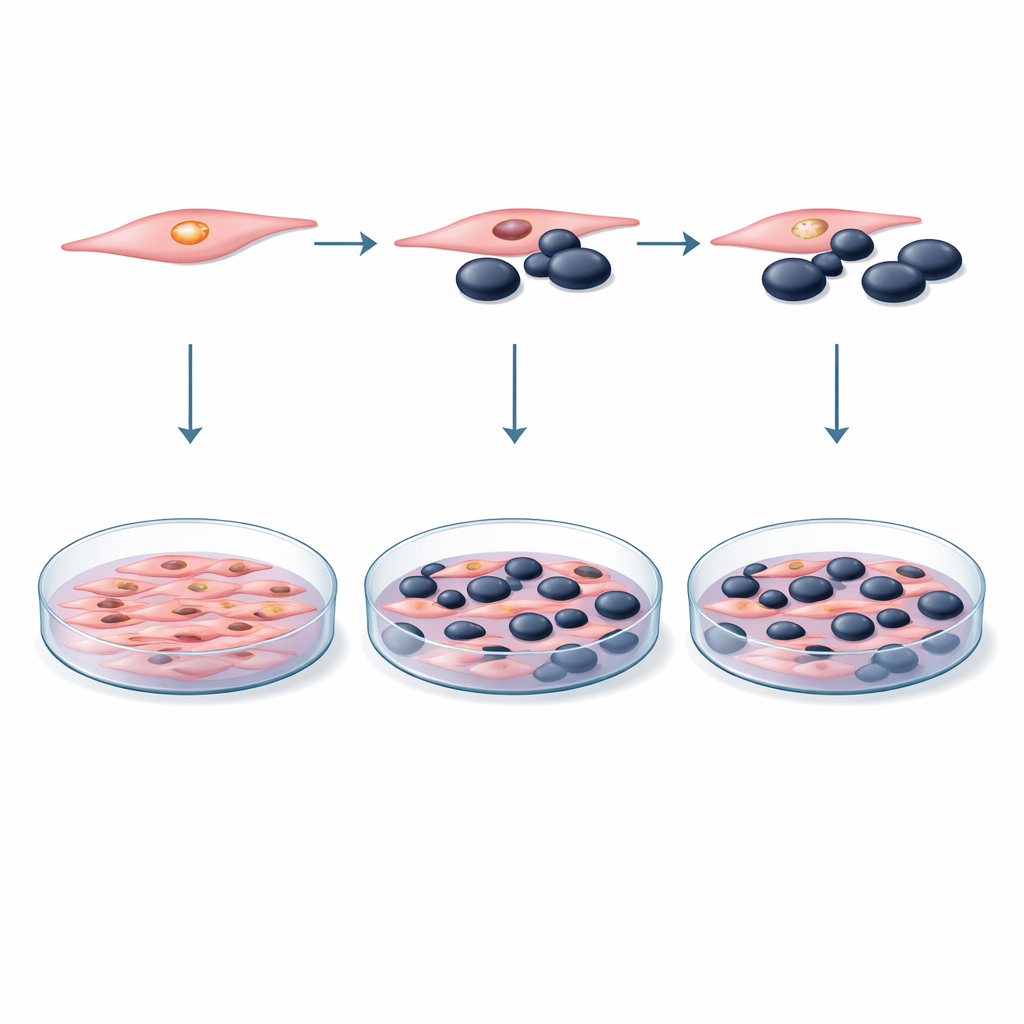
وضع DUSP29 تحت المجهر
ركز الذراع الثاني من الدراسة على DUSP29 نفسه. أولًا، أكّد العلماء أن الخلايا العضلية الوليدة تُنتج رسالة هذا البروتين الجيني بمستويات معتبرة. ثم استخدموا الحمض النووي الريبي الصغير المتداخل (siRNA) — مقاطع جينية قصيرة تعمل كمفاتيح "إيقاف" مستهدفة — لخفض مستويات DUSP29 في خلايا العضلات بشكل حاد. أظهرت الضوابط الدقيقة أن مواد التوصيل وsiRNA الضابطة لم تضر الخلايا بحد ذاتها. بعد خفض DUSP29، نمت الخلايا العضلية المعدلة مرة أخرى مع خلايا الميلانوما، أو تم تطبيق وسط نموها على مزارع الميلانوما. تكررت نفس الاختبارات لقياس بقاء الخلايا وموتها عبر نقاط زمنية متعددة لمعرفة ما إذا كان إسكات هذا البروتين الغني في العضلات سيُرجّح الكفة لصالح الخلايا الورمية أو ضدها.
عندما يكون عدم الحدوث هو النتيجة المهمة
عبر كل هذه التجارب، كان المخرج لافتًا في غيابه عن الدراما. سواء نمت خلايا الميلانوما بمفردها أو إلى جانب الخلايا العضلية الوليدة، مع اتصال مباشر أو بدونه، بقي بقاءها دون تغيير يذكر ضمن تباينات التجربة العادية. لم تُحدث الزراعة المشتركة موتًا إضافيًا في خلايا الميلانوما، ولا عززت نموها. ولم يُغير خفض DUSP29 في الخلايا العضلية أيضًا من قابلية خلايا الميلانوما للحياة، على الرغم من أن نشاط الجين في الخلايا العضلية انخفض بشكل كبير. بعبارة أخرى، ضمن هذه الشروط المبسطة والقصيرة الأمد، لم تُوجّه الجوار مع الخلايا العضلية الوليدة ولا وجود أو غياب DUSP29 خلايا الميلانوما بشكل ملحوظ نحو البقاء أو الزوال.
ماذا تعني هذه النتائج للغز العضلة–السرطان
تشير النتائج إلى أن الحماية النسبية للعضلات الهيكلية من الانبثاث من غير المرجح أن تنجم عن حوار مباشر بسيط بين خلايا الميلانوما والخلايا العضلية القريبة، أو عن عمل DUSP29 بمفرده في هذا التفاعل المبكر. بدلاً من ذلك، يرجح أن تنتج مقاومة العضلات عن مزيج أكثر تعقيدًا من الخصائص — بنية كثيفة، القوى الميكانيكية للانقباض، كيمياء أيضية مميزة، وعدد كبير من الجزيئات الإشارية الأخرى التي لم تُلتقط في هذا النظام القائم على الأطباق. من خلال إظهار بوضوح المكان الذي لا تعمل فيه آلية معقولة، تساعد هذه الدراسة في تضييق نطاق البحث عن كيفية حفاظ العضلات على بقاء معظم السرطانات المنتشرة بعيدًا، وتوجّه الدراسات المستقبلية نحو نماذج نسيجية أكثر واقعية، وأنواع أورام مختلفة، والبيئة الأوسع التي تلتقي فيها خلايا العضلة والسرطان.
الاستشهاد: Ön, S., İlhan, H.A., Günenç, D. et al. DUSP29 does not regulate melanoma–myoblast interactions in a skeletal muscle co-culture model. Sci Rep 16, 8372 (2026). https://doi.org/10.1038/s41598-026-41300-0
الكلمات المفتاحية: انبثاث العضلات الهيكلية, الميلانوما, تداخلات الورم–العضلة, DUSP29, البيئة الدقيقة للورم