Clear Sky Science · ar
دور التهابية NLRP3 في تنوع الضعف المعرفي أثناء الشيخوخة وبعد حقن LPS في الفئران
لماذا لا تتباطأ أدمغة وأجسام المسنين بالطريقة نفسها
مع تقدم الناس في العمر، يبقى بعضهم يقظين ونشيطين بينما يصبح آخرون ضعفاء بدنيًا وبطيئين ذهنيًا. يسمي الأطباء هذا التدهور المشترك «الضعف المعرفي»، وهو يزيد بشكل كبير من خطر العجز والخرف. تستخدم هذه الدراسة الفئران للإجابة عن سؤالين رئيسيين: لماذا يختلف الضعف المعرفي كثيرًا بين الأفراد، وإلى أي مدى يمكن عزوه إلى التهاب خافت داخل الدماغ؟ من خلال تفكيك آثار الشيخوخة الطبيعية عن الالتهاب الناتج عن تحدٍ مناعي، تستكشف الورقة ما إذا كانت نوبات المرض القصيرة تحاكي بالفعل ما يحدث في الدماغ أثناء الشيخوخة الطويلة الأمد.
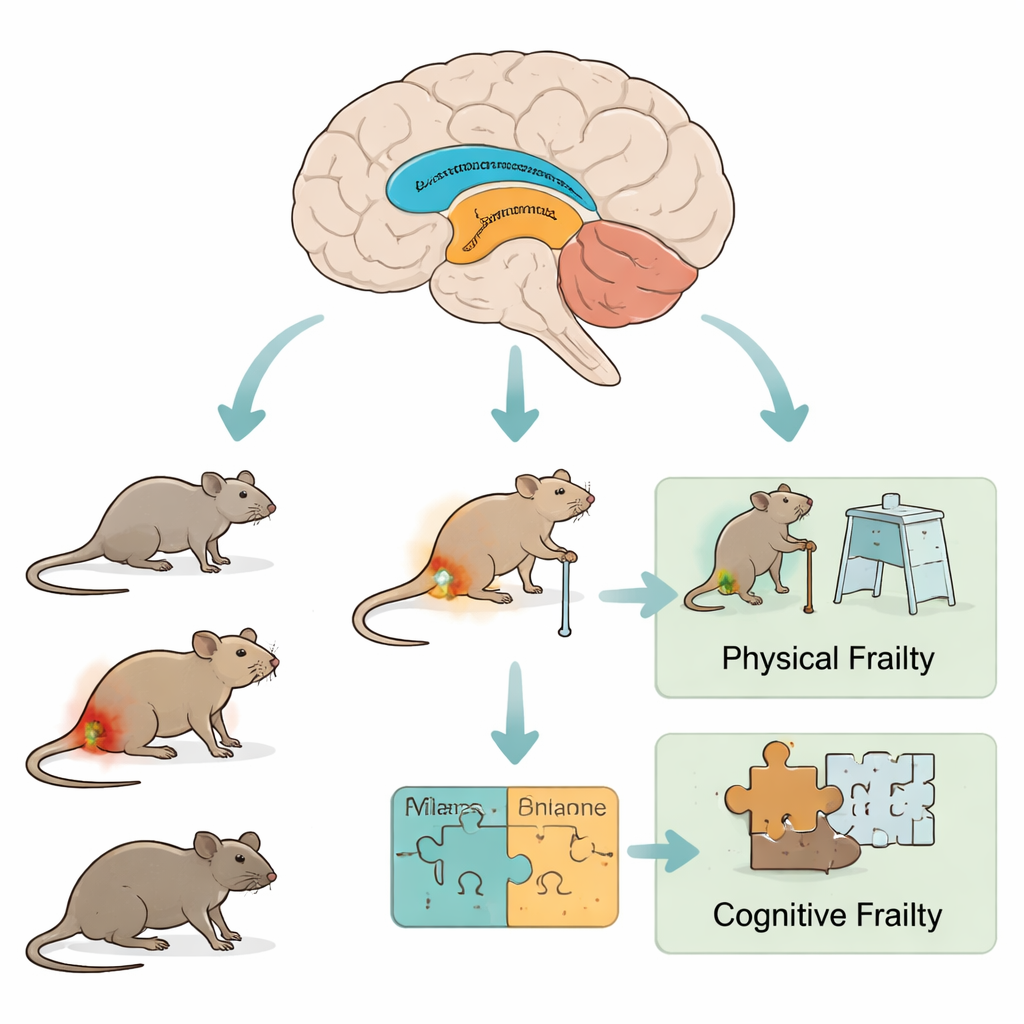
مسارات مختلفة للشيخوخة في المختبر
قارن الباحثون ثلاث مجموعات من الفئران الذكور: بالغون أصحاء، وحيوانات مسنة طبيعيًا، وبالغون تلقوا حقنة واحدة من مادة بكتيرية (LPS) تهيج الجهاز المناعي لفترة قصيرة. على مدى خمسة أيام قاسوا وزن الجسم، وقوة القبضة، والحركة، والتوازن على قضيب دوار، والاستكشاف في مساحات مفتوحة، والقدرة على التعرف على جسم جديد. أتاحت هذه الاختبارات المتنوعة للفريق تسجيل كلٍّ من الصلابة البدنية والمشكلات المعرفية الطفيفة. في نهاية الاختبارات، فحصوا الحُصين واللوزة الدماغية—منطقتين مهمتين للذاكرة والعاطفة—للبحث عن علامات التهاب وتلف خلوي مرتبط بالشيخوخة.
طرق جديدة لقياس «ضعف الجسم والعقل»
للانتقال إلى ما هو أبعد من تسميات نعم-أو-لا، جمع المؤلفون نتائج العديد من الاختبارات في عدة درجات رقمية. التراكيب المعيارية للضعف التقطت مشكلات جسدية مثل تغير الوزن، البطء، ضعف القبضة، وانخفاض النشاط. بالإضافة إلى ذلك، أنشأوا مؤشر الضعف المعرفي (CogFI) الذي يمزج الدرجات البدنية مع مقاييس التعلم والذاكرة والدافع الاستكشافي. هذا المؤشر الجديد تمكن من إظهار مدى اختلاف أداء الحيوانات عن بعضها البعض، خاصة بين الفئران المسنة، حيث أدت بعض الحيوانات تقريبًا مثل البالغين الشباب بينما أظهر آخرون تدهورًا مشتركًا واضحًا.
ما يمكن وما لا يمكن أن تحاكيه المرضات قصيرة الأمد
الفئران البالغة التي تعرضت لـ LPS فقدت الوزن بسرعة، وأصبحت أضعف، وتحركت أقل، واستكشفت محيطها بتردد. في العديد من درجات الضعف المعيارية، بدت متضررة على الأقل بقدر الحيوانات المسنة. لكن هذه التغيرات كانت عابرة: بدأت الحركة وتعلم المهارات الحركية في التعافي خلال بضعة أيام. والأهم أن LPS لم يرفع مؤشرات الشيخوخة الخلوية في الحُصين، ولم يسبب ارتفاعًا مستمرًا لمستشعر التهابي رئيسي يُدعى NLRP3. بالمقابل، ارتبطت الشيخوخة الطبيعية بوجود خلايا أكثر شيخوخة وارتفاع واضح في مستويات NLRP3 في الحُصين، رغم أن بعض المقاييس البدنية الأساسية ظلت محفوظة إلى حد ما.
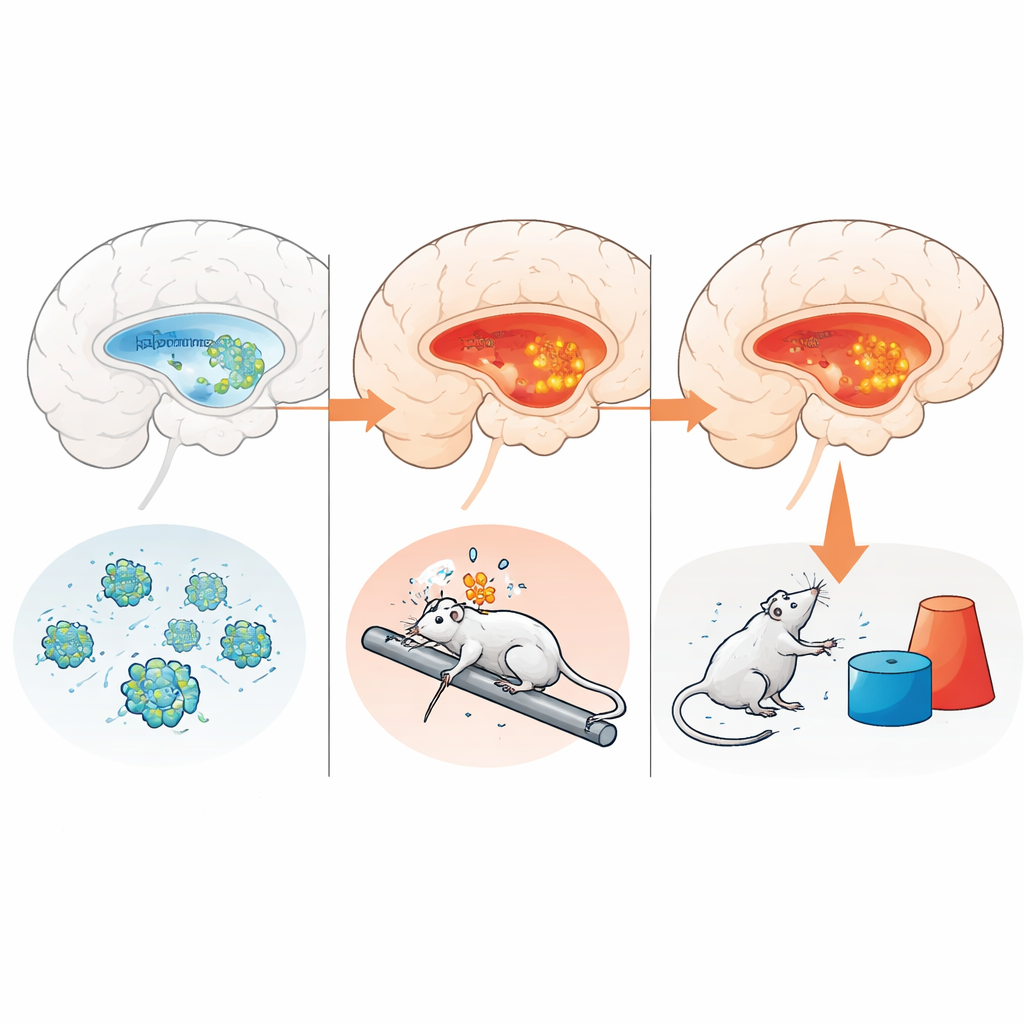
دوائر الذاكرة الملتهبة والضعف الخفي
من خلال مطابقة كيمياء الدماغ مع السلوك، وجد الفريق أن المستويات الأعلى من البروتينات المرتبطة بـNLRP3—وخاصة الإنزيم كاسبيز-1—في الحُصين ارتبطت بدرجات ضعف أسوأ. كانت هذه الروابط قوية للمؤشرات المدمجة التي تشمل السمات البدنية والمعرفية معًا، لكنها لم تكن قوية للمقاييس المعرفية وحدها أو للبروتينات المقاسة في اللوزة. بعبارة أخرى، يبدو أن تنشيط الماكينات الالتهابية المزمن في منطقة دماغية حاسمة للذاكرة مرتبط ارتباطًا وثيقًا بالضعف العام للجسم والعقل. الفئران المعالجة بـLPS، المقاسة بعد تعافيها إلى حد كبير، لم تُظهر هذا التوقيع الدماغي المستمر، مما يؤكد الفرق بين الضربات المناعية القصيرة الأمد والشيخوخة طويلة المدى.
ماذا يعني هذا لفهم الشيخوخة الصحية
تشير هذه الدراسة إلى أن الضعف المعرفي ليس مجرد مسألة أعمار أو التعرض لمرض مؤخرًا. بل إنه يعكس تراكمًا بطيئًا وغير متساوٍ من التلف والالتهاب في دوائر دماغية محددة، لا سيما في الحُصين. يقدم مؤشر الضعف المعرفي المقترح وسيلة حساسة لتتبع هذا التدهور المشترك في نماذج الحيوانات، فاتحًا الباب لاختبار علاجات تستهدف التهاب الدماغ. بينما يمكن لضربة التهابية واحدة أن تجعل كائنًا صحيًا يبدو هشًا مؤقتًا، لم تُعدِّد إلا الشيخوخة الطبيعية التغيرات الخلوية الأعمق والالتهاب الدماغي المستمر المرتبط بالضعف الدائم. بالنسبة للناس، يشير ذلك إلى أهمية مواجهة الالتهاب المزمن منخفض الدرجة على مدار الحياة للمساعدة في الحفاظ على الاستقلالية البدنية والوضوح الذهني.
الاستشهاد: Komleva, Y., Lukyanchuk, A., Blagova, A. et al. The role of NLRP3 neuroinflammation in cognitive frailty diversity during aging and after LPS administration in mice. Sci Rep 16, 9100 (2026). https://doi.org/10.1038/s41598-026-41104-2
الكلمات المفتاحية: الضعف المعرفي, التهاب الدماغ, الشيخوخة, مجمع الالتهاب NLRP3, سلوك الفأر