Clear Sky Science · ar
التأثيرات السامة للخلايا لمركب نانوي من الكيتوزان/السيلينيوم معدل بحمض الجليسيرريزينيك على سلالة خلايا سرطان الساركومة العظمية
أمل جديد لعلاج سرطان العظام
الساركومة العظمية، أكثر أنواع سرطان العظام شيوعًا لدى المراهقين والشباب، تشتهر بصعوبة علاجها دون إلحاق ضرر بالأنسجة السليمة. تستكشف هذه الدراسة نوعًا جديدًا من الجسيمات الدقيقة المصممة التي تهدف إلى مهاجمة خلايا الورم بدقة أكبر مع الحفاظ على خلايا العظام الطبيعية. من خلال الجمع بين معدن يحتاجه الجسم، وبوليمر طبيعي قائم على السكر، ومركب من عرق السوس، بنى الباحثون «حزمة نانوية» ذكية مصممة لدفع خلايا السرطان نحو نمط انتحار خلوي منظم بدلاً من التسبب بموت خلوي فوضوي والتهاب مصاحب.
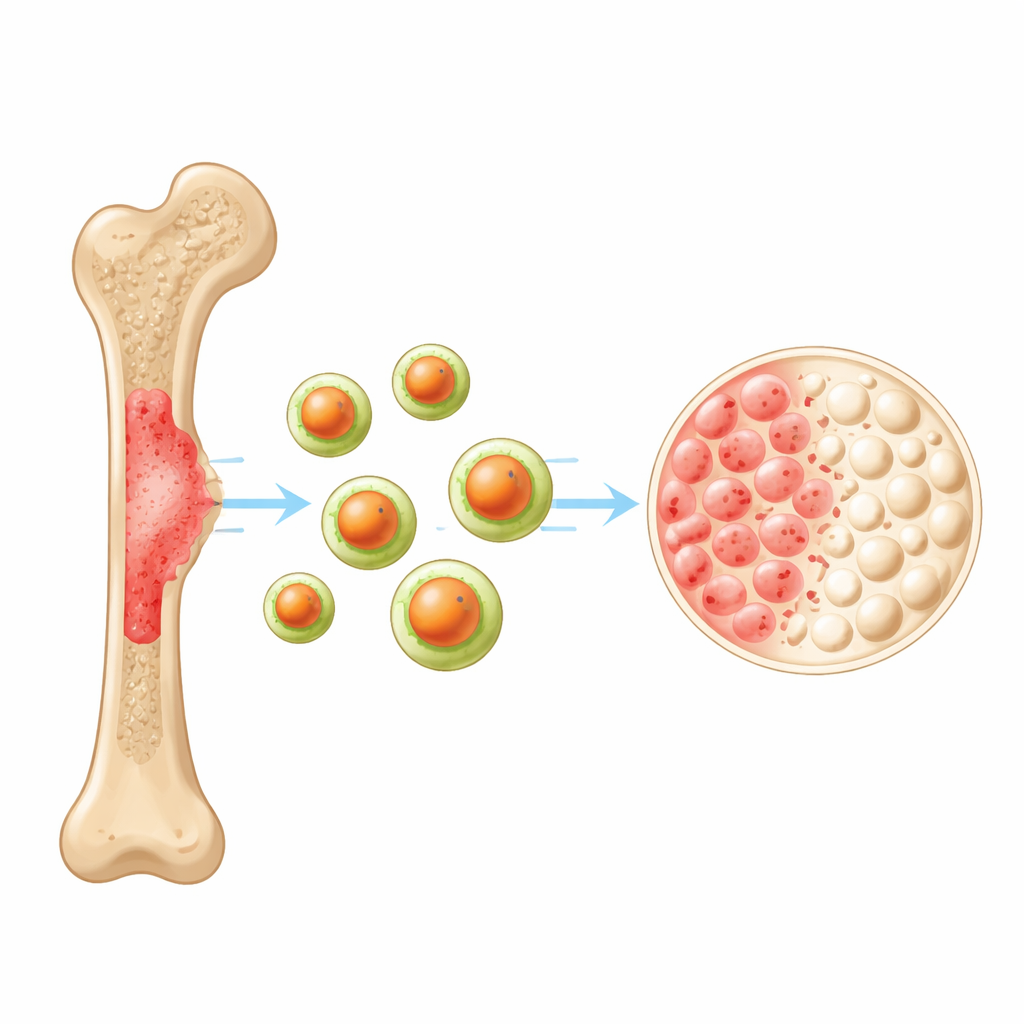
بناء مقاتل نانوي ثلاثي الطبقات
أنتج الفريق جسيمات نانوية بثلاث مكونات رئيسية. في النواة يوجد السيلينيوم، عنصر أثرى معروف بقدرته على إلحاق الضرر بخلايا السرطان عبر زيادة جزيئات الأكسجين الضارة داخلها. هذا اللب مغطى بطبقة من الكيتوزان، وهو بوليمر حيوي مستخلص من مصادر طبيعية مثل القشريات، يساعد على استقرار الجسيمات في الماء ويحسن قدرتها على دخول الخلايا. أخيرًا، تم تعديل السطح بحمض الجليسيرريزينيك، جزيء من جذور عرق السوس له خصائص مضادة للسرطان ومضادة للالتهاب. باستخدام مجهر إلكتروني وفحوصات بنيوية أخرى، أكد الباحثون أن الجسيمات شبه كروية وحجمها نحو 100–200 نانومتر ومغطاة بطبقة متجانسة، وهو نطاق حجم يعتبر مثالياً للتنقل عبر الجسم والتسرب إلى أنسجة الأورام.
تصميم مستقر وسلوك جيد في الجسم
أظهرت قياسات شحنة السطح أن كلًا من جسيمات الكيتوزان–السيلينيوم الأساسية والنسخة المعدلة بعرق السوس تحملان شحنة موجبة معتدلة، تكفي لتنافرها عن بعضها والبقاء موزعة بالتساوي بدلًا من التكتل. كشفت تحليلات الأشعة تحت الحمراء والأشعة السينية أن حمض الجليسيرريزينيك مرتبط بقوة في غلاف الكيتوزان دون أن يعرقل الطبيعة البلورية لنواة السيلينيوم. يقترح هذا المزيج بنية متينة يمكنها الدوران في الجسم والتفاعل مع أسطح الخلايا وإطلاق مكوناتها الفعالة تدريجيًا. كما يحسن غلاف الكيتوزان التوافق مع الأنسجة الحية ويدعم إطلاقًا محكومًا للسيلينيوم، مما قد يقلل الآثار الجانبية مقارنةً بالأدوية الحرة أو الجسيمات غير المستقرة.
ضرب خلايا السرطان أشد من الخلايا السليمة
اختبرت الجسيمات على خلايا ساركومة عظمية بشرية وعلى خلايا داعمة لنخاع العظم الطبيعية مزروعة مخبريًا. خفضت جميع التركيبات الثلاث المختبرة—حمض الجليسيرريزينيك وحده، وجسيمات الكيتوزان–السيلينيوم، والمركب النانوي الثلاثي المكونات—بقاء خلايا السرطان مع زيادة الجرعة. كانت جسيمات الكيتوزان–السيلينيوم البسيطة الأكثر عدوانية، والمركب النانوي المعدل بعرق السوس أقل حدّة بعض الشيء، وحمض الجليسيرريزينيك وحده الأخف تأثيرًا. من اللافت أن أياً من التركيبات لم يصل إلى جرعة ضارة لخلايا نخاع العظم الطبيعية ضمن نطاق التركيز نفسه، مما يشير إلى انتقائية واعدة تجاه خلايا الورم. أظهرت تجارب الصبغ التي تميز الانتحار الخلوي المنظم (الاستماتة) عن التمزق الفوضوي (التحلل) أن المركب النانوي حوّل خلايا السرطان نحو الاستماتة وبعيدة عن التحلل، على عكس جسيمات السيلينيوم غير المعدلة التي تسببت بمعدلات أعلى من الموت التحللي المدمِّر.
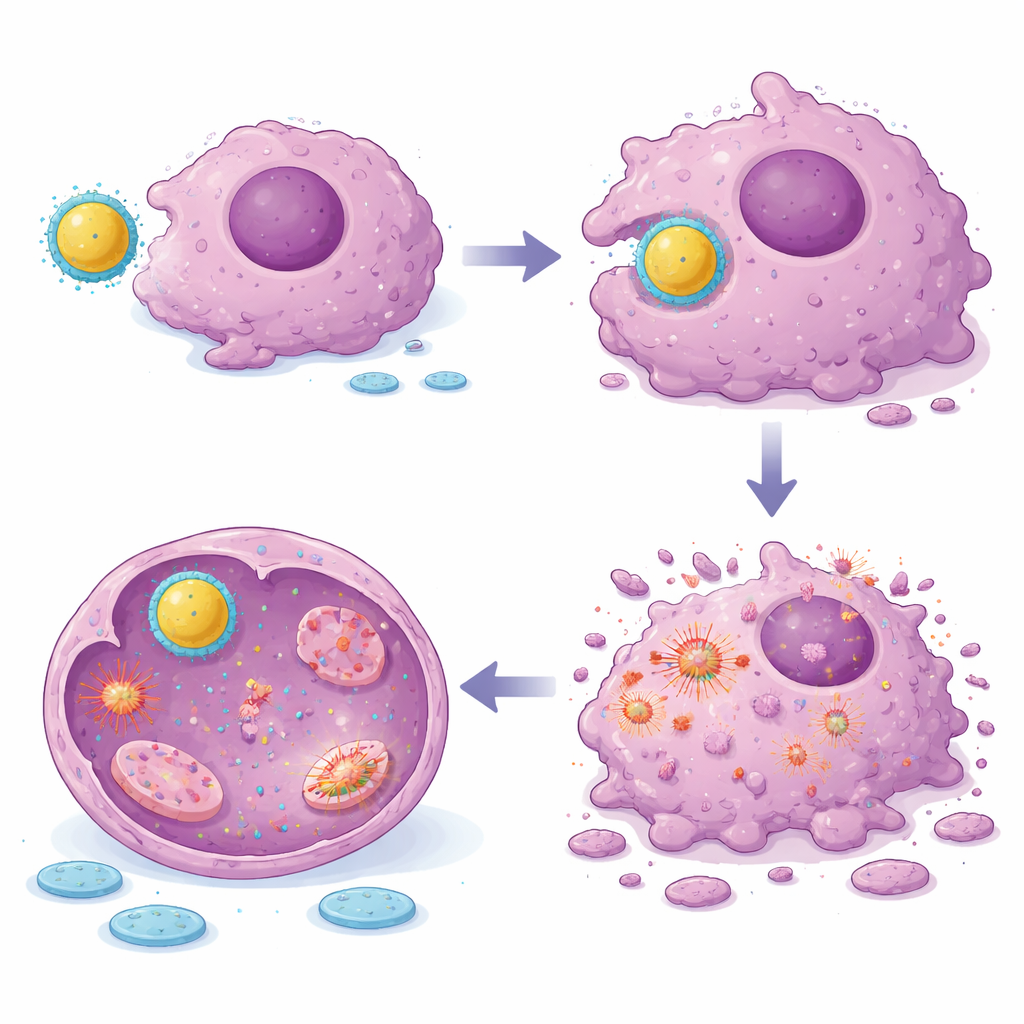
إطلاق إشارات الانتحار الخلوي النظيف داخل خلايا الورم
لفهم كيف تقتل هذه الجسيمات خلايا السرطان، قاس الباحثون إشارات داخلية رئيسية تتحكم في قرارات الحياة والموت داخل الخلايا. عزز المركب النانوي المعدل بعرق السوس بشدة الجينات والبروتينات التي تعزز الاستماتة، مثل Bax والبروتين الكابح للأورام p53، مع تقليل مستويات Bcl‑2، الجزيء الذي يحمي الخلايا عادة من الموت. هذا النمط مميز لبرنامج انتحار خلوي منظم مدفوع بالميتوكندريا بدلاً من تلف عرضي. أكدت صور المجهر للبروتينات الموسومة فلوريًا زيادة Bax وp53 وانخفاض Bcl‑2 في خلايا الساركومة المعالجة، خصوصًا مع المركب النانوي. تتناسب هذه التغيرات مع فكرة أن السيلينيوم في اللب يولد ضغطًا أكسديًا، في حين يضبط حمض الجليسيرريزينيك المسارات الالتهابية ومسارات البقاء، مما يوفر دفعة منسقة نحو موت مبرمج لخلايا السرطان.
ماذا يمكن أن يعني هذا لرعاية سرطان العظام في المستقبل
بالنسبة للقارئ العام، الرسالة الأساسية هي أن الباحثين بنوا جسيمًا نانويًا ثلاثي الطبقات يمكنه أن يدفع خلايا سرطان العظام للموت بطريقة منظمة مع ترك الخلايا الطبيعية المجاورة إلى حد كبير دون أذى—على الأقل في أطباق المختبر. من خلال الجمع بين تأثير الضغط الخلوي للسيلينيوم، وخصائص التوصيل اللطيفة للكيتوزان، والتأثير المضاد للسرطان والمهدئ لمركب من عرق السوس، تهدف هذه التركيبة إلى تعظيم قتل الورم وتقليل الالتهاب الضار أو الأضرار الجانبية. وبينما تظل هذه النتائج أولية ومقيدة بثقافات الخلايا، فإنها تشير إلى نهج نانوي دوائي مستقبلي قد يكمل أو يصقل علاجات الساركومة الحالية، مما يجعل العلاج أكثر استهدافًا وفعالية وربما أقل سمية.
الاستشهاد: El-ghannam, G., Elfeky, S.A., Abo-Elfadl, M.T. et al. The cytotoxic effects of glycyrrhizic acid-modified chitosan/selenium nanocomposite on osteosarcoma cancer cell line. Sci Rep 16, 9677 (2026). https://doi.org/10.1038/s41598-026-41099-w
الكلمات المفتاحية: الساركومة العظمية, الجسيمات النانوية, السيلينيوم, الكيتوزان, حمض الجليسيرريزينيك