Clear Sky Science · ar
تصنيف الشرائح المجمدة عبر أنواع السرطان باستخدام مُحوّل رؤي بنهج مزيج ناعم من الخبراء تحت إشراف ضعيف
لماذا هذا مهم في غرفة العمليات
عندما يزيل الجراحون ورماً مشتبهًا به، غالباً ما تتاح لهم دقائق فقط لمعرفة ما إذا تمت إزالة كل الأنسجة السرطانية. يهرع أخصائيو علم الأمراض لفحص قطعة رقيقة من النسيج تم تجميدها بسرعة وتقديم إجابة بينما لا يزال المريض على الطاولة. يمكن أن تعيق هذه العملية عالية الضغط الشرائح الضبابية، والأورام الطفيفة، والقيود الزمنية البسيطة. تستكشف الدراسة الواردة هنا كيف يمكن لنظام ذكاء اصطناعي أن يساعد الأطباء بسرعة وبشكل موثوق على التمييز بين الأنسجة الحميدة والخبيثة عبر أعضاء متعددة، باستخدام معدات واقعية للمستشفيات اليومية.
اختبار سريع مع تحديات مدمجة
يعد تحليل الشرائح المجمدة ركيزة للجراحة الحديثة: تُجمَّد قطعة رقيقة من النسيج وتُقطع وتُصبغ وتُشاهَد تحت المجهر لتحديد ما إذا كانت حميدة أو خبيثة وما إذا كان الهامش الجراحي خالياً من الورم. على خلاف الشرائح الثابتة في المختبر، غالباً ما تعاني الشرائح المجمدة من تشققات وطيّات وتلوين غير متساوٍ. قد يختلف الأطباء في الحالات الحدية، والوقت دائماً مضغوط. تزداد خطورة هذه المشكلات في المستشفيات الأصغر أو المزدحمة، حيث يجب على عدد قليل من المتخصصين تغطية أنواع كثيرة من السرطان. يجادل المؤلفون بأن مساعداً حاسوبياً قوياً يمكن أن يجعل قرارات الشرائح المجمدة أكثر اتساقاً وسرعة وتوفراً على نطاق أوسع.
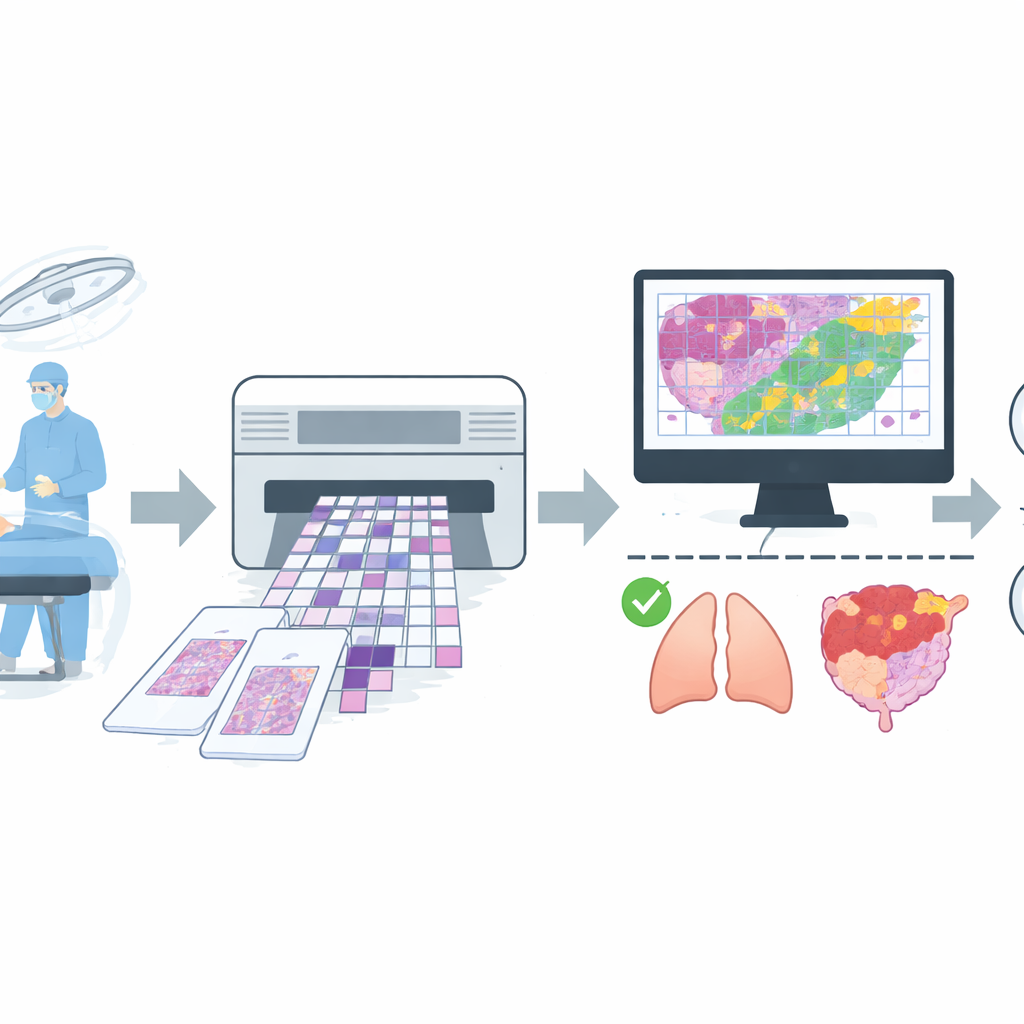
بناء مجموعة صور واسعة النطاق وواقعية
لتدريب مثل هذا المساعد، جمع الفريق مجموعة كبيرة من الصور الرقمية من العمليات الروتينية في مستشفى كبير. جمعوا 4,754 صورة شريحة كاملة لأنسجة مجمدة من أكثر من 2,600 مريض، ثم طبقوا قواعد جودة صارمة لإزالة الشرائح ذات العيوب الشديدة أو التشخيصات غير المؤكدة. احتوى مجموعة البيانات النهائية على 4,667 شريحة، تم وسم كل منها ببساطة على أنها حميدة أو خبيثة استناداً إلى الاتفاق بين قراءة الشريحة المجمدة السريعة وتقرير الشريحة الدائمة الأكثر دقة لاحقاً. غطت الشرائح مواقع شائعة مثل الرئة والثدي والغدة الدرقية والعقد اللمفاوية والأعضاء التناسلية الأنثوية، بالإضافة إلى مجموعة مختلطة من المواقع الأقل تكراراً مثل المعدة والكبد والجلد. قُسِّمت البيانات إلى مجموعات منفصلة للتدريب والتوليف الدقيق والاختبار النهائي، مع الحرص على ألا تظهر صور من نفس المريض في أكثر من مجموعة واحدة.
كيف يتعلّم الذكاء الاصطناعي من دلائل ضعيفة
بنى الباحثون نموذجهم على فئة من الشبكات العصبية تدعى محول رؤي، والتي تتفوق في إيجاد الأنماط عبر الصور الكبيرة. قُطعت كل صورة نسيجية ضخمة آلياً إلى بلاطات وقطع أصغر حتى يمكن معالجتها على عتاد رسومي قياسي. كان الابتكار الرئيسي استبدال جزء من الشبكة بـ «مزيج ناعم من الخبراء»، وهو مجموعة من الفروع التخصصية الصغيرة التي يركز كل منها على أنماط بصرية مختلفة. بدلاً من تفعيل خبير واحد وإيقاف الآخرين، يمزج النظام مساهماتهم بسلاسة، مما يستقرّن عملية التدريب ويستغل البيانات المحدودة بشكل أفضل. ونظراً لأن أخصائيي علم الأمراض لم يرسموا محيطات حول الأورام، اضطر النموذج للتعلم من إشراف ضعيف: كان يعرف فقط ما إذا كانت الشريحة كاملة حميدة أو خبيثة. عززت استراتيجية التعلم متعددة الحالات البلاطات الأكثر اشتباهاً داخل الشريحة الخبيثة لتعمل كأمثلة إيجابية، مما سمح للشبكة أن تركز تدريجياً على المناطق الأكثر إفادة.
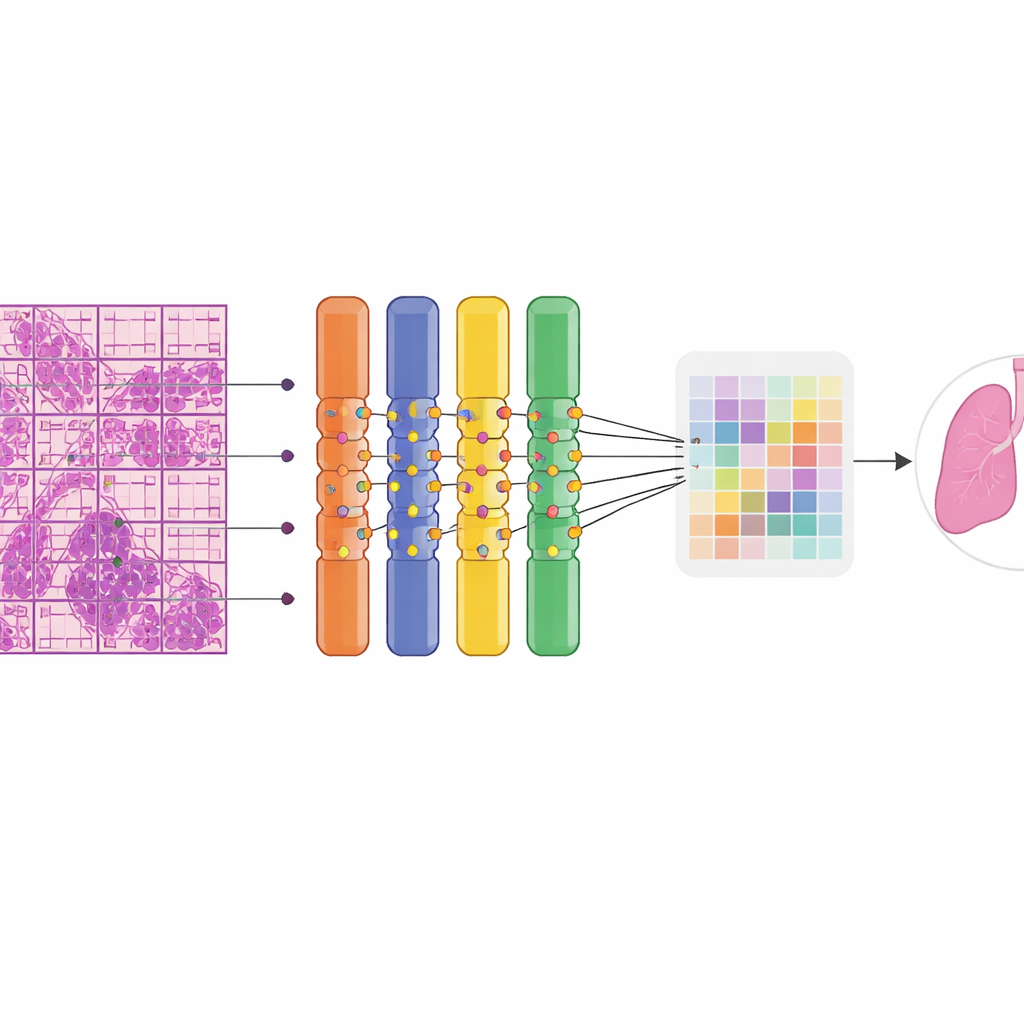
مدى فعالية النظام عملياً
عند اختباره على 669 شريحة لم تُستخدم سابقاً، ميّز الذكاء الاصطناعي بين الأنسجة الحميدة والخبيثة بدقة عالية. صنّف بشكل صحيح نحو 90% من الحالات إجمالاً، وأظهر قدرة ممتازة على فصل المجموعتين عبر عتبات الاحتمال. كانت الحساسية، أي احتمال الإشارة إلى شريحة خبيثة حقيقية، نحو أربعة من كل خمسة حالات، في حين كانت النوعية، أي احتمال اعتبار شريحة حميدة بأنها حميدة، أعلى حتى من ذلك. والأهم أن الأداء ظل قوياً عبر الأعضاء: فقد اكتشف بشكل كامل جميع حالات الرئة والثدي الخبيثة في مجموعة الاختبار وأدى أداءً جيداً على مجموعات أندر مثل أورام الملحقات الأنثوية والأعضاء «الأخرى» المختلطة. كشفت خرائط حرارة لونية مغطاة على الشرائح أن تركيز اهتمام النموذج تمحور حول مناطق اعترف خبراء علم الأمراض بأنها أورام، بما في ذلك النقاط النقيلية في العقد اللمفاوية، مع تجاهل إلى حد كبير البنى الطبيعية. عمل النظام بكفاءة، حيث احتاج ذاكرة تقل عن 5 غيغابايت، مما يجعله مناسباً للاستخدام على بطاقات رسومية متوفرة شائعاً بدلاً من مجموعات حواسيب مكلفة.
القيود، الأخطاء وفرص التحسين
فحص المؤلفون أيضاً حالات تعثر الذكاء الاصطناعي. غالباً ما شملت النتائج السلبية الكاذبة خلايا سرطانية نادرة للغاية، أو مناطق مسح ضبابية، أو التهاباً شديداً يخفي العُشّات الخبيثة. ونشأت الإيجابيات الكاذبة عادة في حالات حميدة تحاكي السرطان تحت المجهر، مثل النمو التفاعلي المفرط أو نسيج مجمد مشوه. وبما أن سير العمل الجراحي الروتيني لا يتضمن مخططات تفصيلية لمناطق الورم، لم يتمكن الفريق من قياس مدى تطابق خرائط الحرارة مع علامات الخبراء بشكل كمي، معتمداً بدلاً من ذلك على مراجعات وصفية. ظل بعض أنواع الأعضاء، مثل اللسان أو بعض أورام الأنسجة الرخوة، ممثلاً تمثيلاً ناقصاً، مما يوحي بأن مجموعات أكبر ومتعددة المراكز ستكون ضرورية لتوسيع نطاق النظام.
ما الذي قد يعنيه هذا للمرضى والمستشفيات
بشكل عام، تُظهر الدراسة أن نظام ذكاء اصطناعي مصمم بعناية يمكنه أن يساعد بدقة وبقابلية للتفسير في مهمة جوهرية في علم الأمراض الجراحي: تقرير، في الوقت الحقيقي، ما إذا كانت الأنسجة حميدة أو خبيثة عبر أنواع أعضاء متعددة. من خلال العمل اعتماداً فقط على وسوم على مستوى الشريحة، والتشغيل على عتاد متوفر على نطاق واسع، وتسليط الضوء على المناطق المشبوهة للمراجعة البشرية، يقدم النموذج طريقاً عملياً نحو قرارات أكثر اتساقاً في الشرائح المجمدة. بالنسبة للمرضى، قد يترجم هذا إلى جراحة أكثر اطلاعا في عملية واحدة؛ أما بالنسبة للمستشفيات، لا سيما تلك ذات الطاقم الخبير المحدود، فيشير إلى مستقبل تقوم فيه الأدوات الرقمية المتقدمة بالمساعدة في تقديم رعاية سرطانية عالية الجودة بشكل أكثر عدلاً.
الاستشهاد: Wu, J., Yang, M., Li, J. et al. Pan-cancer frozen section classification using a soft mixture of experts vision transformer under weak supervision. Sci Rep 16, 10297 (2026). https://doi.org/10.1038/s41598-026-40924-6
الكلمات المفتاحية: شريحة مجمدة, علم الأمراض الرقمي, تشخيص السرطان, محول رؤي, تعلم بإشراف ضعيف