Clear Sky Science · ar
جسيمات ذهبية مشتقة من النباتات مُفعّلة بفيوفوربيد-أ للعلاج الضوئي الفعّال ضد خلايا سرطان الرئة A549
هجوم أخضر معتمد على الضوء ضد سرطان الرئة
سرطان الرئة من أخطر السرطانات على مستوى العالم، والكثير من العلاجات الحالية تُلحق أذى بالأنسجة السليمة إلى جانب الأورام. تستعرض هذه الدراسة نهجًا أكثر رقة واستهدافًا يجمع بين جسيمات ذهبية مستخلصة من النباتات وصبغة حساسة للضوء لتدمير خلايا سرطان الرئة في المختبر بشكل انتقائي. الهدف هو توظيف تكنولوجيا نانوية "خضراء" وضوء ليزري بحيث تتعرض الخلايا السرطانية لضربة قوية بينما تُترك الخلايا السليمة المجاورة إلى حد كبير دون ضرر.
تحويل نبات طبي إلى مساعدين ذهب صغار جدًا
بدأ الباحثون بنبات Dicoma anomala الأفريقي الطبي المستخدم تقليديًا لعلاج عدة أمراض. وبدلاً من استخدام مواد كيميائية قاسية، استخدموا مستخلصًا من أوراق النبات لتحويل أملاح الذهب المذابة إلى جسيمات ذهبية نانوية صغيرة. قامت مركبات النبات كلًا من بتقليل الذهب وتغليف الجسيمات، منتجةً كرات مستقرة بحجم تقريبي 90–100 نانومتر وبسطح سالب الشحنة يساعد على منع تكتلها. أنتجت هذه العملية الصديقة للبيئة جسيمات متجانسة وطويلة الأمد ومناسبة للاستخدام الطبي.
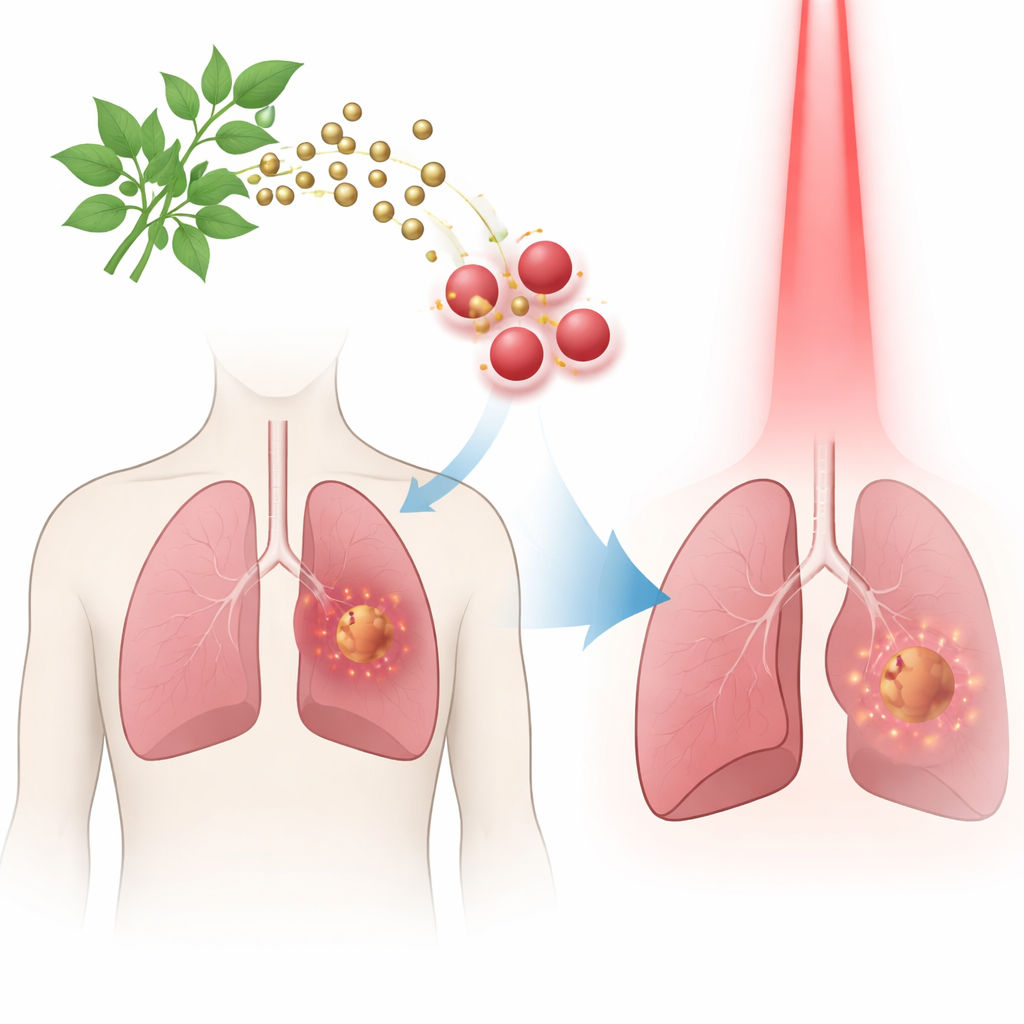
تحميل الجسيمات بعقار مفعل بالضوء
بعدها ربط الفريق مُحسسًا ضوئيًا يسمى فيوفوربيد‑أ—صبغة تصبح سامة فقط عند تعرضها للضوء الأحمر—بسطح الجسيمات الذهبية. باستخدام طريقة ترطيب الفيلم الرقيق، شكلوا مركبًا نانويًا حمّل حوالي 40 بالمئة من الدواء المضاف ارتباطًا ثابتًا بالجسيمات. أظهرت قياسات مفصلة أن القلب الذهبي والصبغة موجودان ومترابطان كيميائيًا، لا مجرد اختلاط. ظل المركب الناتج متشتتًا في الماء، وهي سمة مهمة لأي حقن محتمل في مجرى الدم.
اختبار قدرة العلاج الضوئي على قتل السرطان
لفحص ما إذا كان هذا المركب الهجين قادرًا على مكافحة السرطان، عرض العلماء خلايا سرطان الرئة البشرية A549 المزروعة في أطباق لجرعات مختلفة من المركب النانوي. بعض الخلايا أبقيت في الظلام، بينما تعرضت أخرى للضوء من ليزر أحمر مُعدّ على طول موجي ينشط فيوفوربيد‑أ بشكل قوي ويمكنه اختراق الأنسجة أفضل من الأطوال الموجية الأقصر. في الظلام، بدت الخلايا المعالجة وتصرّفت بشكل مشابه للخلايا غير المعالجة: حافظت على شكلها الطبيعي، وبقيت مستويات طاقتها مرتفعة، وقليل منها مات. لكن عند تشغيل الليزر، انخفض التمثيل الغذائي للخلايا بشكل حاد، وبدأت خلايا سرطان الرئة تتقلص وتنفصل وتتفتت بطريقة تعتمد على الجرعة.
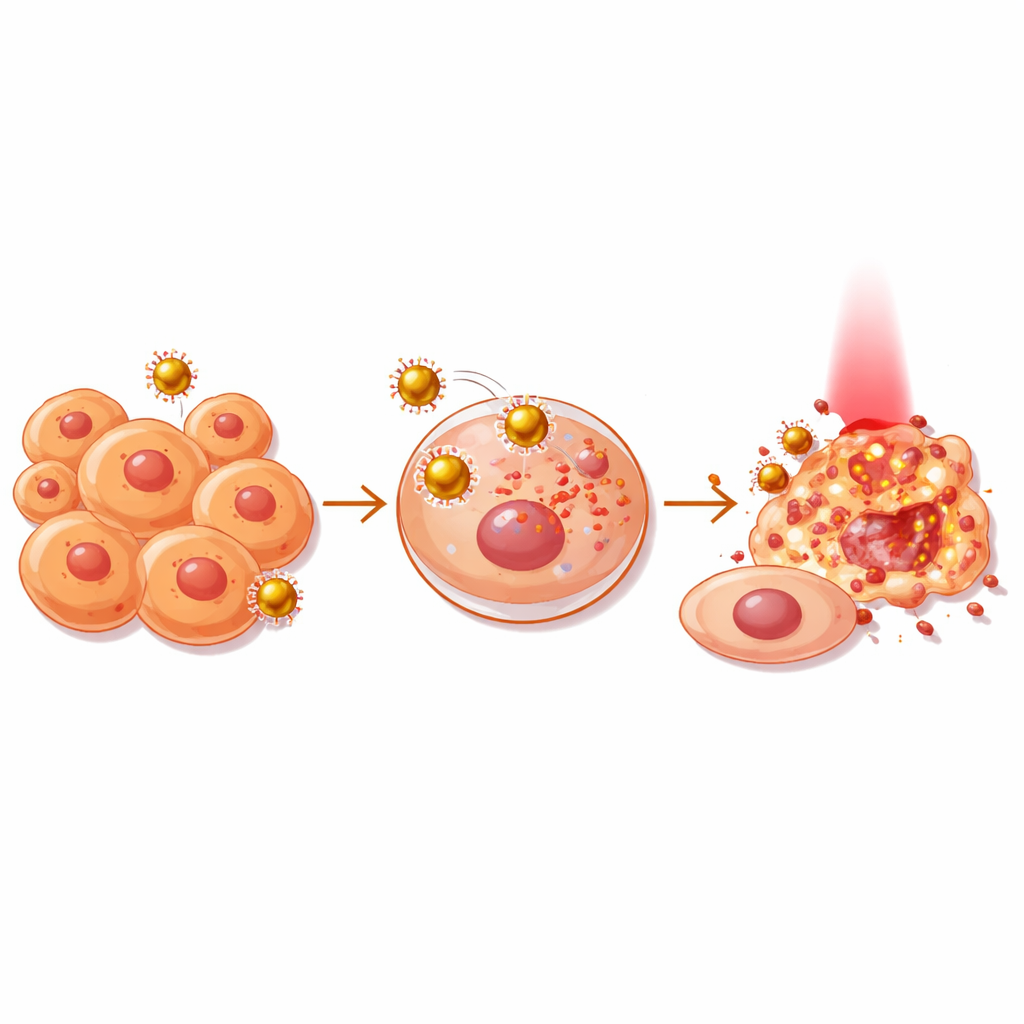
كيف تحفز الجسيمات انتحار الخلية
يكمن مفتاح هذا الانتقائية في أنواع الأكسجين التفاعلية—جزيئات أكسجينية قصيرة العمر وعنيفة تُنتَج عند امتصاص الجسيمات المحمّلة للضوء الأحمر. قيّم الفريق ارتفاعًا قويًا في هذه الجزيئات فقط في العينات المُضاءَة، مما يظهر أن العلاج في الغالب غير فعال حتى يُطبَّق الضوء. اختبارات الصبغ والتدفق الخلوي، الذي يفرز الخلايا بناءً على توهجها، كشفت أن العديد من الخلايا السرطانية المعالجة دخلت في حالة موت مبرمج تُعرف بالاستماتة (apoptosis)، وهو شكل من انتحار الخلايا المفضل عادةً على الموت الفوضوي غير المنضبط. في المقابل، بقيت الخلايا الطبيعية المشتقة من الجلد أكثر مقاومة لنفس العلاج، مما أسفر عن مؤشر انتقائية ملائم يشير إلى نافذة علاجية يمكن فيها ضرب الخلايا السرطانية أقوى من الخلايا السليمة.
ما الذي قد يعنيه هذا لعلاج سرطان الرئة مستقبلاً
تشير هذه الدراسة المعملية إلى أن الجمع بين جسيمات ذهبية مشتقة من النبات وصبغة مفعلّة بالضوء يمكن أن ينتج علاجًا ذكيًا مستقرًا، غير مؤذي إلى حد كبير في الظلام، وذا سمية عالية لخلايا سرطان الرئة عند الإضاءة. وعلى الرغم من أن العمل أُجري في ثقافات خلوية مسطحة وليس في حيوانات أو مرضى، فإنه يؤسس أرضية مهمة لعلاج قد يكون أكثر دقة وأقل إتلافًا من العديد من الخيارات التقليدية. مع مزيد من الاختبارات في نماذج أورام ثلاثية الأبعاد ونُظم حية، قد تدعم هذه المنصة النانوية الخضراء يومًا علاجات لسرطان الرئة توجّه الضوء فقط إلى حيث يلزم—وتترك بقية الجسم في الظلام.
الاستشهاد: Zahra, M., Abrahamse, H. & George, B.P. Plant-derived gold nanoparticles functionalized with pheophorbide-a for potent photodynamic therapy against A549 lung cancer cells. Sci Rep 16, 9819 (2026). https://doi.org/10.1038/s41598-026-40697-y
الكلمات المفتاحية: سرطان الرئة, العلاج الضوئي, جسيمات ذهبية نانوية, تكنولوجيا نانوية خضراء, الطب النانوي