Clear Sky Science · ar
ربط ABE9 بـ SpRY Cas9 نيكيز يمكّن من إنشاء نماذج فأرية خالية من التعديلات المجاورة بدقة
أدوات أكثر دقة لبناء نماذج مرضية أفضل
تحدث العديد من الأمراض الخطيرة بسبب أخطاء حرفية مفردة في حمضنا النووي. لفهم هذه الحالات ومعالجتها لاحقًا، غالبًا ما يصنع العلماء فئرانًا تحمل نفس الطفرات التي لدى المرضى البشريين. لكن إعادة كتابة الحمض النووي بدقة كهذه أمر أصعب مما يبدو: الطرق القديمة يمكن أن تترك ندوبًا في الجينوم، وتدخل طفرات إضافية، وتشوّش نتائج التجارب. تقدم هذه الدراسة أداة محسّنة لتحرير الجينات تُدعى ABE9-SpRY، صممت لتغيير حرف DNA واحد بعينه مع ترك الحروف المجاورة — وباقي الجينوم — إلى حد كبير دون تغيير.
من قصاصات عنيفة إلى تعديلات لطيفة على الحمض النووي
يعمل التحرير التقليدي بواسطة CRISPR-Cas9 مثل مقص جزيئي، يقطع شريطي الحمض النووي. تقوم الخلايا بإصلاح هذه الانقطاعات بشكل غير كامل، وغالبًا ما تترك إدخالات أو حذفًا صغيرًا يعطل الجينات بطرق لا يمكن التنبؤ بها. هذا مفيد لإيقاف عمل الجينات، لكنه غير مناسب لمحاكاة طفرة محددة مسببة للمرض. بالمقابل، تقوم مُعدِّلات القواعد (base editors) بعدم قطع الحمض النووي؛ بل تدفع كيميائيًا حرفًا واحدًا إلى حرف آخر — هنا تحويل A إلى G — مع الحفاظ على اللولب المزدوج سليمًا. هذا النهج يقلل بشكل كبير من الحذف الكبير وإعادة الترتيب، لكن مُعدِّلات الأدينين السابقة عانت من ثلاث مشكلات رئيسية: كانت أحيانًا تعدل حروفًا متجاورة «بالمصادفة»، ويمكنها الوصول فقط لمواقع بجانب تتابعات قصيرة محددة، وأحيانًا تسبب تعديلات في مواقع غير مقصودة في الجينوم.
تصميم قلم جزيئي أكثر انتقائية
سعى الباحثون لمعالجة هذه القيود الثلاثة معًا. بدأوا بـ ABE9، وهو نسخة أحدث من مُعدِّل القواعد تركز نشاطها على نطاق ضيق جدًا من الحمض النووي، ما يصغر «نافذة التحرير» بحيث يَتغيّر عدد أقل بكثير من الحروف المجاورة عن غير قصد. ثم ربطوا ABE9 بـ Cas9 نيكيز معدل يُدعى SpRY. على عكس Cas9 القياسي الذي يتطلب وسمًا صارمًا «NGG» بجانب موقع الهدف، يمكن لـ SpRY التعرف على مجموعة أوسع بكثير من تتابعات الحمض النووي. هذا يجعل من الممكن الوصول لمواضع مرتبطة بالأمراض في الجينوم كانت سابقًا خارج النطاق. الأداة المندمجة الناتجة، ABE9-SpRY، تهدف لأن تكون دقيقة للغاية وأكثر مرونة بخصوص أماكن عملها.
اختبار المُحرِّر الجديد في الخلايا والأجنة
لمعرفة ما إذا كان ABE9-SpRY يفي بتصميمه، قارن الفريق بينه وبين محرر أكثر عدوانية مستخدم على نطاق واسع يُدعى ABE8e-SpRY. استهدفوا أربعة مواقع مرتبطة بالأمراض في جينات تشفر قنوات أيونية (TPC1 وTPC2 وTRPM4)، والتي تلعب أدوارًا مهمة في وظيفة القلب والكبد. في خلايا عصبية فأرية نمت في المختبر، حرّر ABE8e-SpRY الحرف المستهدف بكفاءة أعلى لكنه غيّر أيضًا العديد من القواعد المجاورة. أما ABE9-SpRY فنتجت عنه تعديلات إجمالية أقل، لكن نسبة أعلى بكثير من النتائج «النظيفة» — أي قراءات تغيّر فيها الحرف المقصود فقط دون طفرات إضافية في المنطقة المحلية. ورُصد نفس النمط في أجنة الفئران. عندما حقن الباحثون مكونات التحرير في بيض مخصب، غالبًا ما حوّل ABE8e-SpRY معظم نسخ الجين المستهدف لكن مع تغييرات مجاورة كثيرة. أما ABE9-SpRY فحرّر نسخًا أقل عمومًا، ومع ذلك حيثما فعل ذلك كان التسلسل الوراثي عادةً مصححًا تمامًا كما هو مخطط.
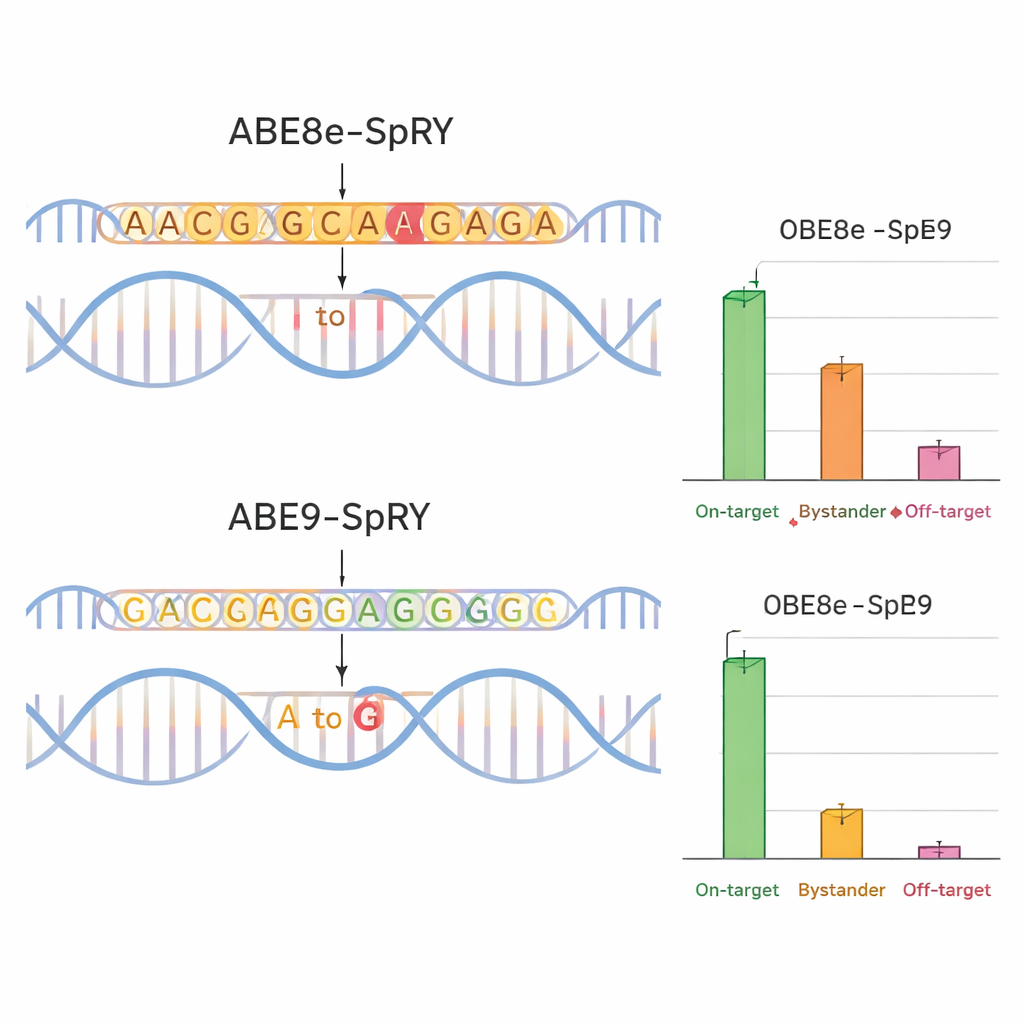
تعديلات أنظف، آثار جانبية أقل
الدقة ليست فقط حول الجوار المحلي للحمض النووي. فحص الفريق أيضًا ما إذا كان محررهم يغير مناطق بعيدة من الجينوم. باستخدام توقعات حاسوبية وتسلسل موجه، قاسوا التغيرات خارج الهدف في مواقع محتملة المشابهة في أجنة الفئران. غالبًا ما أدخل ABE8e-SpRY تغييرات A-to-G غير مقصودة في هذه المواقع، أحيانًا بمستويات مرتفعة مفاجئة. أظهر ABE9-SpRY أحداثًا أقل بكثير من هذا النوع، مع تعديلات خارج الهدف نادرة ونشاط غير قابل للكشف في اختبار متخصص للأضرار المستقلة عن Cas9. والأهم من ذلك، عندما استُخدم ABE9-SpRY بمفرده — وليس في اختبارات مجمعة — لإدخال طفرين محددتين في الفئران، أنتج العديد من الحيوانات المؤسسة التي وُجد فيها التعديل المرغوب بمستويات عالية وتم توريثه إلى النسل بشكل موثوق، مجددًا مع تغييرات مجاورة طفيفة أو إدخالات وحذوفات صغيرة قليلة.
نشر الدقة إلى الخلايا الجذعية البشرية
نظرًا لأن الخلايا الجذعية المخصصة للمرضى تُستخدم بشكل متزايد لدراسة المرض واختبار الأدوية، جرب الباحثون أيضًا ABE9-SpRY في الخلايا الجذعية المحفزة متعددة القدرات البشرية. استهدفوا النسخة البشرية من جين TPC1 في موضع معادل لأحد مواقع الفأر. باستخدام مؤشر فلوري لإثراء الخلايا المحررة، وجدوا أن ABE8e-SpRY أنتج معدلات تحرير خام أعلى لكنه عدّل أيضًا قواعد مجاورة متعددة مجددًا. حرّر ABE9-SpRY نسخًا أقل عمومًا، لكن نسبة السلاسل المحررة تمامًا — تغيير مقصود واحد ولا شيء آخر — كانت أعلى بكثير، مع إدخالات أو حذوفات مدمرة أقل. في أعمال الخلايا الجذعية، حيث تُوسّع العزلات الفردية لدراسات مفصّلة، يكون هذا النوع من التحرير «النظيف» عادةً أكثر قيمة من الكفاءة القوية وحدها.
لماذا هذا مهم لبحوث الأمراض المستقبلية
بالنسبة للعلماء الذين يحاولون فهم كيف يؤدي تغيير حرف واحد في الحمض النووي إلى المرض، يمكن أن تكون الطفرات غير المقصودة مضللة للغاية. تظهر هذه الدراسة أن ABE9-SpRY، رغم أنه أقل قوة إلى حد ما من حيث سرعة التحرير الخام، يمكنه كتابة تغييرات حرفية مفردة في جينومات الفئران والخلايا الجذعية البشرية بدقة لافتة ومرونة استهداف واسعة. هذا يجعله أداة واعدة لبناء نماذج حيوانية وخلوية مخلصة للاضطرابات الوراثية البشرية، خاصة في الحالات التي قد تربك فيها حتى طفرة واحدة منفلتة البيولوجيا أو تعطل علاجًا محتملاً.
الاستشهاد: Ong, J.K., Bhunia, S., Hilbert, B. et al. ABE9 fused to SpRY Cas9 nickase enables precise generation of bystander free mouse models. Sci Rep 16, 7463 (2026). https://doi.org/10.1038/s41598-026-40642-z
الكلمات المفتاحية: تحرير قواعد الأدينين, نماذج الأمراض بواسطة CRISPR, وراثة الفئران, تأثيرات خارج الهدف, تحرير جينات الخلايا الجذعية المحفزة البشرية