Clear Sky Science · ar
اكتشاف هيدروكسيتراتيازول كمثبّت محتمل لإنزيم غلوكزالاز-I باستخدام تقنيات تصميم الأدوية بمساعدة الحاسوب
لماذا قد يقاوم إيقاف منظف خفيف داخل الخلية السرطان
تتزايد خلايا السرطان في كثير من الأحيان بسرعة كبيرة إلى حد أنها تغرق في نفاياتها الخاصة. إحدى حيلها للبقاء هي وجود نظام تنظيف داخلي يزيل المنتجات الضارة الناتجة عن احتراق السكر. تستعرض هذه الدراسة كيفية إيقاف عضو رئيسي في هذا النظام، إنزيم يدعى غلوكزالاز‑I، باستخدام الحاسوب ليفرز عشرات الآلاف من الجزيئات وتجارب لاختبار أفضل المرشحين. الهدف هو اكتشاف «نقاط بداية» دوائية جديدة قد تساعد يوماً ما الأطباء على تسميم خلايا السرطان بشكل انتقائي من الداخل.
نظام نفايات مخفي داخل خلايانا
تفكك كل خلية السكر باستمرار لإنتاج الطاقة، وتنتج هذه العملية مادة نفاية تفاعلية تسمى ميثيلغليوكسال. بكميات طبيعية يحولها الجسم إلى حمض لبني غير ضار عبر نظام الغلوكزالاز، وهو مسار من خطوتين يعتمد على الجلوتاثيون كمساعد. يُعد غلوكزالاز‑I الخطوة الأولى والأكثر أهمية في هذه السلسلة. تعتمد خلايا السرطان، التي تحرق السكر بوتيرة محمومة، بشكل كبير على غلوكزالاز‑I لمنع تراكم الميثيلغليوكسال إلى مستويات سامة. إذا تم حجب هذا الإنزيم، يتراكم الميثيلغليوكسال ويمكن أن يدفع الخلايا المتضررة نحو الموت المبرمج. وهذا يجعل غلوكزالاز‑I هدفاً جذاباً لأدوية مضادة للسرطان تضرب ضعفاً أساسياً في استقلاب الورم.
البحث في فضاء المركبات بالسيليكون والإحصاء
بدلاً من اختبار مواد عشوائية في المختبر، استخدم الباحثون تصميم الأدوية بمساعدة الحاسوب للبحث في مجموعة تجارية كبيرة تضم أكثر من 50,000 جزيء صغير. قامت برمجيات متخصصة أولاً بتنظيف وتوحيد كل جزيء، ثم توقعت شكله ثلاثي الأبعاد وسلوكه عند درجة حموضة شبيهة بالجسم. خطوة فحص افتراضي سريعة قيّمت مدى ملاءمة كل مرشح لموقع نشط غلوكزالاز‑I. ثم طبّق الفريق قواعد بسيطة عن الحجم والذوبان وخصائص مشابهة للدواء لاستبعاد الجزيئات غير المرجح أن تعمل داخل الجسم. برنامج اقتران أكثر تفصيلاً فحص كيف يمكن أن تتجه الجزيئات الأكثر واعدة داخل الإنزيم، وخصوصاً كيف قد تصل وتمسك بذرة الزنك المعدنية التي تقع في صميم كيمياء غلوكزالاز‑I.
طريقة جديدة للتمسك بالنواة المعدنية للإنزيم
ركزت جهود سابقة لحجب غلوكزالاز‑I على مجموعات كيميائية معروفة، مثل الأحماض الكربوكسيلية والأحماض الهيدروكساميك، التي تجيد ربط المعادن لكنها غالباً ما تعاني من ضعف الاستقرار أو تأثيرات جانبية غير مرغوبة. كشفت الدراسة الحالية بدلاً من ذلك عن وحدة مختلفة لـ«الاستيلاء على المعدن»: حلقة هيدروكسيتراتيازول. من بين ستة عشر جزيئاً من الأعلى تقييماً اختيرت للشراء والاختبار المخبري، برز واحد يحمل هذه الحلقة—مرمز SPB07393SC—كالأبرز. في الاقتران الافتراضي، وصلت مجموعة الهيدروكسيتراتيازول إلى ذرة الزنك، بينما انحشرت حلقتاه الأروماتيتان في جيوب دهنية قريبة من الإنزيم. أشارت محاكاة حاسوبية للمجمع على مدى عشرات النانوانيوثانية إلى أن الجزيء ظل مرتبطاً بإحكام، مع مسافات مستقرة، وشكل بروتيني مدمج، وشبكة مستمرة من روابط الهيدروجين.
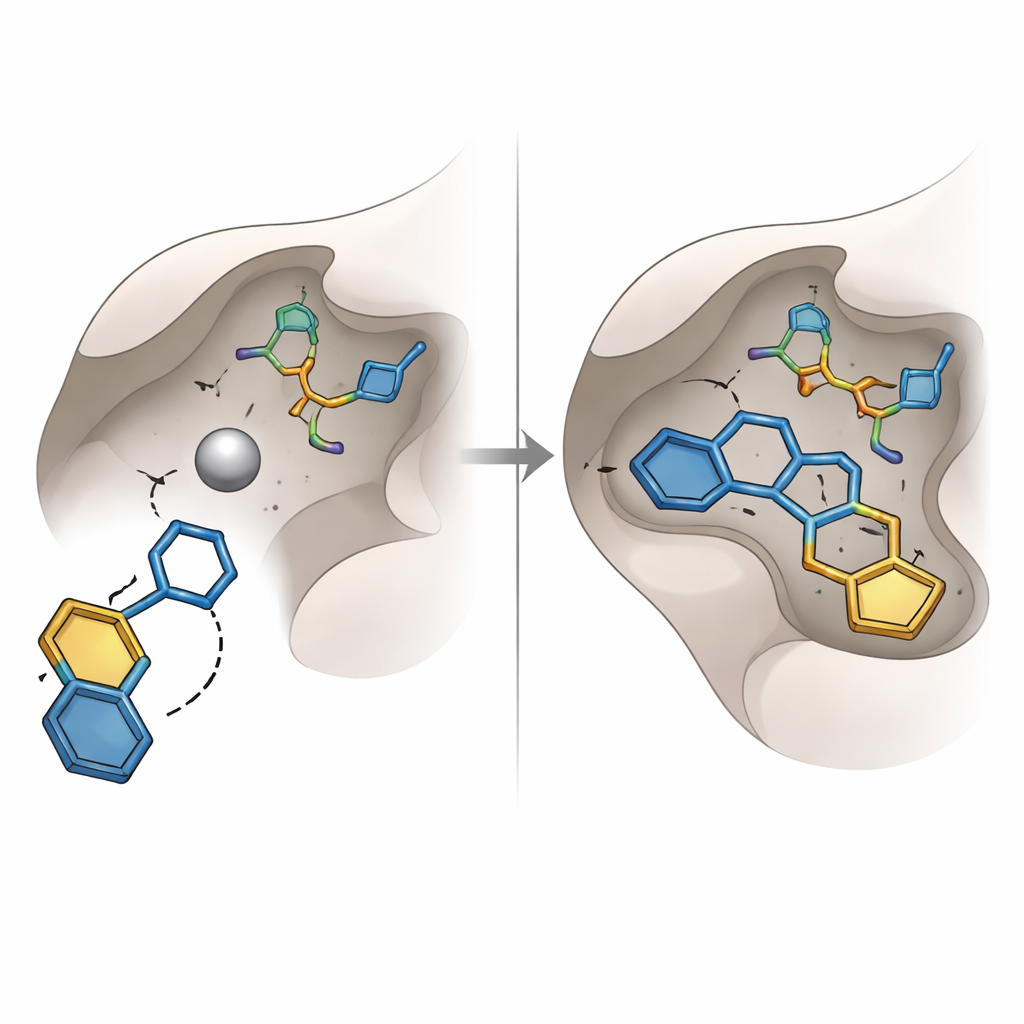
وضع التنبؤات على المحك
للاطلاع على ما إذا كانت نماذج الحاسوب تترجم إلى تأثيرات في العالم الحقيقي، قاس الفريق مدى قدرة الجزيئات المختارة على إبطاء نشاط غلوكزالاز‑I البشري المنقى في اختبار معقد على لوحات. أظهر خمسة عشر من الستة عشر مرشحاً تثبيطاً ضعيفاً أو لا يذكر تحت الشروط المختبرة، مما يسلط الضوء على مخاطر الاعتماد كلياً على درجات الاقتران الثابتة. في المقابل، ثبّت SPB07393SC الإنزيم بقوة، مع فعالية متوسطة بالميكرومولار تجعل منه «ضربة» مبكرة جيدة بدلاً من دواء مكتمل. توقعت أدوات برمجية إضافية أن لهذا الجزيء ذوبانية مقبولة، وامتصاص جيد، وقدرة على الوصول إلى الدماغ عند الحاجة، واحتمال منخفض للتسبب في سمّية وراثية أو كبدية معينة، رغم أن هذه التنبؤات الخاصة بالسلامة ما تزال تتطلب تأكيداً تجريبياً.
ماذا يعني هذا لأدوية السرطان المستقبلية
تقدم الدراسة الهيدروكسيتراتيازول كطريقة جديدة لترسيخ مرشحي الأدوية إلى ذرة الزنك في قلب غلوكزالاز‑I، موسعةً قائمة الحيل الكيميائية المتاحة لمصممي الأدوية. وعلى الرغم من أن SPB07393SC نفسه ليس سوى نقطة بداية، فإن مزيجه من قوة حجب الإنزيم، وسلوك متوقع شبيه بالدواء، والارتباط المستقر في محاكيات الحركة يميّزه كهيكل واعد لمزيد من التحسين. وبشكل أوسع، تظهر الدراسة نقاط القوة والحدود في الفرز الموجه بالحاسوب: يمكنه تضييق مكتبات كيميائية هائلة بسرعة إلى عدد قليل من المتنافسين الواقعيين، لكن التجارب المخبرية الدقيقة تظل أساسية لكشف أي الجزيئات تعطل الإنزيم فعلاً الذي تعتمد عليه خلايا السرطان لإدارة نفاياتها السامة.
الاستشهاد: Al-Qazzan, M., Al-Balas, Q., Alnajjar, B. et al. Discovery of hydroxytriazole as a potential glyoxalase-I inhibitor utilizing computer-aided drug design techniques. Sci Rep 16, 9945 (2026). https://doi.org/10.1038/s41598-026-40497-4
الكلمات المفتاحية: غلوكزالاز I, استقلاب السرطان, تصميم الأدوية بمساعدة الحاسوب, مثبطات رابطة للزنك, الاقتران الجزيئي