Clear Sky Science · ar
ناقلات نانوية مطلية بالكيتوزان تستجيب للمحفزات لتوصيل الكابسيسين المستهدف ونشاط حيوي انتقائي على خلايا HepG2 يعتمد على النواة
بهار بقوة خفية
تضيف الفلفل الحار أكثر من مجرد حرارة إلى طعامنا: إحراقه ناتج عن الكابسيسين، مركب طبيعي يمكنه أيضاً قتل الخلايا السرطانية. ومع ذلك، كان من الصعب استخدام الكابسيسين كدواء لأنه يذوب بصعوبة في الماء، ويختفي بسرعة من الجسم، ويسبب تهيج الأنسجة السليمة عند الجرعات العالية. تستعرض هذه الدراسة طريقة لترويض ذلك الجزيء الناري عبر وضعه داخل جسيمات دقيقة وذكية قادرة على حمل الكابسيسين بأمان عبر مجرى الدم وإطلاقه أساسًا داخل أورام الكبد.
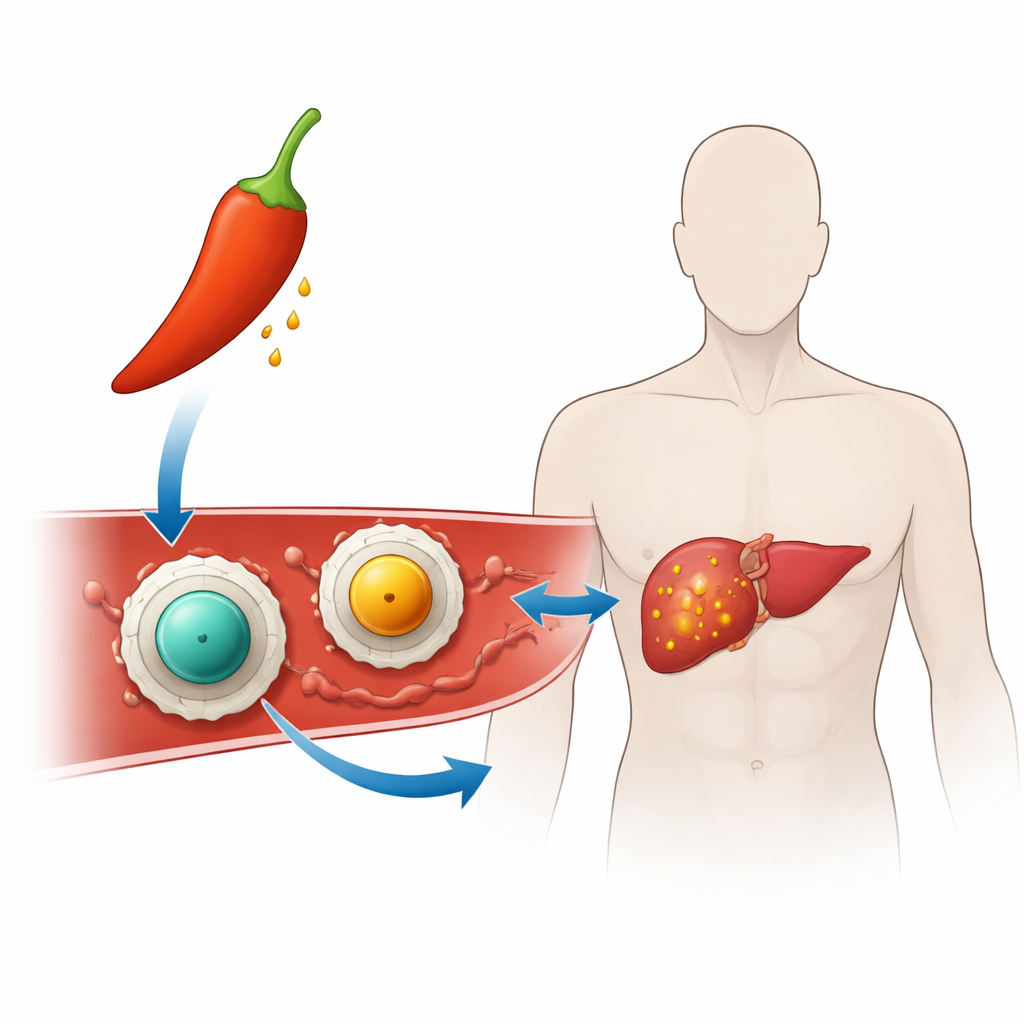
تحويل الفلفل الحار إلى علاج موجه
بنى الباحثون «ناقلات نانوية» — جسيمات أصغر آلاف المرات من حبة رمل — لنقل الكابسيسين إلى الخلايا السرطانية. لكل ناقل نانوي نواة صلبة مصنوعة من معدن مغناطيسي يسمى فيرايت (إما فيرايت الزنك أو فيرايت المنغنيز) مغطاة بطبقة رقيقة من الكيتوزان، وهو مادة شبيهة بالسكر مشتقة من قشور القشريات وتُستخدم فعلاً في المنتجات الطبية والغذائية. تجعل هذه الطبقة الجسيمات أسهل على التعليق في الماء وتساعدها على الالتصاق بأسطح الخلايا والحمض النووي، وهو أمر مهم لقتل السرطان. من خلال تحميل الكابسيسين داخل غلاف الكيتوزان هذا، أمّل الفريق في الحفاظ على استقرار الدواء وإبقائه مخفياً حتى يصل إلى البيئة القاسية داخل الورم.
إطلاق ذكي في ظروف الورم
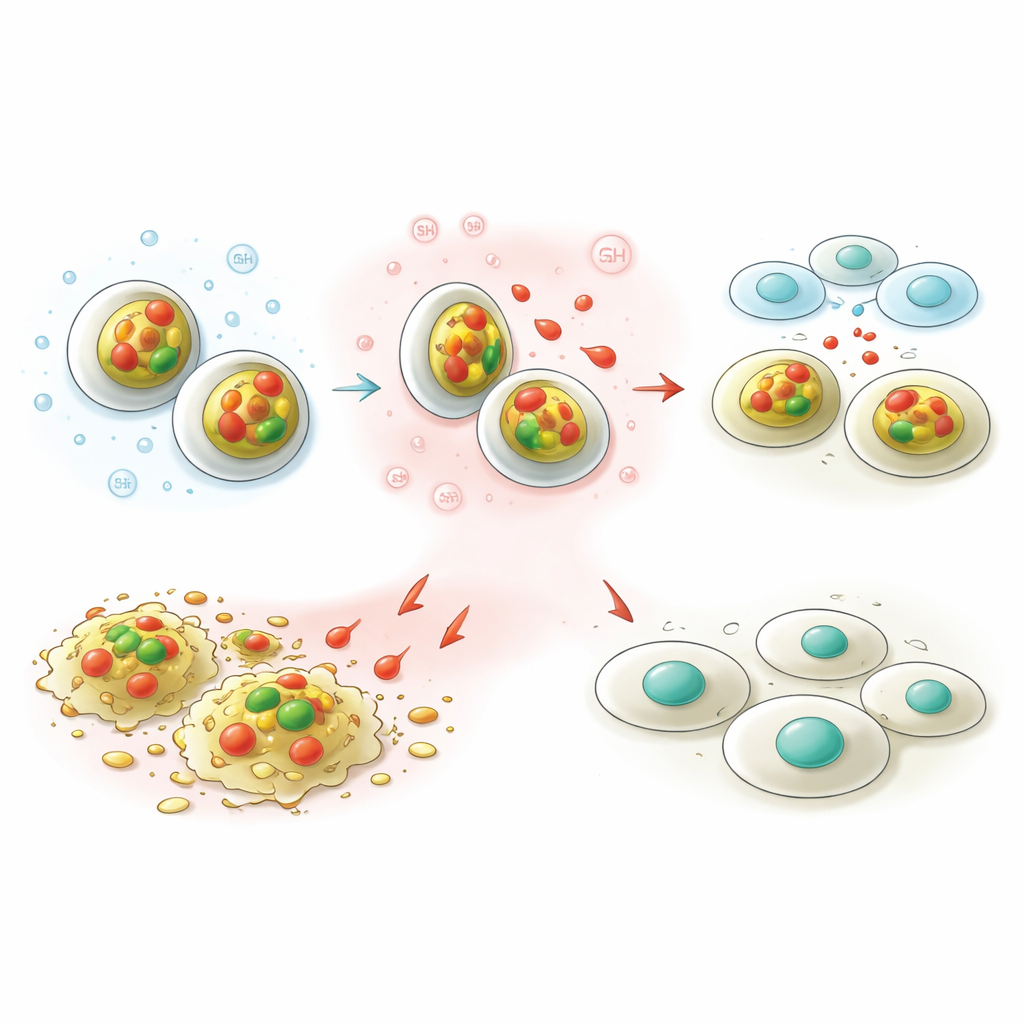
من الخصائص الرئيسية للأورام أنها تميل لأن تكون أكثر حموضة وأغنى ببعض مضادات الأكسدة، مثل الغلوتاثيون، مقارنة بالأنسجة الصحية. صمم الفريق ناقلاتهم النانوية لاستشعار هذه الظروف. في الاختبارات المخبرية عند درجة حموضة الدم الطبيعية، تسرب أقل من 10 بالمئة من الكابسيسين المخزون خلال يومين، مما يوحي بأن الجسيمات ستحمل حمولتها بأمان أثناء الدوران. في ظل ظروف شبيهة بالورم — أكثر حموضة ومع وفرة من الغلوتاثيون — أفرجت الجسيمات عن نحو ثلث الكابسيسين. هذا السلوك «تشغيل–إيقاف» يعني أن الدواء من المرجح أن يُفرَغ داخل الخلايا السرطانية بدلاً من على طول الطريق، مما قد يعزز الفائدة بينما يقلل الآثار الجانبية.
كيف تشكّل مكونات الجسيمات السلامة والفعالية
رغم أن الناقلات النانوية بدت متشابهة من بعيد، فإن أنويتها الداخلية أحدثت فرقاً حقيقياً. كانت الجسيمات القائمة على الزنك تميل لأن تكون أصغر وتمسك بالكابسيسين بشدة أكبر، بينما كانت جزيئات المنغنيز أكثر مسامية وتسمح للدواء بالخروج بسهولة أكبر. كلا النوعين حمل شحنة سطحية موجبة قوية، مما يساعدها على التفاعل مع الأسطح السالبة الشحنة للخلايا والحمض النووي. أظهرت اختبارات مع الدم البشري ضرراً ضئيلاً لخلايا الدم الحمراء، وكانت الجسيمات الفارغة لطيفة على خلايا الرئة الطبيعية، مما يدعم سلامتها الأساسية. عند تحميلها بالكابسيسين، أصبحت كلا المنظومتين أكثر فعالية ضد خلايا سرطان الكبد، لكن نسخة المنغنيز حققت أفضل توازن: أضرت بالخلايا السرطانية بقوة أكبر بينما ظلت أكثر لطفاً نسبياً مع الخلايا الطبيعية.
أبعد من السرطان: تأثيرات واقية إضافية
لم تقتصر وظيفة الناقلات النانوية على توصيل الكابسيسين فحسب. فقد أبطأت أيضاً نمو عدة بكتيريا ممرِضة بفاعلية مشابهة لمضاد حيوي قياسي في بعض الاختبارات، وساعدت في تحييد الجذور الحرة الضارة المرتبطة بالالتهاب وتلف الأنسجة. أظهرت قياسات دقيقة معتمدة على الضوء أنه بعد تعبئة الكابسيسين داخل جسيمات الفيرايت–الكيتوزان، ارتبط بشكل أقوى وأكثر ثباتاً بالحمض النووي. كشفت تجارب حركية سريعة عن تفاعل من خطوتين: يلتصق الحمض النووي أولاً بسطح الجسيم الموجب الشحنة، ثم يعيد المركب ترتيب نفسه إلى ارتباط أوثق وأكثر دواماً. من المرجح أن تفسر هذه التفاعلات المقواة سبب إظهار الجسيمات المحمّلة تأثيرات مضادة للسرطان والبكتيريا ومضادة للأكسدة أقوى من الكابسيسين أو جزيئات الفيرايت وحدها.
ماذا قد يعني هذا للمرضى
حتى الآن، هذه النتائج مستخلصة من أطباق مخبرية، وليست من مرضى. ومع ذلك، فهي تشير إلى أن الناقلات النانوية المصممة بعناية يمكن أن تحول مكوّناً من الطعام الحار إلى سلاح أكثر دقة ضد السرطان. عبر اختيار مادة النواة والغطاء المناسبين، أنشأ الباحثون عبوات صغيرة تحافظ على استقرار الكابسيسين، وتحمله بأمان في الدم، وتفكك حمولته بشكل تفضيلي في ظروف شبيهة بالورم، خاصة في خلايا سرطان الكبد. من بين التصاميم المختبرة، قدمت الجسيمات القائمة على المنغنيز المزيج الأكثر واعدة بين القتل السرطاني الموجه، وقلة الضرر للخلايا الطبيعية، والفوائد الإضافية المضادة للبكتيريا ومضادة للأكسدة. مع دراسات حيوانية وأبحاث سلامة إضافية، قد تسهم مثل هذه الجسيمات «الذكية» المستوحاة من الفلفل يوماً ما في علاجات أكثر لطفاً وتركيزاً لسرطان الكبد وربما أمراض أخرى.
الاستشهاد: Bakr, E., Elshami, F.I., Okba, E.A. et al. Stimuli-responsive chitosan-coated ferrite nanocarriers for targeted capsaicin delivery and core-dependent HepG2-selective bioactivity. Sci Rep 16, 8957 (2026). https://doi.org/10.1038/s41598-026-40433-6
الكلمات المفتاحية: كابسيسين, سرطان الكبد, جزيئات نانوية, توصيل دوائي موجه, ناقلات تستجيب للمحفزات