Clear Sky Science · ar
ترابسيديكين بالإضافة إلى عامل النسيج المستهدف CD13 tTF-NGR ضد الساركومة الطرية المتقدمة المنتكِسة أو المقاومة للعلاج: بيانات ترجمة، سلامة سريرية وفعالية
لماذا يهم هذا البحث
الأشخاص المصابون بالساركومات الطرية المتقدمة — سرطانات نادرة تنشأ في العضلات أو الدهون أو الأنسجة الداعمة الأخرى — غالبًا ما تنفد أمامهم خيارات علاجية فعالة. يستكشف هذا البحث استراتيجية دوائية جديدة على مرحلتين تهدف إلى حجز دواء كيميائي موجود داخل الورم وقطع إمداد الدم عنه، على أمل تحسين السيطرة على المرض مع الحفاظ على آثار جانبية قابلة للتحكم.
سرطان نادر بحاجة إلى خيارات أفضل
تشكل الساركومات الطرية نحو 1% فقط من سرطانات البالغين، لكنها غالبًا ما تكون عدوانية بمجرد أن تنتشر أو لا يمكن استئصالها جراحيًا. يمكن للعلاج الكيميائي القياسي أن يبطئ نموها، ومع ذلك يبقى البقاء على قيد الحياة لدى المرضى ذوي المرض المتقدم ضعيفًا. يُعد الترابسيديكين أحد الأدوية الرئيسية المستخدمة بعد فشل العلاجات الخط الأول. يعمل عن طريق إتلاف الحمض النووي للخلايا السرطانية وكذلك عبر التأثير على الخلايا في محيط الورم. ومع ذلك، تعود العديد من الأورام للنمو في نهاية المطاف، مما يدفع الباحثين للبحث عن طرق لتعزيز تأثيره دون زيادة كبيرة في الضرر للمرضى.
«فخ» من خطوتين للورم
اختبر الفريق مفهومًا يسميه «فخ الترابسيديكين» (TRABTRAP). في البداية، يتلقى المرضى الترابسيديكين عبر تسريب طويل لمدة 24 ساعة. في اليومين أو الثلاثة التالية، يتلقون دواءً ثانيًا، tTF-NGR. هذا البروتين المصمم يتجه نحو علامة تُسمى CD13 الموجودة أساسًا على الأوعية الدموية المغذية للأورام. عندما يرتبط tTF-NGR بهذه الأوعية، فإنه يطلق تخثرًا محليًا للدم ويغلق تدفق الدم، مما يؤدي إلى موت أجزاء من الورم. الفكرة أن إعطاء الترابسيديكين أولًا يسمح له بالتسرب داخل الورم، ثم يقوم tTF-NGR بسد المنافذ بإغلاق الأوعية الدقيقة للورم، مما يحبس الدواء حيثما هو مطلوب ويضخم تأثير كلا العلاجان.
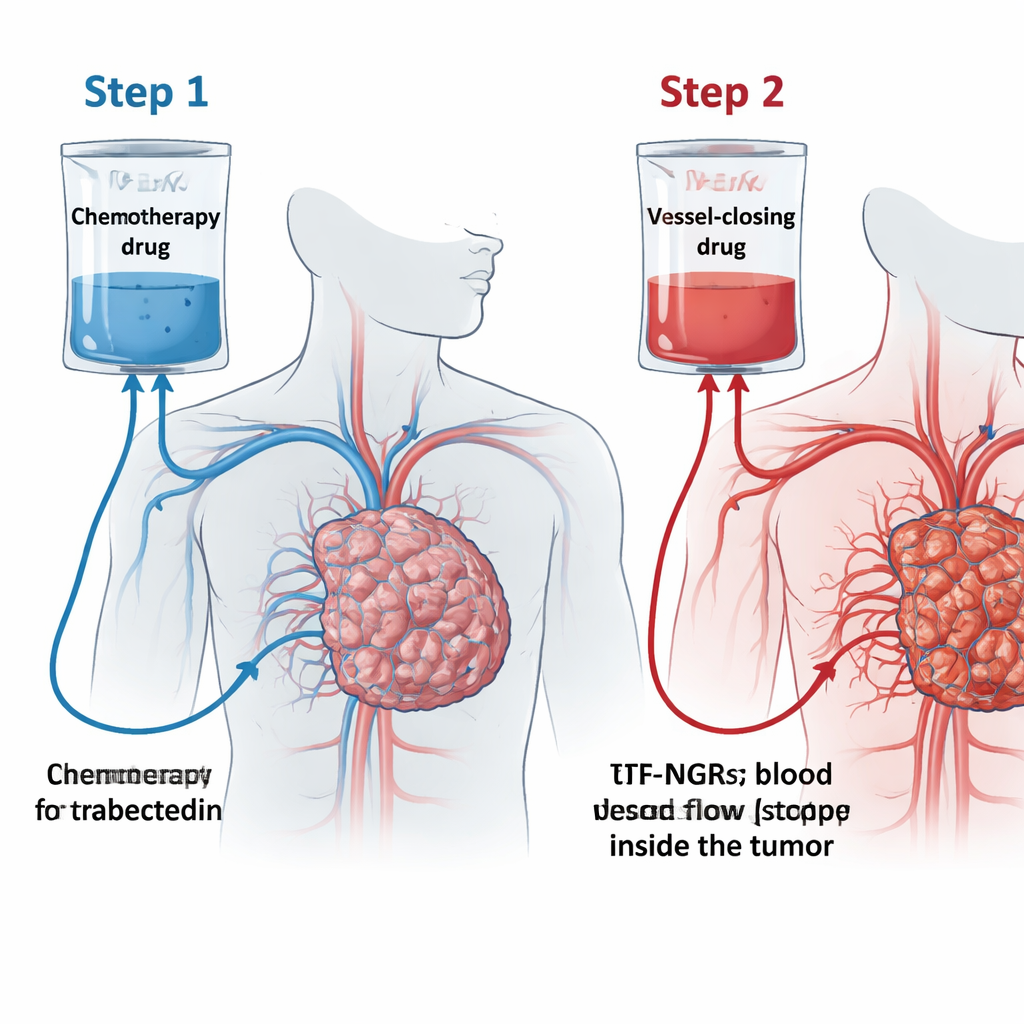
من المختبر إلى اختبارات مبكرة على المرضى
في تجارب مخبرية، أظهر الباحثون أن الترابسيديكين يجعل خلايا الأوعية الدموية وخلايا الساركومة تعرض المزيد من جزيء دهني معين على سطحها يدعم التخثر. هذا التغير جعل tTF-NGR أكثر فعالية في إثارة تشكل جلطات محلية على هذه الخلايا، وهذا بالضبط ما يلزم لإغلاق أوعية الورم. في فئران حاملة لأورام ساركومة بشرية، أدى تتابع الترابسيديكين يليه tTF-NGR إلى انكماش الأورام أكثر من كل دواء بمفرده. وبما أن الأورام الحيوانية تحللت تمامًا تحت التركيبة، لم يتمكن الفريق من قياس مقدار الترابسيديكين المحتجز بدقة، لكن السيطرة الأقوى على الورم دعمت الفكرة الأساسية للفخ.
إيجاد جرعة آمنة في مرضى حقيقيين
جوهر هذه الورقة هو مرحلة «البدء» المتعلقة بالسلامة في تجربة TRABTRAP على 19 مريضًا يعانون من ساركومات طرية متقدمة وخضعت لعلاجات كثيرة سابقًا. تلقى جميع المرضى الجرعة القياسية من الترابسيديكين. الدواء الثاني، tTF-NGR، بدأ عند أعلى جرعة تم تحملها سابقًا عند استخدامه بمفرده، ثم خُفضت بعناية عند ظهور آثار جانبية خطيرة. عند الجرعات الأعلى، أصيب بعض المرضى بمشكلات قلبية أو تخثرية ملحوظة، مثل إصابة صامتة لعضلة القلب تُرى في اختبارات الدم، جلطات رئوية صغيرة، أو خثار وريدي عميق. كانت هذه الأحداث قابلة للعكس بالعلاج وإيقاف أو تقليل tTF-NGR، لكنها أشارت إلى ضرورة خفض الجرعات. عند 0.5 ملغ/م² من tTF-NGR يُعطى في يومين بعد الترابسيديكين، أكمل ستة مرضى دورتين على الأقل دون سمية محددة الجرعة، واستمر بعضهم حتى 14 دورة.
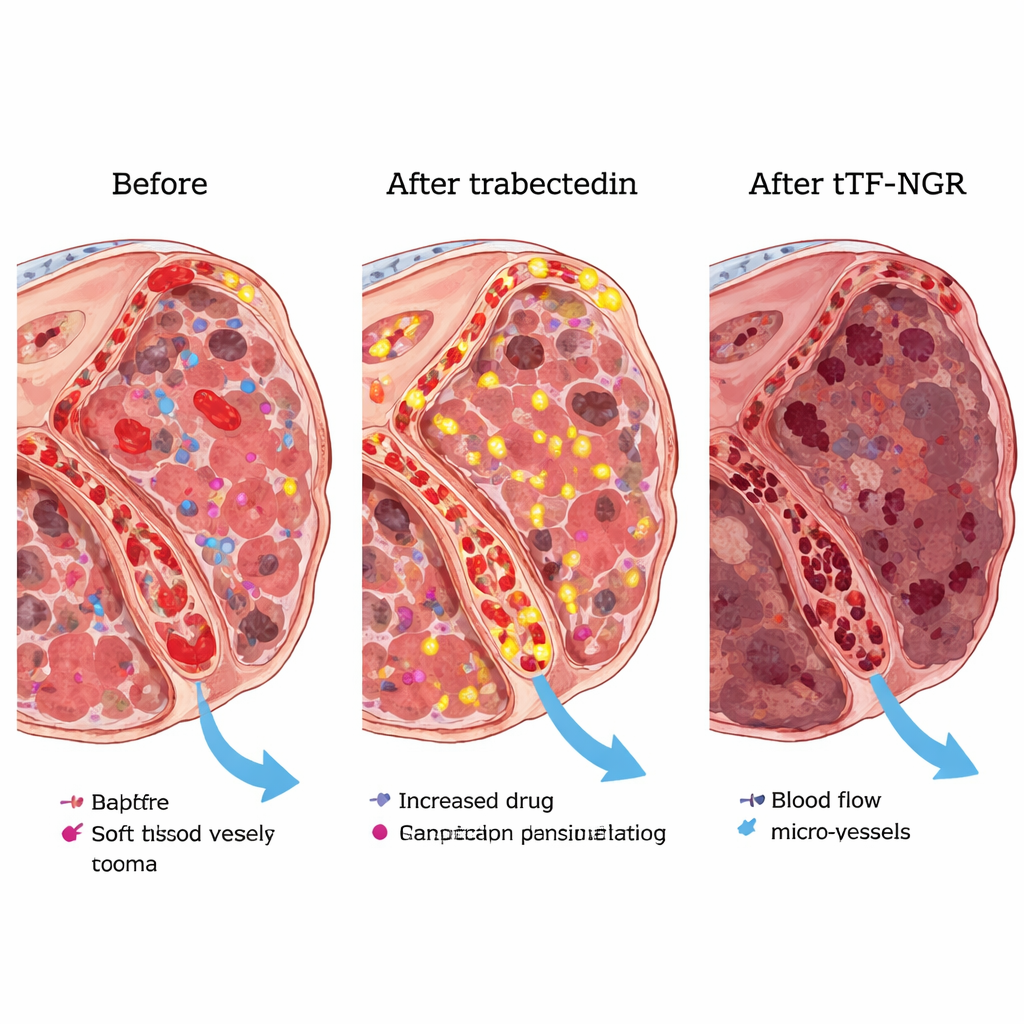
دلائل مبكرة للفائدة وكيفيت تفاعل الدواءين
على الرغم من أن هذه الجزئية من الدراسة كانت صغيرة جدًا لإثبات الفعالية، كانت النتائج مشجعة. بين 19 مريضًا، حظي معظمهم بسيطرة على المرض على الأقل مؤقتًا، وكان لدى اثنين تقلص جزئي واضح في أورامهم. لدى المصابين بالليبو ساركومة أو الليومي وساركومة — وهما نوعان شائعان من الساركومة يستجيبان للترابسيديكين — كان ما يقرب من ثلثي المرضى لديهم مرض مستقر أو استجابات جزئية عند أول فحص رئيسي. أكدت فحوصات الرنين المغناطيسي التفصيلية في مريض واحد أن tTF-NGR عند الجرعة المختارة قد يقلل بشكل انتقائي تدفق الدم داخل بؤر الورم. أظهرت اختبارات الدم أنه عندما يُعطى بعد الترابسيديكين، يبقى tTF-NGR في الدورة الدموية لفترة أطول ويبدو أكثر نشاطًا مما هو عليه عند استخدامه بمفرده، مما يساعد على تفسير سبب كون الجرعة الآمنة في التركيبة أدنى من جرعته كدواء منفرد.
ماذا يعني هذا للمرضى
بالنسبة للأشخاص المصابين بساركومة طرية متقدمة، يمثل TRABTRAP محاولة مصممة بعناية لاستخلاص المزيد من دواء كيميائي موجود عبر إقرانه بعامل يغلق الأوعية ويستهدف إمداد الورم الدموي. تُظهر مرحلة البدء المتعلقة بالسلامة أنه، بعد تعديل الجرعات، يمكن إعطاء هذا المزيج بشكل متكرر، مع آثار جانبية مهمة لكنها عمومًا قابلة للإدارة والانعكاس تحت مراقبة دقيقة. وبينما لا يزال من المبكر القول ما إذا كان سيطيل الحياة أو يسبب تقلصات متسقة للأورام، فإن السيطرة المبكرة المشجعة على المرض والتأثيرات الواضحة على تدفق دم الورم تبرران التقدم نحو تجربة عشوائية أكبر. إذا جاءت النتائج المستقبلية إيجابية، فقد تفتح هذه المقاربة ذات المرحلتين طريقًا جديدًا لعلاج الساركومات وقد تُلهم استراتيجيات مماثلة لأنواع سرطانية أخرى صعبة العلاج.
الاستشهاد: Hessling, K., Brand, C., Schwöppe, C. et al. Trabectedin plus CD13-targeted tissue factor tTF-NGR against advanced relapsed or refractory soft tissue sarcoma: translational data, clinical safety and efficacy. Sci Rep 16, 7389 (2026). https://doi.org/10.1038/s41598-026-40362-4
الكلمات المفتاحية: الساركومة الطرية, ترابسيديكين, أوعية دم الورم, علاج التخثر المستهدف, العلاج الكيميائي المركب