Clear Sky Science · ar
الكشف المعتمد على الليكتين وتصنيف التعبير عن الغلايكو-RNA الطبيعي
الحمض النووي الريبي يلبس أغطية سكرية
تحمل خلايانا أعدادًا هائلة من جزيئات الحمض النووي الريبي، المعروفة أساسًا كالرُسُل التي تساعد في تحويل الجينات إلى بروتينات. خلال السنوات الأخيرة، اكتشف العلماء مفاجأة: بعض أنواع الحمض النووي الريبي مُزينة بسكريات معقّدة وتظهر حتى على سطح الخلايا. يبدو أن هذه الحمضيات النووية الريبية "المكسوة بالسكر"، المسماة غلايكو-RNA، تؤثر في حركة الخلايا المناعية، وفي انتشار السرطانات، وفي استجابات أجسامنا للعدوى. الملخص المنشور هنا يقدم طريقة أبسط لاكتشاف هذه الجزيئات المراوغة ويرسم خريطة أماكن وجودها في الجسم، مما يفتح أبوابًا لتشخيصات وعلاجات جديدة.
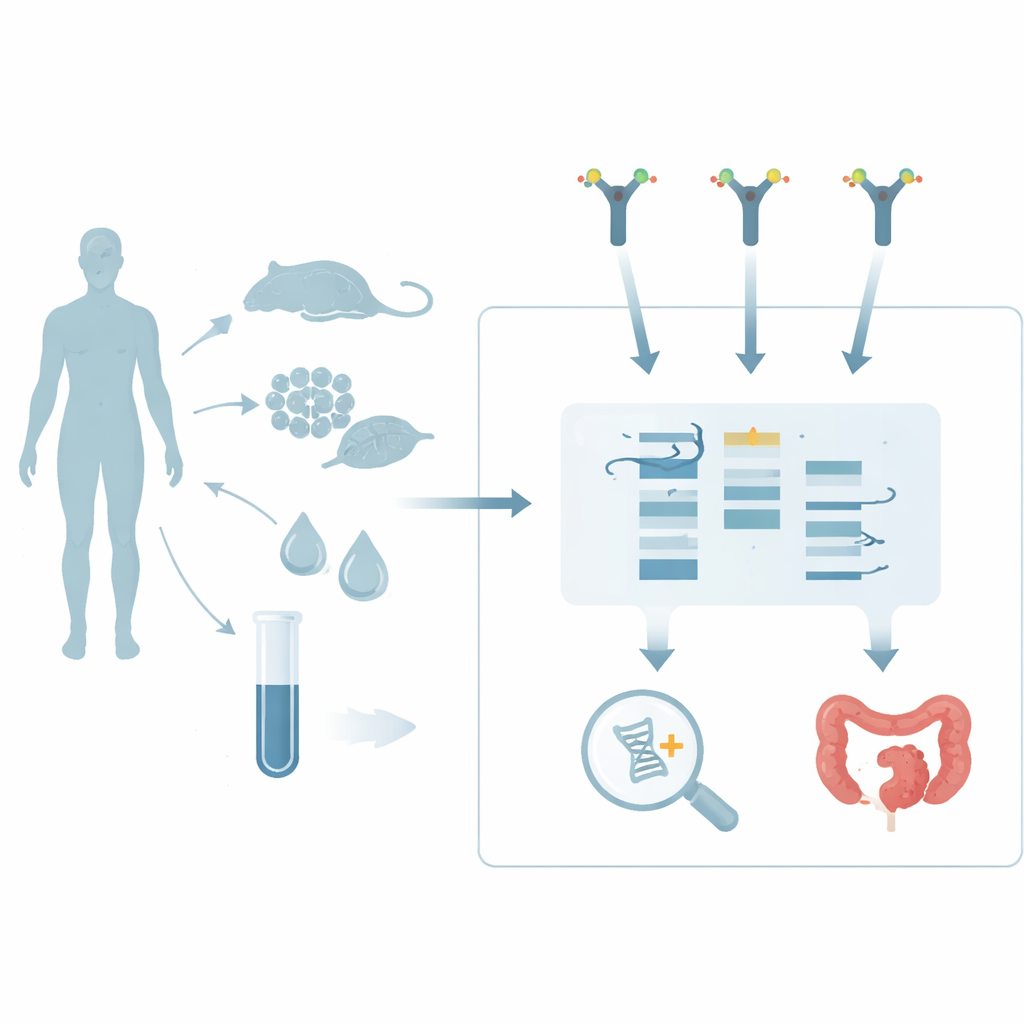
طريقة جديدة لرصد RNA المكسو بالسكر
حتى الآن، كان العثور على غلايكو-RNA يتطلب طرقًا فنية متقدمة. إحدى الطرق تجبر الخلايا الحية أو الحيوانات على امتصاص وحدات بناء سكرية اصطناعية تظهر لاحقًا على الغليكانات الجديدة، والتي يمكن بعد ذلك وسمها وتصورها. طريقة أخرى، تسمى rPAL، تُعدّل كيميائيًا أنواعًا معينة من السكريات على RNA المنقى بحيث يمكن اكتشافها. كلا الاستراتيجيتين حسّاسيتان لكن لهما عيوب: إحداهما تعتمد على أنظمة حية تمتص المجس، والأخرى ترى فقط مجموعة فرعية من غلايكو-RNA ذات أطراف سكرية محددة. طور مؤلفو هذه الورقة بديلًا أبسط يعمل مباشرة على RNA المستخرج. تعتمد طريقتهم، الكشف المعتمد على الليكتين (LBD)، على الليكتينات—بروتينات طبيعية تتعرف على أشكال سكرية معينة—للارتباط بالغلايكو-RNA على بلوت، تمامًا كما ترتبط الأجسام المضادة بالبروتينات.
تحسين تدفق عمل مخبري بسيط
لبناء LBD، عزّل الفريق أولًا إجمالي الحمض النووي الريبي من أحاديّات البلعمة البشرية المزروعة وفصلوا الجزيئات حسب الحجم باستخدام إجراء نورثرن بلوت القياسي. ثم اختبروا 24 ليكتينًا مختلفًا لقدرتهم على إبراز شريط غلايكو-RNA مميز، مقارنين النتائج مع rPAL كمرجع. نجح عدة ليكتينات، لكن واحدًا مستخلصًا من طماطم، يدعى LEL، أعطى إشارات قوية بشكل خاص وأصبح مجسّهم المفضّل. بعد ذلك حسن الباحثون خطوات روتينية—كيفية نقل RNA إلى الأغشية، نوع المادة الغشائية المستخدمة، كيفية منع الالتصاق الخلفي، مدة الحضانة، وكمية الليكتين المطبقة—حتى أصبحت الإشارات واضحة وقابلة للتكرار، مع الحفاظ على بساطة البروتوكول بما يكفي لمعمل بيولوجيا جزيئية نموذجي.
التحقق من الحساسية والخصوصية وما هو الذي يُرى
سؤال أساسي هو ما إذا كانت LBD حسّاسة ومحددة حقًا لغلايكو-RNA. بمقارنة LBD جنبًا إلى جنب مع الوسم الأيضي وrPAL عبر نطاق من كميات RNA، وجد المؤلفون أن LBD يستطيع اكتشاف ما يقارب نصف ميكروغرام من إجمالي RNA، في مستوى مماثل للطرق المعيارية. لاختبار الخصوصية، عالجوا عينات RNA بإنزيمات تقطع RNA أو DNA أو البروتينات، أو تقطع السكريات المرتبطة بالغلايكو-RNA (السكريات المرتبطة بشكل N). لم تزل الإشارة إلا بالعلاجات التي دمرت RNA نفسه أو أزالت سلاسل السكر؛ بينما لم تؤثر الإنزيمات القاطعة للـDNA أو هاضمة البروتين. قللت الأدوية التي تمنع بناء الغليكان داخل الخلايا أيضًا إشارة LBD بشكل حاد. معًا، تظهر هذه الاختبارات أن الطريقة المعتمدة على الليكتين تستجيب فعليًا لحمض نووي ريبي معدل بالسكر وليس لشوائب.
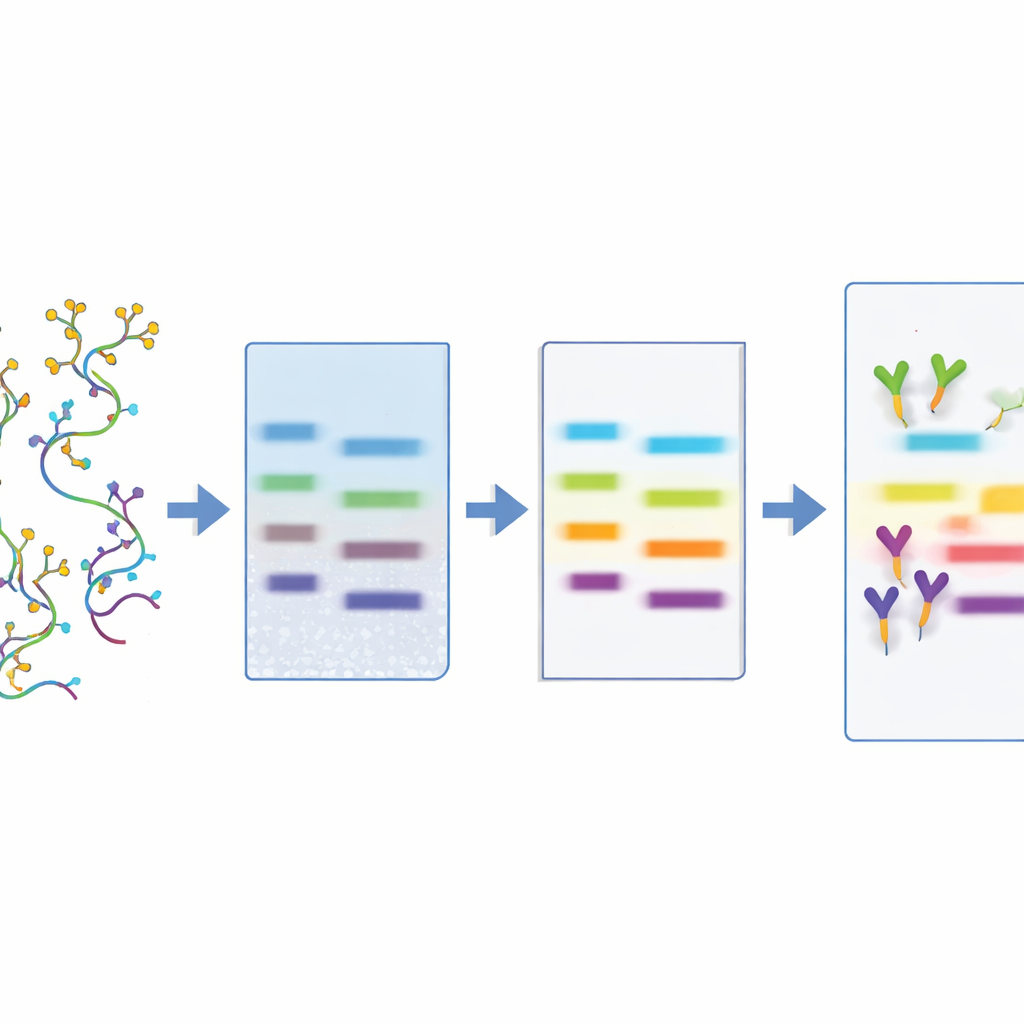
أين تظهر RNA المكسوة بالسكر في الصحة والمرض
مع امتلاك الطريقة، أجرى الفريق مسحًا لأماكن ظهور الغلايكو-RNA في مجموعة واسعة من الخلايا والأنسجة وسوائل الجسم من فئران، وفئران جرذان، وبشر. وجدوا إشارات قوية بشكل خاص في الخلايا المرتبطة بالمناعة (مثل أحاديّات البلعمة، والعدلات، وكريات الدم البيضاء)، وفي الأعضاء التي تشكّل حواجز تجاه العالم الخارجي (كالأمعاء ومجرى التنفس)، وفي مناطق معينة من الدماغ والقلب. من اللافت أن الغلايكو-RNA كانت غائبة أو منخفضة جدًا في بعض الأعضاء الرئيسية، بما في ذلك الكبد والكلى والعضلات الهيكلية. كشفت LBD أيضًا عن أشرطة متعددة في بعض الأنسجة، واعترفليكتينات مختلفة بمجموعات فرعية مختلفة من الأشرطة، مما يوحي بوجود "نكهات" غلايكو-RNA متنوعة بتزيينات سكرية مميزة. والأهم من ذلك، اكتشف المؤلفون غلايكو-RNA حرة في بلازما الإنسان والبول والبراز والسائل الأمنيوسي، مما يوحي بأن هذه الجزيئات قد تدور خارج الخلايا ويمكن أخذ عينات منها عبر اختبارات غير تدخلية إلى حد ما.
روابط مع السرطان واستخدامات طبية مستقبلية
استقصت الدراسة أيضًا كيفية تغير أنماط الغلايكو-RNA في السرطان. في عينات بشرية مطابقة، أظهرت أورام الثدي والقولون مستويات أعلى من الغلايكو-RNA مقارنةً بنظرائها الطبيعية، مع أقوى الإشارات في المرض النقيلي. في سرطان الثدي النقيلي، هاجرت أشرطة الغلايكو-RNA بشكل مختلف على الهلام مقارنةً بتلك المستمدة من الأورام الأولية، ما يوحي بتغيّرات بنيوية قد تتزامن مع تقدم المرض. مثل هذه المتغيرات المرتبطة بالأورام قد تساعد في التفريق بين السرطانات العدوانية أو توجيه العلاجات الموجَّهة في نهاية المطاف. وبما أن LBD يستخدم مواد متاحة بسهولة ويتجنب خطوات وسم الكائنات الحية، فإنه يوفر وسيلة عملية لفحص العديد من العينات ومقارنتها عبر طرق مختلفة، كاشفًا كيف تبرز استراتيجيات الكشف المتباينة مجموعات متداخلة لكن غير متماثلة من غلايكو-RNA.
لماذا هذا مهم للصحة اليومية
بعبارات بسيطة، يوفر هذا العمل مجموعة أدوات لرؤية فئة جديدة معترف بها من الجزيئات البيولوجية التي تساعد الخلايا على التحدث مع بعضها، خصوصًا في الجهاز المناعي وعلى أسطح الجسم المواجهة للميكروبات والسموم. من خلال إظهار أن مجسًا بسيطًا لالتصاق السكر يمكنه الكشف بثقة عن الغلايكو-RNA عبر الأنسجة وفي سوائل الجسم وفي السرطانات، يضع البحث أساسًا لتحويل هذه الجزيئات إلى مؤشرات للالتهاب أو العدوى أو انتشار الورم. وبالرغم من الحاجة إلى اختبارات إكلينيكية أكثر حساسية ودراسات وظيفية أعمق، يجعل الكشف المعتمد على الليكتين من الأسهل بكثير للعديد من المختبرات استكشاف أماكن وجود الغلايكو-RNA والأدوار التي تؤديها في الصحة والمرض.
الاستشهاد: Li, Y., Qian, Y., Li, X. et al. Lectin-based detection and expression profiling of native glycoRNAs. Sci Rep 16, 9031 (2026). https://doi.org/10.1038/s41598-026-40291-2
الكلمات المفتاحية: غلايكو-RNA, الكشف المعتمد على الليكتين, RNA على سطح الخلية, المؤشرات البيولوجية, انتشار السرطان