Clear Sky Science · ar
اختيار أمثلة تكيفي لكشف الانقسام الخلوي القابل للتفسير في علم الأمراض الرقمي المبني على النماذج الأولية
لماذا هذا مهم لرعاية السرطان
عندما ينظر أخصائيو علم الأمراض إلى عينات السرطان تحت المجهر، يساعد عد الخلايا الورمية التي تنقسم بنشاط في تحديد مدى عدوانية السرطان واختيار العلاجات المناسبة. يمكن للذكاء الاصطناعي الآن تحديد هذه الخلايا المتقسمة بسرعة في الشرائح الرقمية، لكن قراراته غالبًا ما تظل غامضة حتى بالنسبة للخبراء. تقدم هذه الورقة طريقة تسمى الاختيار التكيفي للأمثلة (AES) تتيح لنظام الذكاء الاصطناعي «عرض طريقته» عبر الإشارة إلى حالات سابقة حقيقية تدعم أو تتعارض مع كل قرار، مما يجعل كشف الانقسام الآلي أكثر شفافية وجديرة بالثقة سريريًا.
التحدّي في رصد الخلايا المنقسمة
الخلايا الورمية المنقسمة، المعروفة بالأشكال الطافرة للانقسام، صغيرة ونادرة ومختلفة بصريًا. تحت الصبغة الوردية والبنفسجية المعتادة، قد تبدو مشابهة جدًا لهياكل غير ضارة مثل الخلايا المحتضرة أو بعض الخلايا المناعية. على الخبراء البشريين أن يمسحوا شرائح رقمية ضخمة للعثور عليها، وهي عملية بطيئة ومرهقة ومعرضة للاختلافات في التقييم. يمكن لأنظمة التعلم العميق الحديثة أن تضاهي أو تتفوق على أداء الخبراء في هذه المهمة، لكنها تتصرف كصناديق سوداء: تعطي درجة لكل خلية مشتبه بها دون تفسير واضح. في الطب، حيث قد تكون قرارات العلاج مصيرية، يمثل هذا الغموض عقبة كبيرة أمام استخدام الذكاء الاصطناعي في الممارسة اليومية.
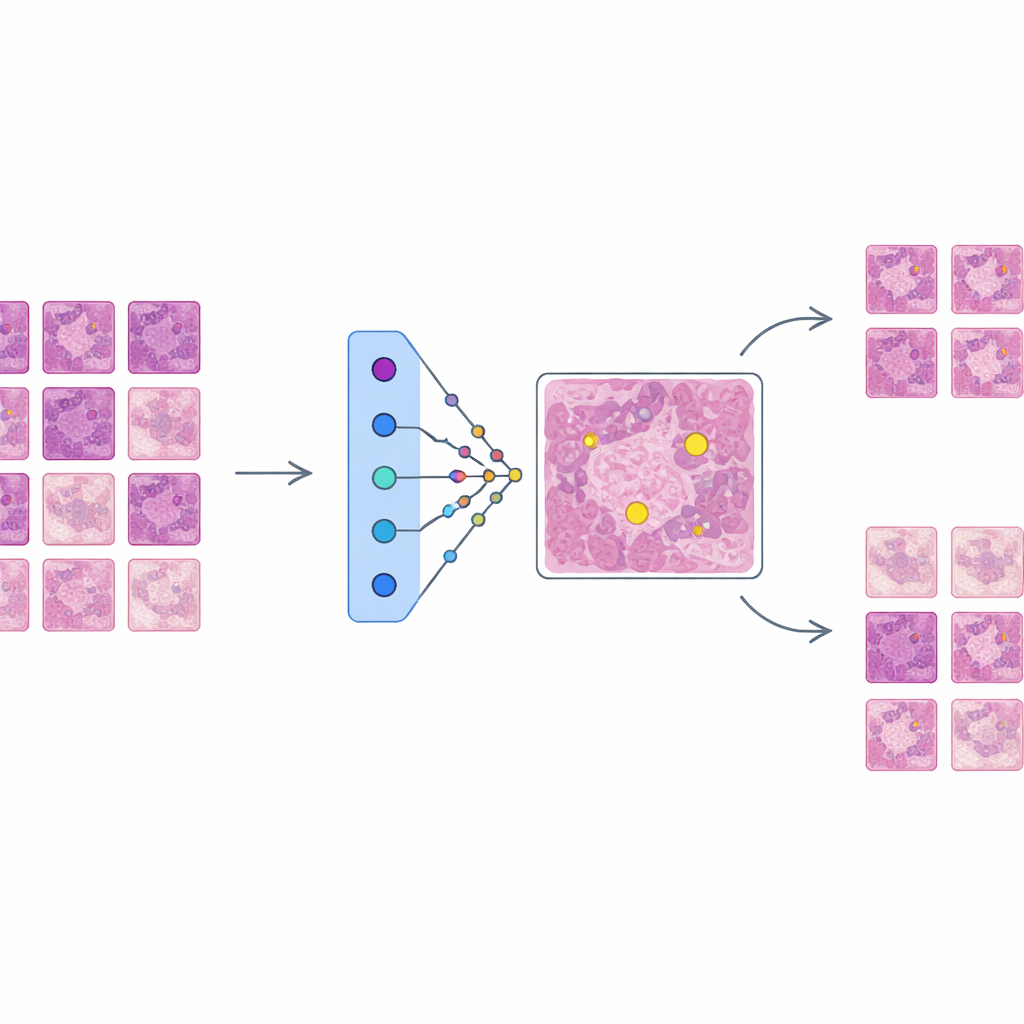
بناء كاشف قوي لكنه غامض
أولًا يدرب المؤلفون شبكة كشف أجسام متطورة مبنية على بنية Faster R-CNN للعثور على أشكال الانقسام في مجموعة بيانات كبيرة ومتنوعة تسمى MIDOG++. تأتي هذه الصور من أورام بشرية وكلبية عبر عدة أنواع سرطانية ومختبرات، وتضم أكثر من أحد عشر ألف خلية منقسمة مُعلَّمة بعناية. للحفاظ على التفاصيل الدقيقة، تُقطع الشرائح إلى رقع صغيرة وتُطبَّق عليها تحسينات مكثفة لتقليد التباينات الحقيقية في الصبغ والتصوير. يحقق الكاشف الناتج أداءً قويًا عبر أنواع الأورام، مع قيم F1 تصل حتى 0.84، مما يؤكد دقّته لكنه معقد — وهو بالضبط نوع النظام الذي يحتاج إلى تفسير أفضل قبل أن يثق به الأطباء في الممارسة السريرية.
تعليم الذكاء الاصطناعي شرح قراراته بواسطة أمثلة
تقع AES فوق هذا الكاشف المدرب كطبقة تفسيرية بدلاً من تغيير طريقة عمل الكاشف. لكل منطقة مرشحة يُشير إليها الكاشف كاحتمال انقسام، تبحث AES في مكتبة من رقع الأنسجة الحقيقية المأخوذة من بيانات التدريب. من هذه المكتبة تختار مجموعة صغيرة من الأمثلة «الداعمة» التي تشبه الانقسامات الحقيقية ومجموعة من الأمثلة «المتناقضة» التي تبدو أقرب إلى خلايا غير منقسمة. خلف الكواليس، تتعامل AES مع درجات ثقة الكاشف كمنظومة سلسة وتستخدم أداة رياضية تُسمى دوال الأساس الشعاعية لتقريب كيفية تغير هذه الثقة بالقرب من كل حالة. تُحتفظ فقط بالنماذج الأولية التي تؤثر بشكل معنوي على الثقة المحلية، لذا عادة ما تتضمن الشرح لقرار واحد نحو عشرة أمثلة مختارة بعناية بدلًا من مئات قليلة الصلة.
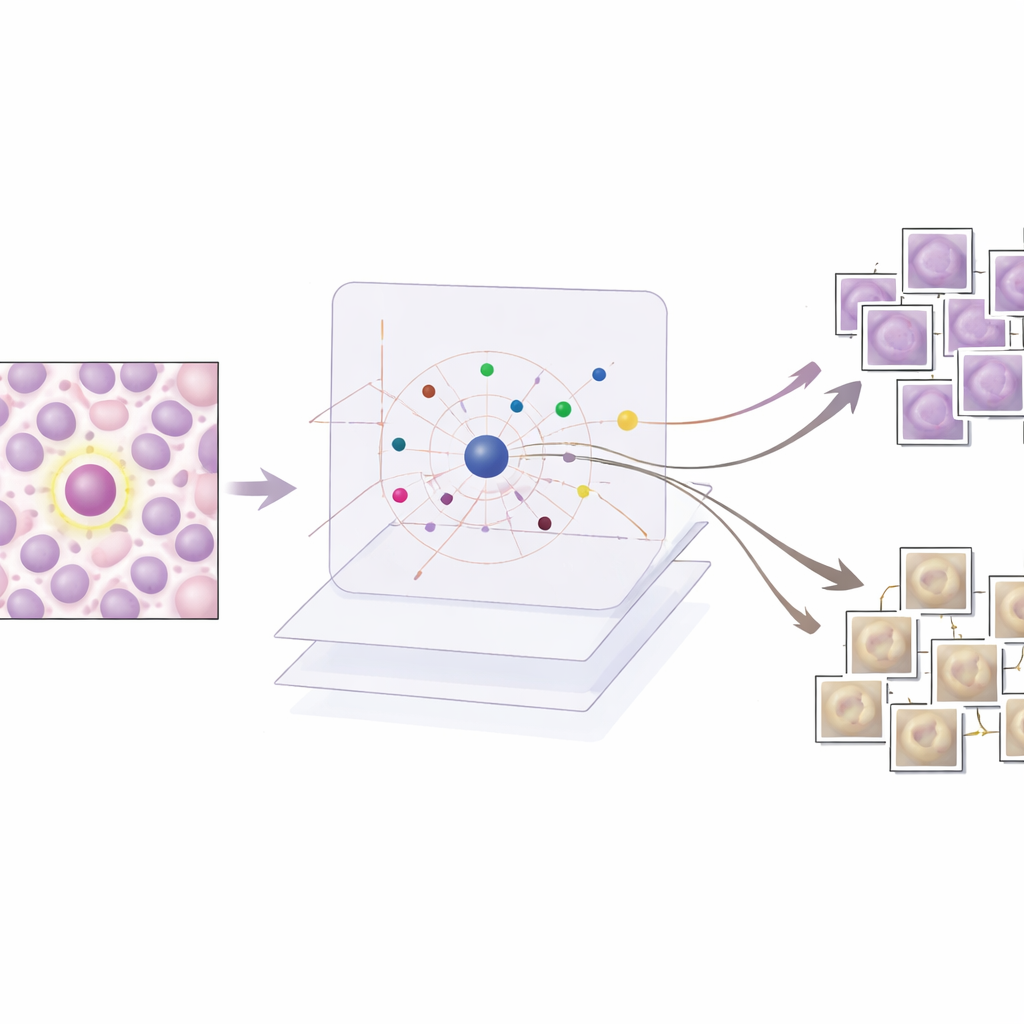
ما تكشفه الأمثلة عن قرارات الذكاء الاصطناعي
يقيم الباحثون AES كميًا وسرديًا. من الناحية الكمية، يُظهرون أن قاموسًا مُدمجًا مكوّنًا من نحو 190 صورة نموذجية يمكنه تقليد درجات ثقة الكاشف بدقة عالية جدًا، مع إبقاء عدد الأمثلة المعروضة لكل حالة منخفضًا بما يكفي لتمكين المراجعة البشرية. نوعيًا، يفحصون ثلاث سيناريوهات شائعة. عندما يكون الكاشف صحيحًا بوضوح، تعيد AES نماذج انقسام تدعم القرار بقوة، وهو أمر يطمئن الأطباء. بالنسبة للإنذارات الكاذبة، تبرز الطريقة أمثلة تشبه الانقسام تبيّن لماذا خُدع الكاشف بنسيج أو نمط كروماتين مشابه، غالبًا إلى جانب نماذج غير منقسمة أضعف تلمح إلى وجود شك. بالنسبة للانقسامات الفائتة، تميل AES إلى إرجاع نماذج غير منقسمة أو أمثلة غامضة، مما يشير إلى نقاط عمياء في بيانات التدريب ويقترح أين هناك حاجة إلى أمثلة جديدة أو مُعلمة بشكل أفضل.
من صندوق أسود إلى أداة تعاونية
عن طريق تأسيس كل توقع على حفنة من رقع الأنسجة الحقيقية والمُعلَّمة، تجعل AES كاشفًا معقدًا يتصرف بصورة أقرب إلى زميل بشري يبرر قراراته عبر تذكر حالات سابقة. لا يكتفي النظام بالإبلاغ عما إذا كانت الخلية على الأرجح منقسمة، بل يوضح السبب ومدى اليقين من خلال مزيج وتأثير النماذج الداعمة والمتناقضة. يتيح هذا التصميم لأخصائيي علم الأمراض تأكيد التوقعات الواضحة بسرعة، وتركيز الانتباه على المناطق الحدودية أو المحيرة، وتحديد أنماط الأخطاء المنهجية التي يمكن أن توجه تدريبًا لاحقًا. وعلى الرغم من تطويره لكشف الانقسام، يمكن تمديد نفس النهج إلى مهام أخرى في علم الأمراض الرقمي، مما يساعد على نقل الذكاء الاصطناعي من أتمتة غامضة نحو مساعد قابل للتفسير قائم على الحالات يمكن للأطباء الاستفسار عنه والثقة فيه وتطويره.
الاستشهاد: Banik, M., Kreutz-Delgado, K., Mohanty, I. et al. Adaptive example selection for prototype based explainable mitosis detection in digital pathology. Sci Rep 16, 9481 (2026). https://doi.org/10.1038/s41598-026-40283-2
الكلمات المفتاحية: الذكاء الاصطناعي القابل للتفسير, علم الأمراض الرقمي, كشف الانقسام الخلوي, نماذج قائمة على النماذج الأولية, تشخيصات السرطان