Clear Sky Science · ar
مصدر نابض فائق الشدة للإشعاع المؤين قائم على تسريع الإلكترونات بالليزر المباشر لدراسة تأثير FLASH
لماذا تهم النبضات الإشعاعية فائقة السرعة
العلاج الإشعاعي للسرطان يمشي على حبل مشدود: إعطاء إشعاع كافٍ لقتل الأورام دون التسبب في ضرر دائم للأنسجة السليمة. فكرة حديثة ومثيرة، تُسمى تأثير FLASH، تشير إلى أن إعطاء الإشعاع في وميض فائق القصر والفورية قد يحمي النسيج الطبيعي بينما لا يزال يهاجم السرطان. تقدم هذه الدراسة نوعًا جديدًا من مصادر الإشعاع التجريبية قائمًا على ليزر قوي ينتج وميضًا قصيرًا للغاية من الإلكترونات عالية الطاقة، وتستخدمه لمراقبة كيف يُستهلك الأكسجين في الماء والسوائل البيولوجية فجأة أثناء الإشعاع — عملية يُعتقد أنها مركزية في تأثير FLASH. 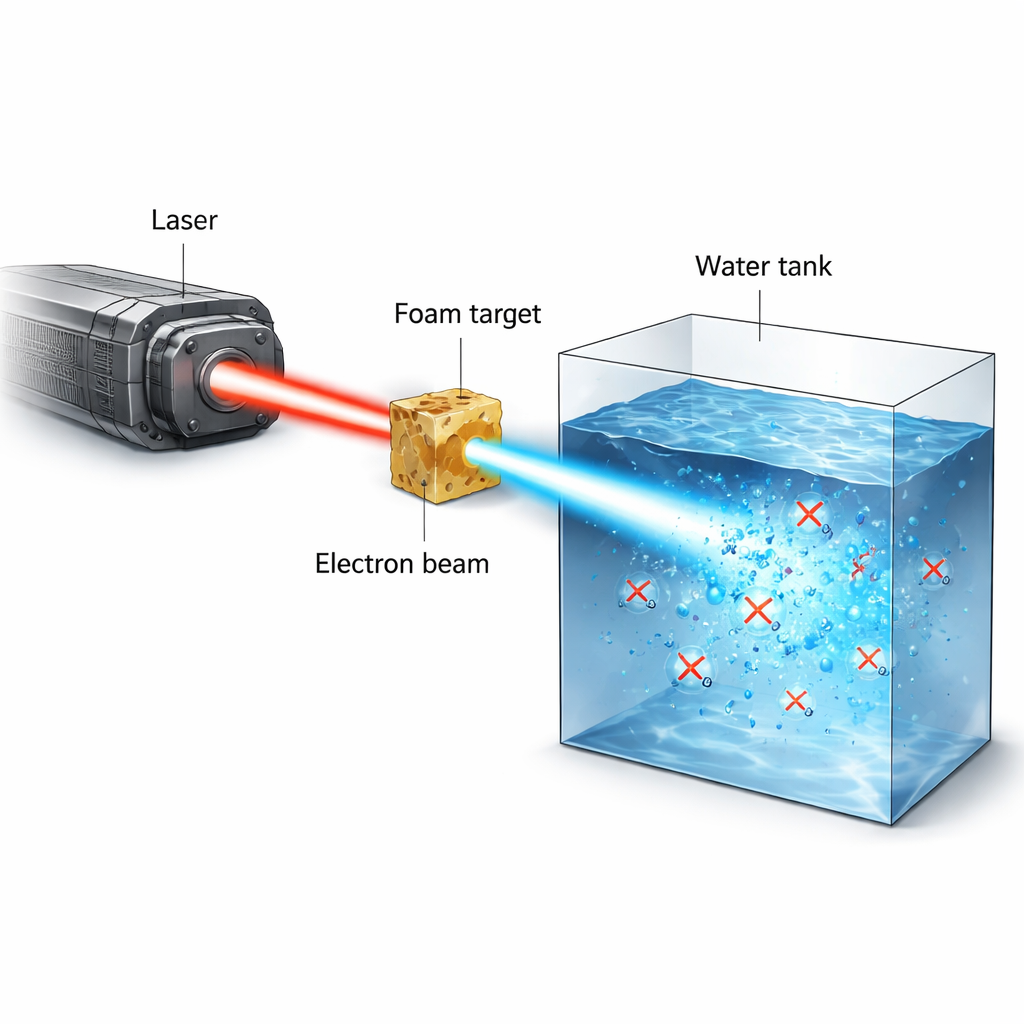
من أجهزة المستشفيات إلى الحزم المدفوعة بالليزر
يستخدم العلاج الإشعاعي التقليدي أشعة X أو إلكترونات أو بروتونات من مسرعات كبيرة. تسلم هذه الأجهزة الجرعة عادة على مدى مليثانية إلى ثوانٍ، ومع أنّها دقيقة جدًا، فإنها لا تزال تضر النسيج الطبيعي لأن الإشعاع يكسّر الماء بشكل غير مباشر مولدًا أنواعًا تفاعلية من الأكسجين التي تضر الحمض النووي. في الأنسجة السليمة جيدة التروية، يجعل الأكسجين هذا الضرر أسوأ — ما يُعرف بتأثير الأكسجين. يهدف العلاج الإشعاعي FLASH إلى قلب هذه المعادلة عبر تسليم الجرعة العلاجية كاملة في جزء صغير من الثانية وبمعدلات جرعة فائقة الارتفاع، وهو ما يبدو أنه يحمي النسيج الطبيعي مؤقتًا في دراسات حيوانية دون حماية الأورام. ومع ذلك، تكافح المسرعات الطبية التقليدية للوصول إلى هذه المعدلات القصوى، مما يدفع للبحث عن مصادر بديلة مثل الليزر عالي الطاقة.
تحويل الرغوة والضوء إلى وميض إلكتروني قوي
استخدم الباحثون ليزر PHELIX عالي الطاقة لإنشاء حزم إلكترونية ضيقة وعالية التيار بطاقة عدة ملايين إلكترون فولت (MeV). يؤين الليزر أولاً رغوة بوليمر منخفضة الكثافة إلى بلازما قريبة من الحالة الحرجة. في نبضة ثانية فائقة القصر تدوم أقل من تريليون من جزء الثانية، يدفع الليزر الإلكترونات ويحبسها داخل قناة بلازمية، مسرِّعًا إياها مباشرة إلى طاقات عالية. تُنتج هذه العملية، المسماة التسريع بالليزر المباشر، حزمة متقاربة يمكن أن تحمل عشرات نانوكولوم من الشحنة في وميض زمني على مقياس البيكوسيكند. عندما تضرب هذه الحزمة الماء أو مادة شبيهة بالماء، يمكنها إيداع 20–50 غراي من الجرعة في طلقة واحدة، بمعدلات جرعة آنية تتجاوز 10¹³ غراي في الثانية — وهو ما يفوق بكثير ما يمكن للأجهزة التقليدية تحقيقه.
مراقبة اختفاء الأكسجين في لمحة
لمعرفة كيف تؤثر مثل هذه الومضات المكثفة على الكيمياء في ظروف شبيهة بالأنسجة، بنى الفريق خزانات ماء معبأة ومحكمة يمكن تشغيلها في فراغ وملؤها إما بماء نقي أو وسط زرع خلوي أو خلايا مهضومة، جميعها مُشَبَّعة بالأكسجين مسبقًا. شكّل الباحثون عارضة الإلكترونات ومروّجوها بحيث تهيمن الإلكترونات عالية الطاقة على الجرعة داخل الخزان، بينما تم قمع البروتونات وأشعة X إلى حد كبير أو أخذها بعين الاعتبار بعناية باستخدام طبقات من الدرع وأفلام راديوكرومية. رصد حساس بصري موضوع على الجدار الداخلي للخزان الأكسجين المذاب عبر قياس كيف يُخمد الأكسجين توهُّج بقعة صبغة. بعد كل إشعاع بنبضة واحدة، سجل الحساس انخفاضًا مفاجئًا في تركيز الأكسجين ثم استرخاءًا بطيئًا مع انتشار الأكسجين داخل منطقة الحساس. من خلال الجمع بين بيانات الأفلام والمحاكاة وقوة إيقاف الإلكترونات المعروفة، أعاد المؤلفون بناء الجرعة المودعة في الحجم المشع وربطوها مباشرة بفقدان الأكسجين المقاس. 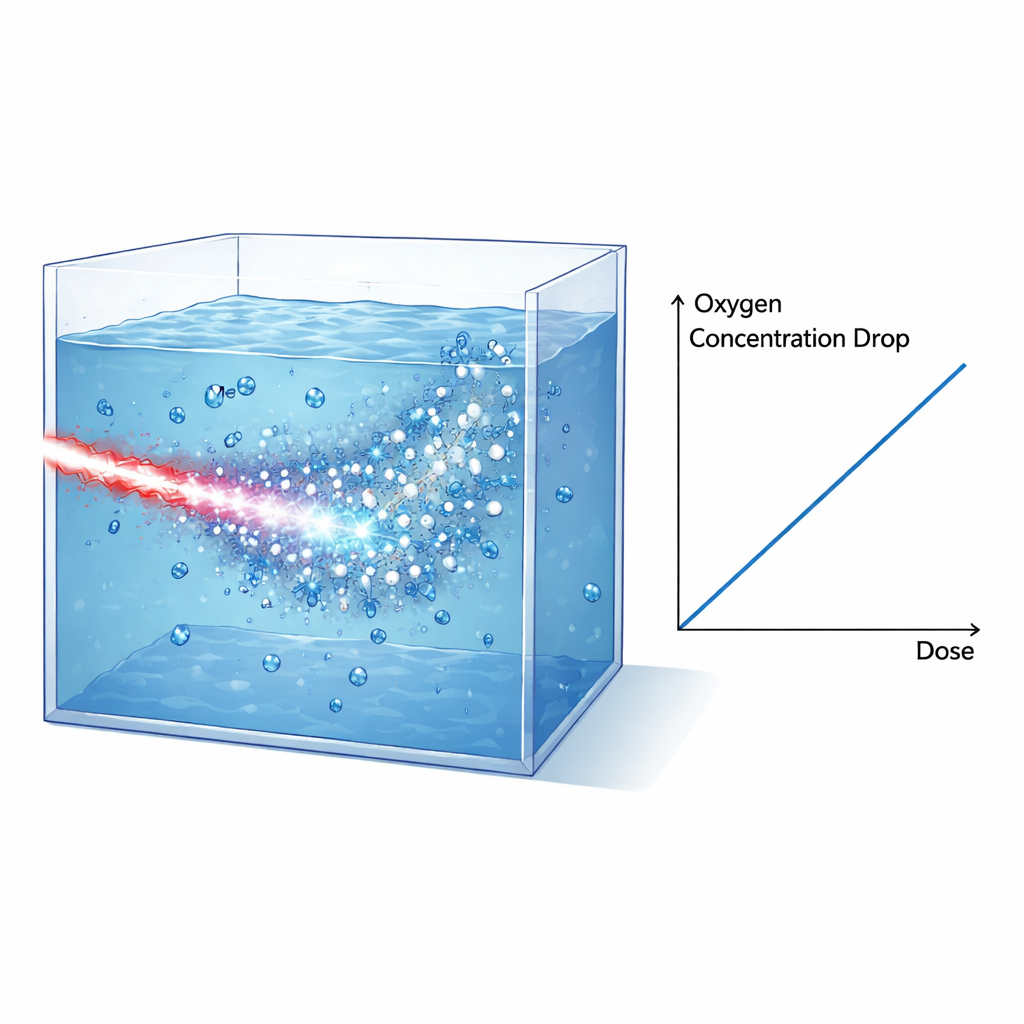
ربط التجربة والنظرية
النتيجة الأساسية هي أن الانخفاض في الأكسجين المذاب يتناسب طرديًا مع الجرعة المودعة لكل من الماء ووسط الزرع، مع انحدارات متشابهة جدًا. بعد تصحيح لجرعة إضافية صغيرة من أشعة X، يكون استهلاك الأكسجين المقاس في الماء حوالي 0.32 ميكرومول لكل لتر لكل غراي. يتطابق هذا المقدار بشكل ملحوظ مع توقعات محاكاة مسار-الهيكل مونت كارلو التفصيلية (TRAX-CHEM)، التي تتتبع مسارات الإلكترونات في الماء وتُحاكي الكيمياء السريعة التي تتكشف في ميكروثوانٍ بعد الإشعاع. والأهم من ذلك، في هذا الإعداد المدفوع بالليزر تُقدَّم تقريبًا كل الجرعة خلال نحو بيكوسيكند واحد — أقصر كثيرًا من الأزمنة المميزة للتفاعلات الكيميائية التالية. هذا يعني أن التجربة تُعيد بشكل وثيق الشروط المثالية المفترَضة في هذه المحاكاة، مما يوفّر اختبارًا صارمًا للنماذج الأساسية.
بناء منصة اختبار أفضل لعلوم FLASH
إلى جانب التحقق من النظرية، يستخدم المؤلفون نتائجهم لتصميم تخطيط تجريبي محسّن. من خلال تبسيط الهندسة، وإزالة المغناطيسات، ووضع الماء وأفلام قياس الجرعة بشكل متماثل حول الحزمة، يمكن للتجهيزات المستقبلية قياس الجرعة داخل الخزان مباشرة دون إعادة بناء معقّدة، مع مزيد من القمع لمساهمات البروتونات وأشعة X غير المرغوب فيها. تُظهر المحاكيات أن تعديل الهدف — مثل إضافة طبقات رقيقة من البلاستيك أو الذهب — يسمح بضبط الجرعة لكل طلقة بين نحو 40 و80 غراي، موفّراً منصة مرنة لاستكشاف نطاق واسع من الشروط ذات الصلة بـFLASH.
ما يعنيه هذا لعلاجات السرطان المستقبلية
للغير متخصصين، الرسالة الأساسية هي أن هذا المصدر القائم على الليزر يخلق نبضات إلكترونية فائقة الكثافة وقصيرة للغاية تحاكي — وفي بعض النواحي تتجاوز — الظروف المتصورة لعلاج FLASH الإشعاعي. تُظهر الدراسة أن هذه النبضات تستهلك بسرعة الأكسجين المذاب في الماء والوسائط البيولوجية بطريقة تتفق مع التنبؤات النظرية المتقدمة. وبما أن نقص الأكسجين والكيمياء الجذرية المرتبطة بهما هما من المرشحين الرئيسيين لشرح سبب حفاظ FLASH على الأنسجة السليمة، فإن وجود مصدر متحكم به ومفهوم جيدًا كهذا يعد خطوة مهمة إلى الأمام. فهو يوفر منصة اختبار قوية لتنقيح النماذج وفي النهاية لتوجيه تصميم الآلات السريرية المستقبلية التي قد تعالج السرطان بفعالية أكبر مع تقليل الآثار الجانبية.
الاستشهاد: Gyrdymov, M., Bukharskii, N., Fabian, V. et al. Ultra-intense pulsed source of ionizing radiation based on direct laser acceleration of electrons for studying the FLASH effect. Sci Rep 16, 7164 (2026). https://doi.org/10.1038/s41598-026-40281-4
الكلمات المفتاحية: العلاج الإشعاعي FLASH, الإلكترونات المدفوعة بالليزر, معدل جرعة فائق الارتفاع, نقص الأكسجين, تحلل الماء بالإشعاع