Clear Sky Science · ar
التحليل متعدد الوسائط لبدايات ونمو الجلطة الناجمة عن التدفق في أجهزة الاكسجة خارج الجسم
لماذا تهم جلطات الدم في أجهزة دعم الحياة
الاكسجة خارج الجسم، أو ECMO، هي شكل من أشكال تجاوز عمل القلب والرئتين يمكنه إبقاء المرضى في حالات حرجة على قيد الحياة أثناء تعافي أعضائهم. لكن ضخ الدم عبر مضخات وأنابيب بلاستيكية يعرضه لقوى ميكانيكية قاسية لم تُصمم أجسامنا لتحملها. هذه القوى قد تحفّز تشكّل جلطات خطيرة داخل الدائرة، مما يزيد بدوره من خطر السكتة الدماغية، أو تلف الأعضاء، أو فشل الجهاز. هدفت هذه الدراسة إلى كشف الكيفية التي يشكّل فيها تدفق الدم عبر مضخة ECMO ولادة ونمو هذه الجلطات، بهدف بعيد المدى جعل ECMO أكثر أمانًا وفعالية.
كيف يحافظ ECMO على حياة المرضى
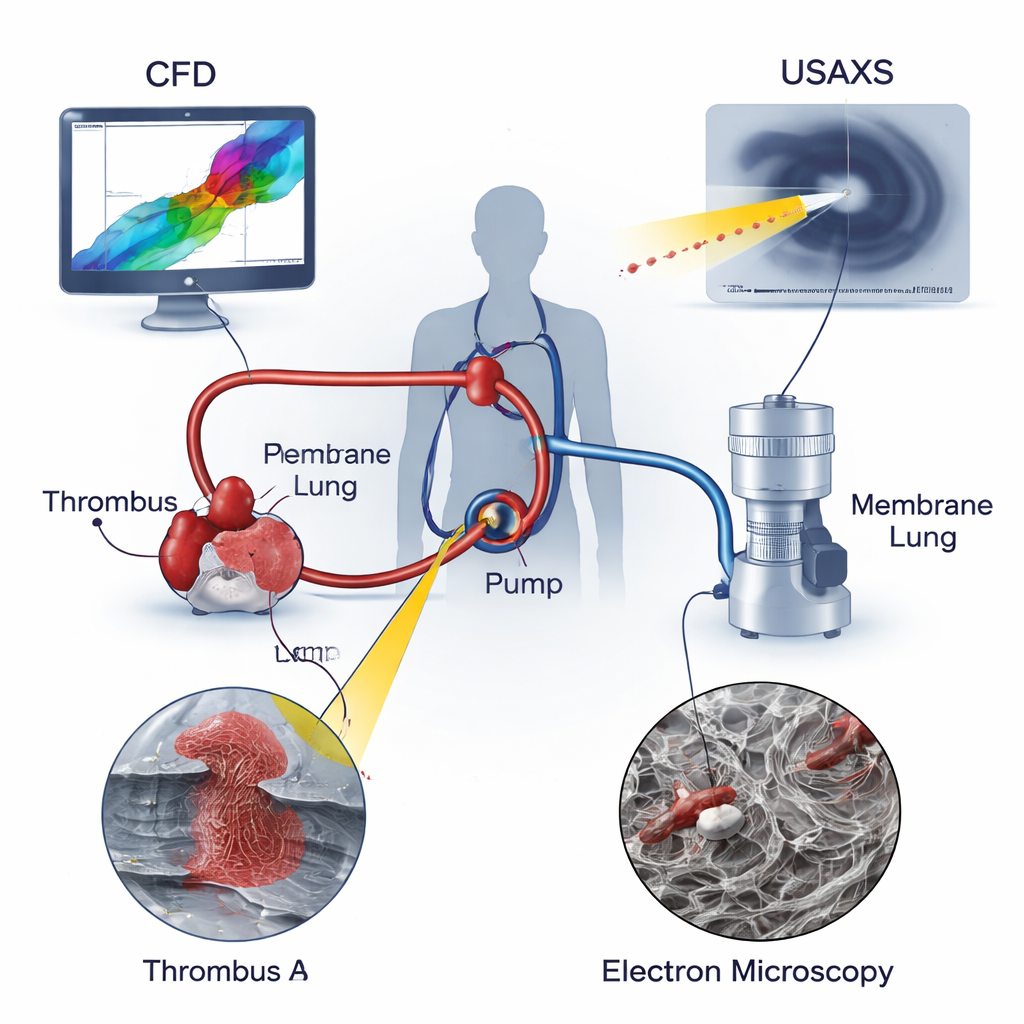
في ECMO، يُسحب الدم من وريد أو شريان كبير، وتدفعه مضخة طرد مركزي عبر «رئة غشائية» تضيف الأكسجين وتزيل ثاني أكسيد الكربون، ثم يعود إلى المريض. على خلاف الدم الذي يتدفّق بسلاسة عبر الأوعية الطبيعية، يتضمّن التدفق في دارة ECMO ظروفًا قصوى: تيارات سريعة جدًا، تغيّرات حادة في الاتجاه، وجيوب شبه راكدة حيث يتوقّف الدم لفترة. هذه البيئات معروفة بإلحاق الضرر بخلايا الدم وتحفيز التجلط. تعتمد النماذج الطبية التقليدية على التدفق البطيء أو الانسدادي في الأوعية الدموية، لكنها لا تَأخذ بالكامل بالاعتبار القص والتمدد الشديدين اللذين يتعرض لهما الدم داخل مضخة دوّارة. يرى المؤلفون أنه لفهم مخاطر التجلط في ECMO حقًا، يجب دراسة كل من القوى الميكانيكية في الجهاز والبنية المجهرية للجلطات الناشئة.
النظر إلى الجلطات من ثلاث زوايا
جمع الباحثون ثلاث أدوات قوية لتحليل جلْطتين حقيقيتين مأخوذتين من دوائر ECMO استُخدمت لدى أطفال: جلطة عند مدخل المضخة (الجلطة A) وأخرى في أنبوبية بعد المضخة مباشرة (الجلطة B). حاكات ديناميكا السوائل الحسابية (CFD) كيفية تحرّك الدم عبر المضخة، وكشفت عن مناطق تدفق معاد الدوران وتيارات دوّامية وحدّدت حيث بلغت قوى القص والتمدد ذروتها. استكشفت تشتّت الأشعة السينية عند زاوية صغيرة جدًا (USAXS) عمق كل جلطة، مقيسة مدى إحكام وتراص ومدى اتجاهية سقالة الفبرين—شبكة البروتين التي تمسك الجلطات معًا—في العينة بأكملها. قدّم التصوير المجهري الإلكتروني الماسح (SEM) صورًا مكبّرة للغاية لأسطح الجلطة، مظهرة أشكال خلايا الدم الحمراء والبيضاء والصفائح الدموية والألياف الفبرينية المحيطة. بواسطة تراكب هذه الرؤى الثلاث، تمكن الفريق من ربط ظروف التدفق المحلية بالهندسة الداخلية لكل جلطة.
منطقة إعادة الدوران تولّد جلطة صلبة ومحاذية
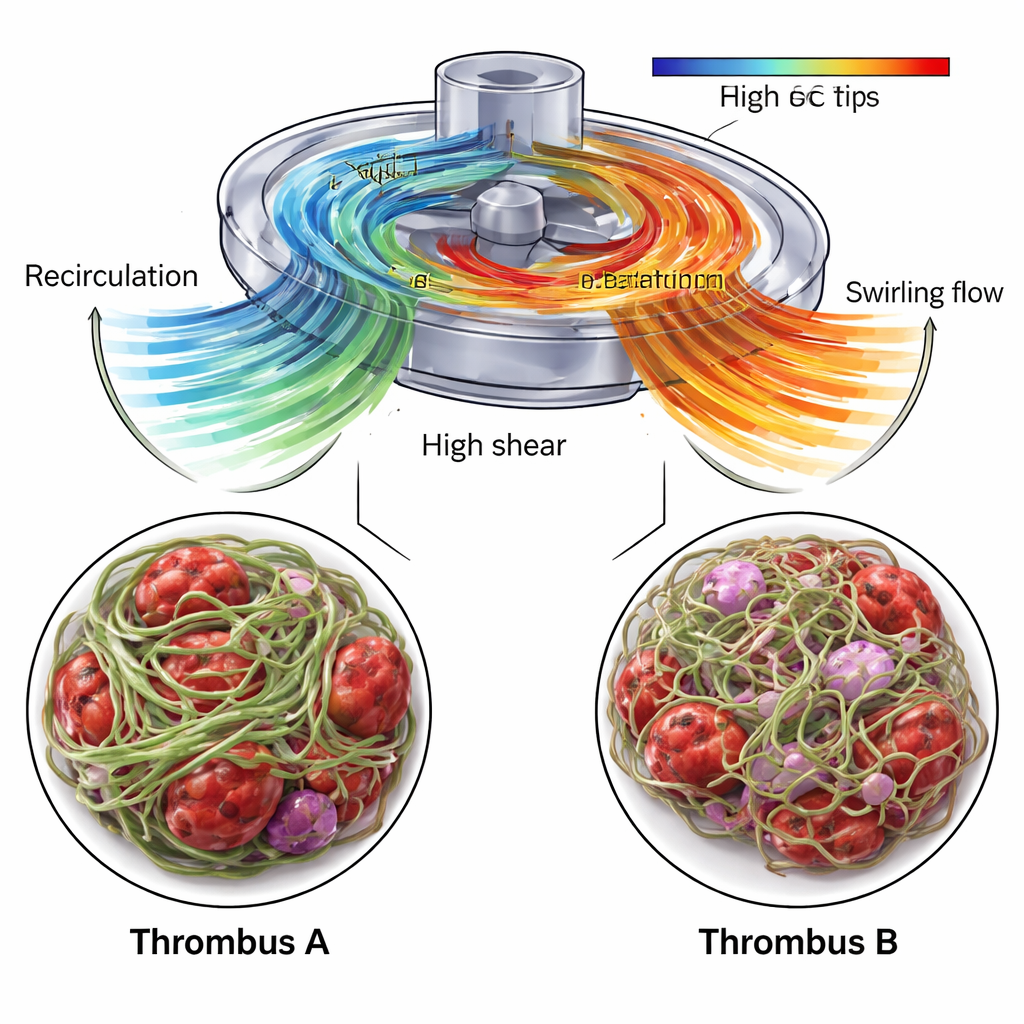
أظهرت محاكاة CFD أن المنطقة قرب مدخل المضخة، حيث تشكّلت الجلطة A، احتوت على منطقة إعادة دوران: كان الدم يُدفع إلى الخلف وللأعلى على طول جسم الحجرة قبل أن يعود إلى التيار الرئيسي. سمحت هذه المنطقة لمكوّنات الدم بالبقاء لفترة بينما كانت تتعرّض أيضًا لفروقات سرعة حادّة عند الحد الفاصل بين التدفق المعاد التدفق والتدفق الوارد. داخل الجلطة A، أشارت بيانات USAXS إلى محتوى فبرين عالٍ—لا يقل عن 70 بالمئة—ومحاذاة قوية للألياف في اتجاه مفضّل، مما يوحي بسقالة مكثفة وصلبة. أكدت صور SEM وجود شبكة منسوجة بإحكام من الفبرين، متداخلة مع خلايا دم حمراء مشوّهة وشظايا صفيحات دموية. يقترح المؤلفون أن مزيج أوقات الإقامة الطويلة والقص المحلي القوي فضّل نمو جلطة مضغوطة ومنظمة تنظيماً عالياً قادرة على تحمل الضغوط الميكانيكية للمضخة.
التدفّق الدوّامي الخارج يشكل جلطة أكثر ارتخاءً وملتوية
بالمقابل، نشأت الجلطة B، المأخوذة من الأنابيب بعد المضخة، في منطقة سيطر عليها تدفق خروجي دوّامي. كشفت محاكاة CFD عن هياكل تدفق دوّارة شبيهة باللولب تنبثق من مخرج المضخة، وأظهرت بيانات USAXS شبكة فبرين لا تزال مسيطرة لكنها أقل كثافة وأقل محاذاة بشكل عام. تحوّل الاتجاه الرئيسي لترتيب الفبرين تدريجيًا عبر الجلطة، من زاوية ميل إلى أخرى، في صدى لنمط التدفق الملتوي. أظهرت صور SEM خيوط فبرين بسمك متغيّر والعديد من خلايا الدم الحمراء والبيضاء المحبوسة، بما في ذلك دلائل على تلف الخلايا والالتهاب. ومن المهم أن المحاكاة حدّدت أيضًا أجزاء صغيرة لكنها ذات دلالة من حجم المضخة حيث كانت قوى الشد كافية لفتح عامل فون ويلبراند، وهو بروتين دموي رئيسي يصبح لاصقًا تحت الإجهاد ويمكنه جذب الصفائح بسرعة. كانت هذه المناطق مركزة قرب شفرات الدافعة والمخرج، ما يجعلها مواقع مرجّحة لبدء أحداث التفعيل التي أدّت إلى الجلطة B.
نحو أجهزة دعم حياة أكثر أمانًا
بدمج محاكاة مفصّلة لتدفق الدم مع قياسات بالأشعة السينية والمجهر الإلكتروني لجلطات ECMO الحقيقية، تُظهر هذه الدراسة أن «حبيبات» وكثافة الجلطة الداخلية تعكس البيئة الميكانيكية التي تشكّلت فيها. رُبط التدفق المعاد الدوران قرب مدخل المضخة بسقالة فبرينية كثيفة ومحاذاة عالية، في حين ارتبط الخروج الدوامي بشبكة أكثر التواءً وافتراقًا لا تزال تحبس العديد من خلايا الدم والخلايا المناعية. تبرز هذه الرؤى مناطق محددة في مضخات وأنابيب ECMO حيث قد تكون تغييرات التصميم أو تعديلات مستهدفة في مضادات التخثر الأكثر فعالية لتقليل مخاطر الجلطة. على المدى الطويل، قد يوجّه هذا النمط متعدد المقاييس—من هندسة المضخة وأنماط التدفق وصولًا إلى ترتيب البروتين—تصاميم أجهزة أكثر أمانًا ويساعد الأطباء على تحقيق توازن أفضل بين مخاطر النزف والتخثر أثناء دعم ECMO المنقذ للحياة.
الاستشهاد: Nilsson, F., Sochor, B., Henriksson, S. et al. Multimodal characterization of flow-induced thrombus initiation and growth in extracorporeal membrane oxygenation. Sci Rep 16, 7166 (2026). https://doi.org/10.1038/s41598-026-40177-3
الكلمات المفتاحية: ECMO, تجلط الدم, إجهاد القص, مضخة دم طرد مركزي, بنية الفبرين