Clear Sky Science · ar
سيبروفول يقلل إصابة نقص التروية–إعادة التروية الدماغية في الفئران عن طريق تثبيط الفيروبتوز عبر زيادة تعبير AMPK
لماذا حماية الدماغ بعد السكتة مهمة
عندما يصاب شخص بسكتة إقفارية، يتسابق الأطباء لفتح الوعاء الدموي المسدود واستعادة تدفّق الدم إلى الدماغ. ومفارقةً، قد يتسبب هذا الإجراء المنقذ للحياة في ضرر إضافي بحد ذاته، وهو ما يُعرَف باسم إصابة إعادة التروية. فالدماغ، الذي يغمره فجأة الأكسجين والمواد المغذية بعد فترة من الحرمان، يطلق عاصفة من التفاعلات الكيميائية التي قد تقتل الخلايا العصبية الضعيفة. تستقصي هذه الدراسة ما إذا كان سيبروفول، وهو مخدر جديد يُستخدم بالفعل للتخدير والتهدئة، يمكن أن يعمل أيضاً كعامل واقٍ للدماغ خلال هذه النافذة الحرجة عن طريق تهدئة بعض أكثر العمليات الضارة التي تُثار بعد عودة الدم.
من انسداد تدفّق الدم إلى تلف الدماغ
لمحاكاة ما يحدث في السكتة البشرية، قام الباحثون بسد شريان دماغي رئيسي مؤقتاً في الفئران ثم أعادوا تدفّق الدم، محدثين ما يُعرف بإصابة نقص التروية–إعادة التروية الدماغية. خضعت بعض الفئران للإجراء وحده، بينما تلقت أخرى سيبروفول بعد إعادة تدفّق الدم بقليل. قيّم الفريق بعد ذلك قدرة الحيوانات على الحركة والاستجابة للمس، وفحص أدمغتها بحثاً عن مناطق نخر وهيكلية تالفة في الخلايا العصبية. أظهرت الفئران التي تلقت سيبروفول مناطق إصابة دماغية أصغر، وخلايا عصبية ذات مظهر أكثر صحة، ودرجات حركة وحسّية أفضل مقارنة بالحيوانات غير المعالجة، ما يشير إلى أن الدواء خفف أسوأ تبعات الإصابة.
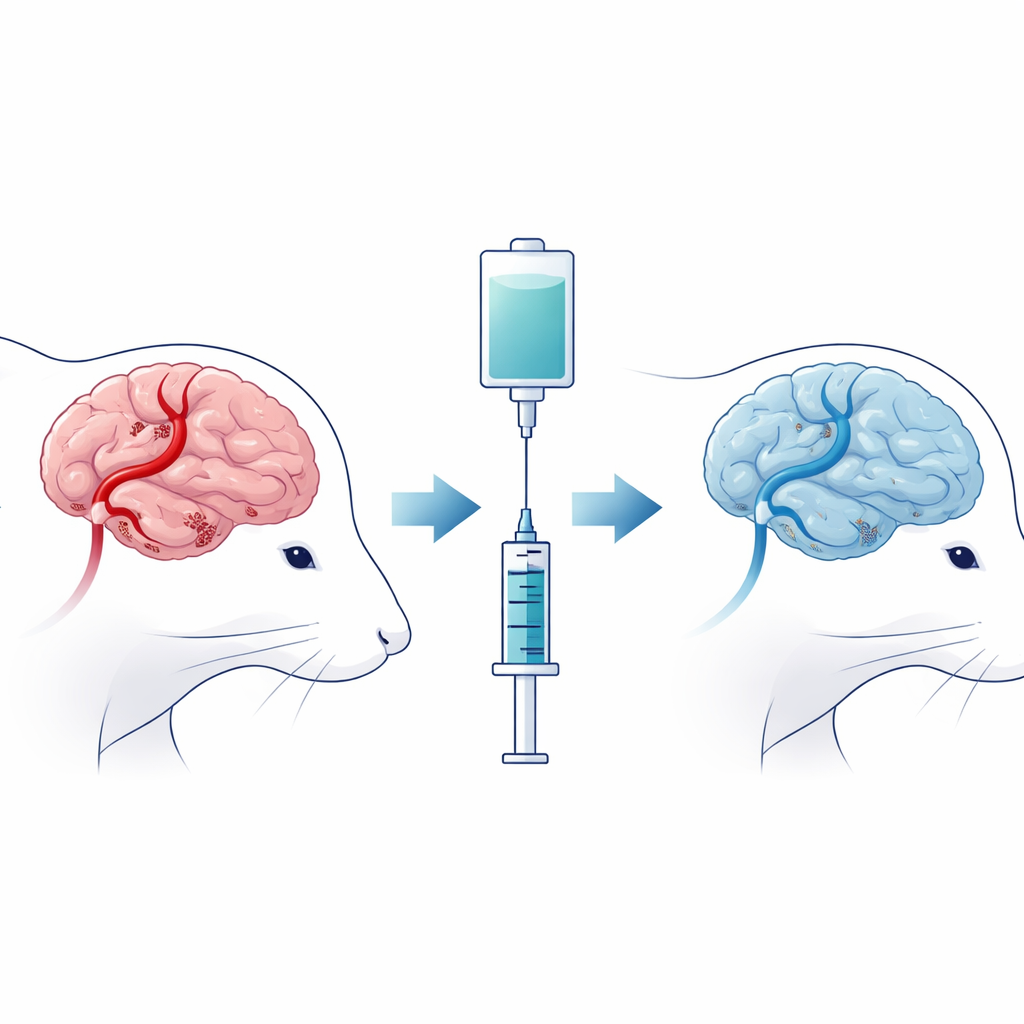
شكل خفي من موت الخلايا يغذّيه الحديد
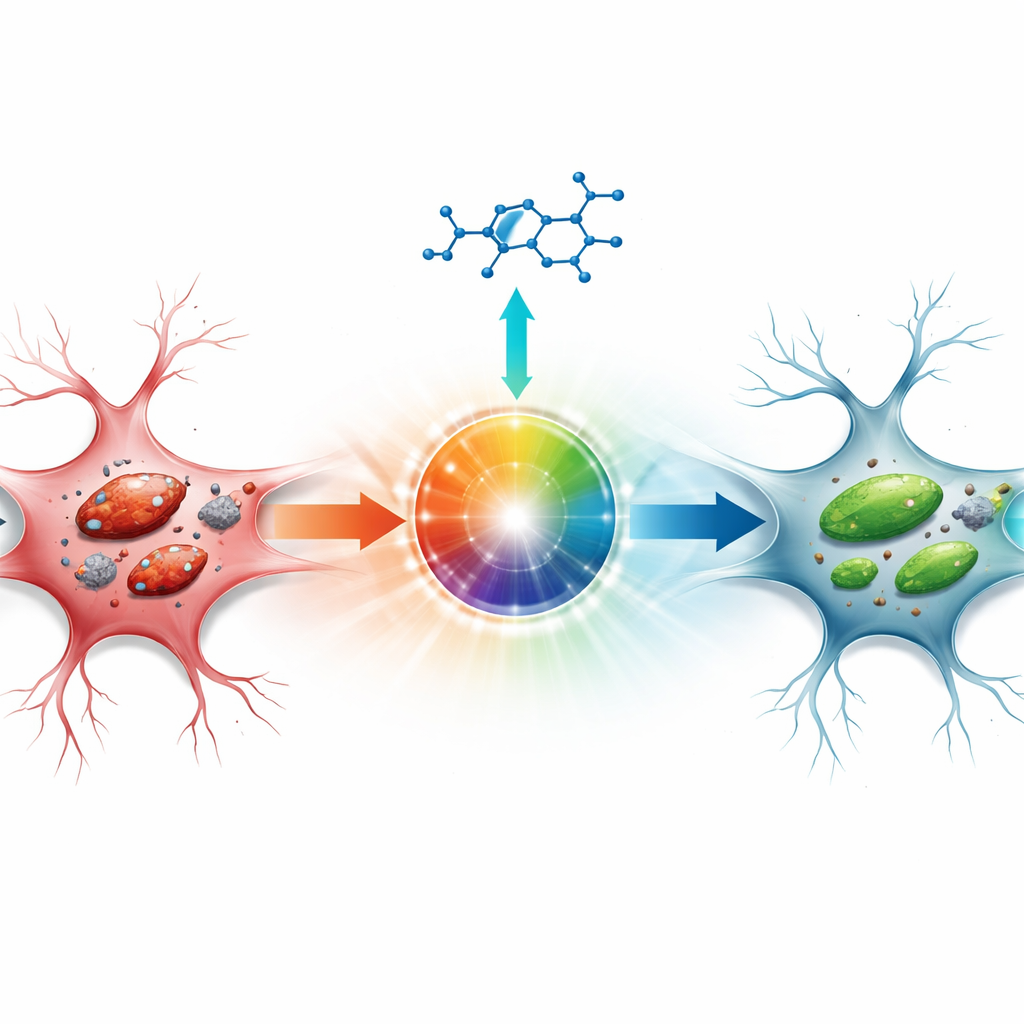
بعيداً عن التلف النسيجي الظاهر، ركز المؤلفون على نوع حديث الاعتراف به من موت الخلايا يُسمى الفيروبتوز، والذي يغذيه الحديد والتفاعلات الكيميائية الهائلة التي تهاجم المكونات الدهنية لأغشية الخلايا. في أدمغة نماذج السكتة غير المعالجة، احتوى النسيج المحيط بنواة الإصابة على مستويات أعلى من الحديد، وكميات أكبر من نواتج تلف الدهون، وبدت متقدرات الخلايا العصبية منتفخة ومُتلفة هيكلياً تحت المجهر الإلكتروني. أظهرت الاختبارات الجزيئية أن البروتينات الوقائية التي تعمل عادةً على نزع سمّية نواتج الدهون الضارة كانت منخفضة، بينما ارتفعت البروتينات التي تعزز هذه العملية المدمرة. عكس سيبروفول هذه التغيرات إلى حد كبير: تراجعت مستويات الحديد وتلف الدهون، وتحول توازن البروتينات الرئيسية نحو الحماية، وحافظت المتقدرات على أشكال وبنية داخلية أقرب إلى الطبيعية.
حساس طاقة خلوي يعمل كمفتاح تحكم
تحرى البحث بعد ذلك كيف يحقق سيبروفول هذه التأثيرات الوقائية. تركز الاهتمام على AMPK، وهو بروتين يعمل كحساس لطاقة الخلية ومستجيب للإجهاد. في أدمغة الفئران المصابة غير المعالجة، كانت فعالية AMPK منخفضة. زاد سيبروفول من الشكل المنشط من AMPK، بالتوازي مع الانخفاضات في أضرار الفيروبتوز. لاختبار ما إذا كان هذا الحساس الطاقي يقع فعلاً في موقع أعلى من سلسلة الأحداث الوقائية، استخدم الباحثون دواءً آخر، المركب C، الذي يثبط AMPK. عندما تلقت الحيوانات كلّاً من سيبروفول ومثبط AMPK هذا، فقدت فوائد سيبروفول جزئياً: عادت علامات الفيروبتوز لتقترب من المستويات الضارة، وتراكم الحديد عاد، وإشارة نشاط AMPK هبطت إلى ما دون مستوياتها في حيوانات السكتة غير المعالجة. يدعم هذا النمط فكرة أن تفعيل AMPK هو خطوة مفتاحية في كيفية حماية سيبروفول للخلايا العصبية.
تهدئة العاصفة الالتهابية في الدماغ
الإصابة المرتبطة بالسكتة ليست مجرد مسألة موت داخل الخلايا العصبية؛ فاستجابة الجهاز المناعي في الدماغ تلعب أيضاً دوراً رئيسياً. قاس الفريق عدة جزيئات مرسلة التهابية ترتفع عادة بعد نقص التروية–إعادة التروية. في الحيوانات غير المعالجة، كانت هذه الإشارات مرتفعة بشدة، مما يعكس رد فعل التهابي مكثف. قلّل سيبروفول من ثلاثة علامات التهابية رئيسية مقاسة، مما يوحي بأنه لا يقمع فقط تلف الأغشية المدفوع بالحديد بل يخفف أيضاً العاصفة الالتهابية التي تلي ذلك. عندما حُجب AMPK بالمركب C، ضعفت هذه التأثيرات المهدئة على الالتهاب، ما يربط مجدداً فوائد سيبروفول بهذا المسار المركزي لحسّ الطاقة.
ماذا قد يعني هذا للرعاية المستقبلية
تجمع النتائج معاً لتشير إلى أن سيبروفول أكثر من مجرد مهدئ: في نموذج الفئران هذا، يبدو أنه يحدّ من تلف الدماغ المرتبط بالسكتة عن طريق تفعيل AMPK، والذي بدوره يكبح موت الخلايا المدفوع بالحديد ويخفف الالتهاب. ونظراً لأن سيبروفول يُستخدم حالياً في العيادات للتخدير والتهدئة أثناء الإجراءات، فإن إمكاناته الإضافية كعامل واقٍ للدماغ تثير الاهتمام بشكل خاص. ومع ذلك، لدى العمل قيود مهمة، بما في ذلك الاعتماد على نموذج حيواني واحد وإمكانية أن يكون لمثبط AMPK آثار جانبية خاصة به. ستكون هناك حاجة إلى مزيد من الدراسات، بما في ذلك في أنواع حيوانية أخرى وفي نهاية المطاف في مرضى البشر، لتأكيد ما إذا كان سيبروفول يمكن أن يساعد بأمان في حماية الدماغ أثناء وبعد علاج السكتة.
الاستشهاد: Zeng, H., Yu, X., Zheng, Z. et al. Ciprofol attenuates cerebral Ischemia‒reperfusion injury in rats by inhibiting ferroptosis through upregulating AMPK. Sci Rep 16, 9282 (2026). https://doi.org/10.1038/s41598-026-40104-6
الكلمات المفتاحية: السكتة الإقفارية, إصابة إعادة التروية, سيبروفول, الفيروبتوز, الحماية العصبية