Clear Sky Science · ar
ديناميكيات الأكتين بوساطة كالديزمون‑1 ضرورية للتمايز العظمي لخلايا المُتَبَطِّن الصِمَامي الأورطي
لماذا يهم تصلب صمامات القلب
مع تقدم العمر، قد يصبح أحد الممرات الرئيسية للقلب — الصمام الأورطي — جامدًا وصلبًا تدريجيًا. هذه الحالة، المسماة تضيق الأورطي، تجبر القلب على الضخ بقوة أكبر وقد تؤدي إلى فشل القلب. اليوم، العلاجات الموثوقة الوحيدة هي استبدال الصمام جراحيًا أو عن طريق القسطرة. يطرح الملخص البحثي هنا سؤالًا أساسيًا لكنه حاسم: ما الذي يجعل نسيج الصمام المرن واللطيف يتحول تدريجيًا إلى مادة تشبه العظم؟ من خلال الكشف عن لاعب جزيئي رئيسي في هذه العملية، تشير الدراسة إلى أدوية مستقبلية قد تبطئ أو تمنع تكلس الصمام بدلًا من الاكتفاء باستبدال الصمام المتضرر.
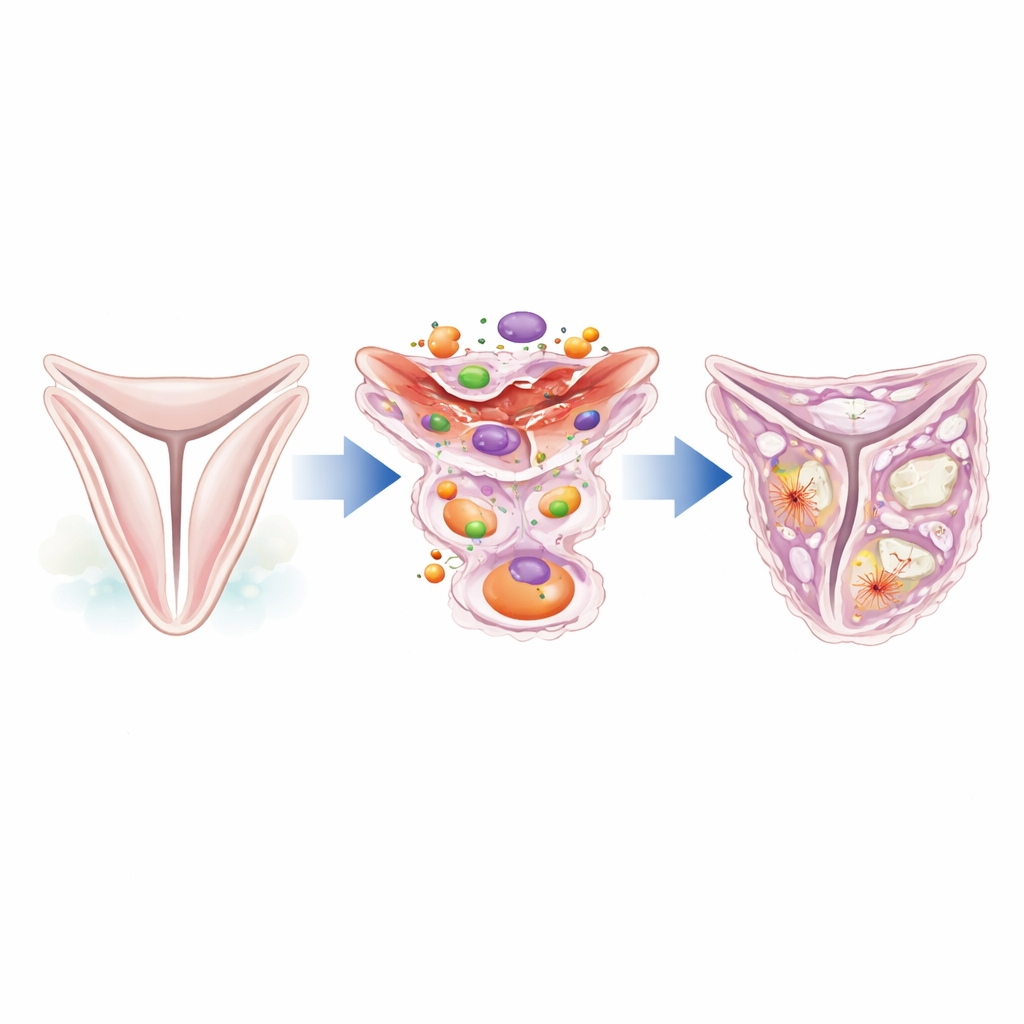
نظرة أقرب على العاملين الخفيين في الصمام
تُدعم شفرات الصمام الأورطي بطبقة رقيقة من الخلايا المتخصصة المسمّاة خلايا المتباطن الصِمَامي. في الصمام السليم، تبقى هذه الخلايا في حالة سكينة وتساعد على الحفاظ على بنية النسيج. لكن تحت الضغط أو عند التعرض للإيذاء، يمكن أن تغير هويتها وتبدأ في التصرف مثل خلايا مكوّنة للندبات أو حتى خلايا مكوّنة للعظم. ركز الباحثون على بروتين يُدعى كالديزمون‑1، الذي يساعد في التحكم في السقالة الداخلية للخلايا المصنوعة من خيوط الأكتين. من خلال تحليل بيانات تسلسل الحمض النووي الريبي أحادي الخلية المتاحة من صمامات بشرية، وجدوا أن مستوى كالديزمون‑1 يرتفع بشدة في صمامات مرضى التضيق الأورطي مقارنة بالصمامات الطبيعية، لا سيما في الخلايا المتباطنة الموجودة في المناطق السميكة والمتليفّة.
من نسيج مرن إلى رقع ليفية وتشبه عظم
أظهرت دراسات المجهر على عينات صمام بشرية أن بروتين كالديزمون‑1 موجود بوفرة في الشفرات المريضة ويتواكب مع علامات الخلايا المنشطة القابضة والخلايا الشبيهة بالفيبروبلاست التي تصنع الكولاجين. تتجمع هذه الخلايا الغنية بكالديزمون‑1 حول مناطق التليف والبداية المبكرة للتكلس، مما يوحي بأنها تساهم في بناء المصفوفة الزائدة التي تثخن الصمام. أظهر التحليل الإضافي أن هذه الخلايا تعبر عن جينات نموذجية لأنواع خلوية شبيهة بالعضلات الملساء ومهيأة لتكوين العظم، وأنها منتجة رئيسية لبروتينات هيكلية مثل كولاجين النوع الأول. بعبارة أخرى، أينما كان الصمام يتصلب ويتليف، توجد خلايا متباطنة موجبة لكالديزمون‑1 في الموقع.
كيف يدفع بروتين يتحكم بالشكل الخلايا نحو تكوين العظم
لفهم السببية، عزل الفريق خلايا المتباطن الصِمَامي البشرية واستخدموا حمض نووي ريبوزي صغير متداخل لإخماد كالديزمون‑1. بدون هذا البروتين، فقدت الخلايا شكلها المستطيل المغزلي وأصبحت أكثر استدارة. رقت خيوط الأكتين الداخلية لديها، وتراجعت قدرتها على الانقسام والتحرك باتجاه محدد. عندما عرّض الباحثون هذه الخلايا وسطًا مزروعًا محفزًا للعظام، كوّنت الخلايا الطبيعية رواسب كالسيوم بسهولة، لكن الخلايا المنخفضة كالديزمون‑1 أظهرت تراكمًا معدنيًا أقل بكثير. وأكد تسلسل الحمض النووي الريبي على نطاق واسع أن العديد من الجينات المشاركة في تكوين العظم وإعادة تشكيل النسيج، بما في ذلك محركات تمايز عظمية معروفة مثل RUNX2 والفوسفاتاز القلوية، أُنشطت بشدة تحت ظروف تحفيز العظم لكنها فشلت في الارتفاع عند قمع كالديزمون‑1.
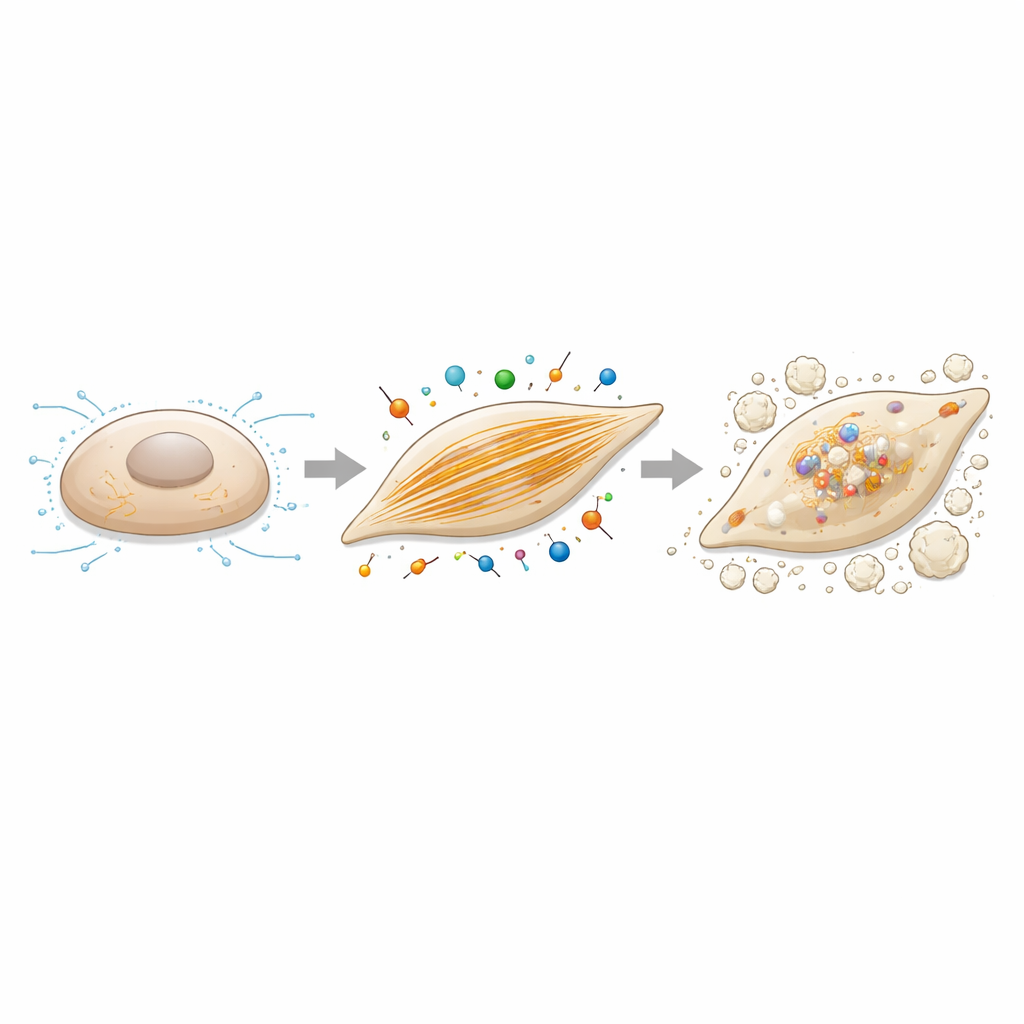
خيوط الأكتين كرَافعة تحكم في التكلس
بما أن كالديزمون‑1 منظم للأكتين، تساءل المؤلفون بعد ذلك عما إذا كانت تغييرات تركيب الأكتين نفسها ستغير ميل الخلايا للتكلس. عالجوا خلايا المتباطن الصِمَامي بمادة سيكتوكيلازين B، مركب يعيق نمو خيوط الأكتين بلطف، أثناء تطبيق نفس ظروف الزرع المحفزة للعظم. عند جرعات لم تضر بقاء الخلايا بشكل كبير، خفض هذا العلاج بشدة ترسبات الكالسيوم وقلل من تعبير الجينات المرتبطة التَحَجُّر، بما في ذلك كالديزمون‑1 وRUNX2. إلى جانب تجارب الإخماد، ترسم هذه النتائج صورة متسقة: شبكات خيوط الأكتين القوية والقوى الانقباضية التي تدعمها ليست مجرد مراقبٍ سلبي — بل تدفع بنشاط التحول من خلايا داعمة هادئة إلى خلايا مكوّنة للعظم في الصمام.
ما الذي يعنيه هذا للعلاجات المستقبلية
للواعي من غير المتخصصين، الرسالة الأساسية هي أن تصلب الصمام الأورطي عملية نشطة ومنظمة وليست مجرد «اهتراء واحتكاك». تحدد هذه الدراسة كالديزمون‑1 كمنسق مركزي يربط الهيكل الداخلي للخلية بالبرنامج الجيني لصنع نسيج شبيه بالعظم. من خلال مساعدة خلايا المتباطن الصِمَامي على اعتماد هوية قابضة وليفية وفي النهاية عظمية، يساهم كالديزمون‑1 مباشرة في تراكم الرواسب الصلبة التي تضيق الصمام. وعلى الرغم من أن أي علاج يستهدف هذا البروتين أو ديناميكيات الأكتين سيحتاج إلى اختبار دقيق لتجنب تأثيرات غير مرغوبة في أنسجة أخرى، فإن المسارات الوسيطة بوساطة كالديزمون‑1 تبرز الآن كمرشحين واعدين لأدوية مصممة لإبطاء أو وقف تكلس الصمام قبل أن يصبح الاستئصال الجراحي ضروريًا.
الاستشهاد: Komoda, M., Sakaue, T., Nakao, Y. et al. Caldesmon-1–mediated actin dynamics is essential for osteogenic differentiation of aortic valve interstitial cells. Sci Rep 16, 9385 (2026). https://doi.org/10.1038/s41598-026-39938-x
الكلمات المفتاحية: تكلس الصمام الأورطي, كالديزمون‑1, خلايا المتباطن الصِمَامي, هيكلية الأكتين الخلوية, التمايز العظمي