Clear Sky Science · ar
تحديد أهداف رئيسية متعددة المستويات لتميُّز الخلايا المكونة للعظام من الخلايا الرافدية النخاعية البشرية تحت الإجهاد التأكسدي
لماذا تهم العظام المجهدة
مع التقدم في العمر أو عند الإصابة بأمراض مزمنة مثل السكري وهشاشة العظام، تفقد عظامنا قدرتها على إصلاح نفسها. المسبب الرئيسي هنا هو «الإجهاد التأكسدي» — تراكم جزيئات تفاعلية تُلحق الضرر بالخلايا. تطرح هذه الدراسة سؤالًا عمليًا ذا دلالة على الكسور وزرع العظام: ما الذي ينهار بالضبط داخل خلايا جذع نخاع العظم البشرية عند تعرضها للإجهاد التأكسدي، وهل يمكننا العثور على مفتاح جزيئي يساعدها على الاستمرار في تكوين عظام جديدة؟
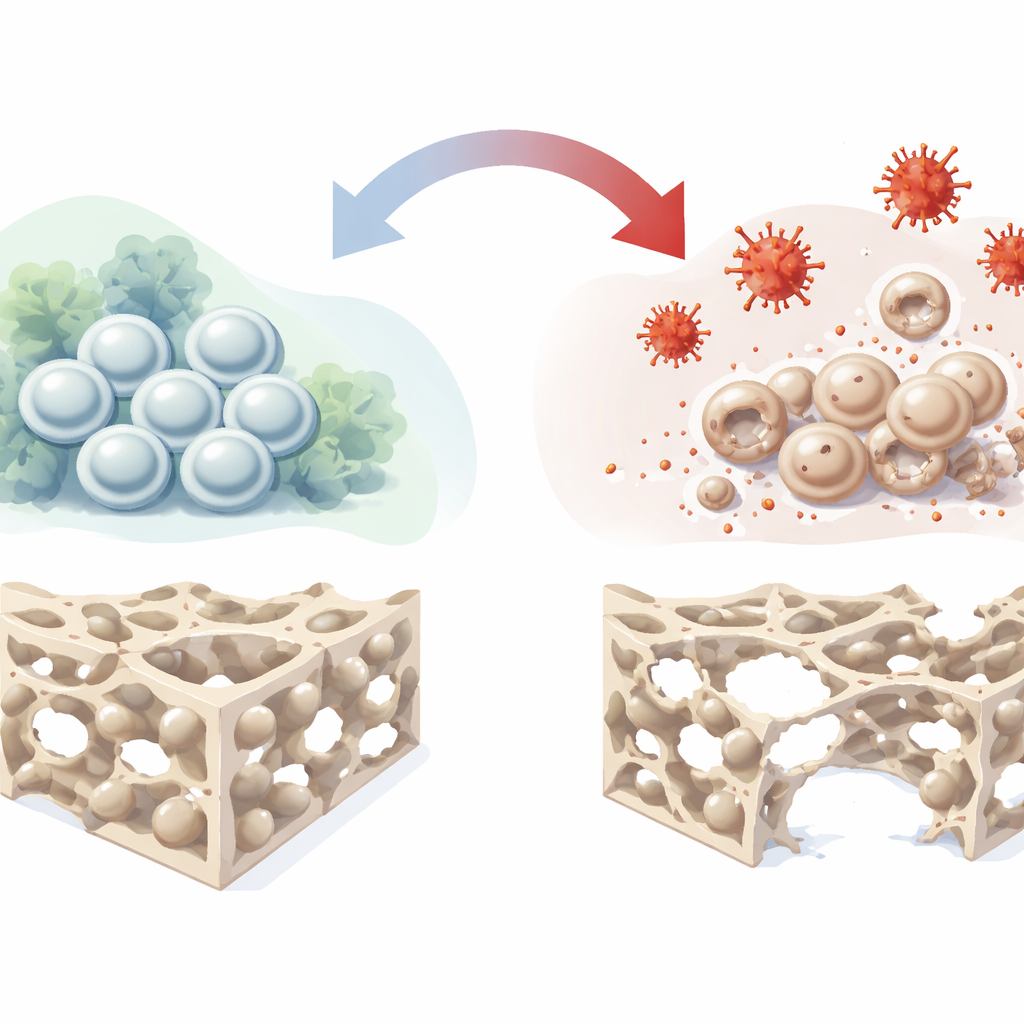
الخلايا الجذعية التي تبني العظم
في أعماق عظامنا تعيش خلايا رافدية نخاعية ميزانشيمية، وهي مجموعة مرنة قادرة على تجديد نفسها والنضوج إلى خلايا مكوِّنة للعظم وخلايا غضروف وخلايا دهنية. وبما أنها تساعد طبيعيًا في ترميم الأنسجة المتضررة، فهي مرشح رئيسي لعلاجات الجيل القادم لإصلاح عيوب العظام ونخر العظم. ومع ذلك، في المرضى الفعليين غالبًا ما توجد هذه الخلايا في بيئات معادية تتسم بسوء التروية، وانخفاض الأكسجين، والالتهاب، والإجهاد التأكسدي. في مثل هذه الظروف تتراجع قدرتها على التحول إلى خلايا عظمية، مما يحد من نجاح العلاجات القائمة على الخلايا الجذعية. سعى المؤلفون لإعادة خلق هذا البيئة المعادية في المختبر ورسم خريطة تفصيلية لكيفية تعطّل تكون العظم.
إعادة خلق بيئة قاسية في المختبر
استخدم الباحثون بيروكسيد الهيدروجين، مصدر شائع للجزيئات الأكسجينية التفاعلية، لفرض الإجهاد التأكسدي على خلايا نخاع العظم البشرية المزروعة في المختبر. قاموا بتدرج الجرعة بعناية للعثور على نطاق يجهد الخلايا دون قتلها. عند 400 ميكرو مولار أو أقل، حافظت الخلايا على شكلها المغزلي الطبيعي وبقت حية، على الرغم من أن كيميائها الداخلية تغيرت بوضوح: ارتفعت مستويات الأكسجين التفاعلي، وبدأت وظيفة الميتوكوندريا بالتغير، وتحولت الموازنة بين البروتينات المرتبطة بالبقاء والموت باتجاه التكيّف مع الإجهاد. عند جرعات أعلى، فقدت الخلايا شكلها وماتت بأعداد كبيرة. باستخدام الجرعة المتحملة جيدًا 400 ميكرو مولار، حفز الفريق الخلايا لاحقًا على تكوين عظم وراقب ما حدث.
كيف يعيق الإجهاد بناء العظم
تحت الإجهاد التأكسدي، انخفضت قدرة الخلايا الجذعية على التحول إلى خلايا عظمية في عدة اختبارات متمِّمة. انخفض النشاط العظمي المبكر، المتتبَّع بواسطة إنزيم الفوسفاتاز القلوي، مع ازدياد الإجهاد. لاحقًا، عندما كان من المفترض أن تودع الخلايا رواسب معدنية، أظهرت أطباق الزرع عُقيدات كالسيوم أقل وكثافة أضعف. كما تقلص تعبير جينات وبروتينات مرتبطة بالعظم مثل RUNX2 والأوستيوبيونتين. لفحص الآليات، جمع العلماء طريقتين قويتين من التحليل «أومكس»: تسلسل الرنا لرصد الجينات النشطة والأقل نشاطًا، وتحليل بروتيني واسع النطاق لرؤية البروتينات التي تغيّرت كميًا. كشفت هذه المجموعات من البيانات عن مئات التغيرات في ضوابط دورة الخلية، وسلوك الكروموسومات، والتمثيل الغذائي، وتنظيم الهيكل الخلوي المحيط بالخلايا، مجسدة صورة خلايا جذعية اختلت توقيتها الداخلي ودعمها البنيوي بسبب الإجهاد التأكسدي.
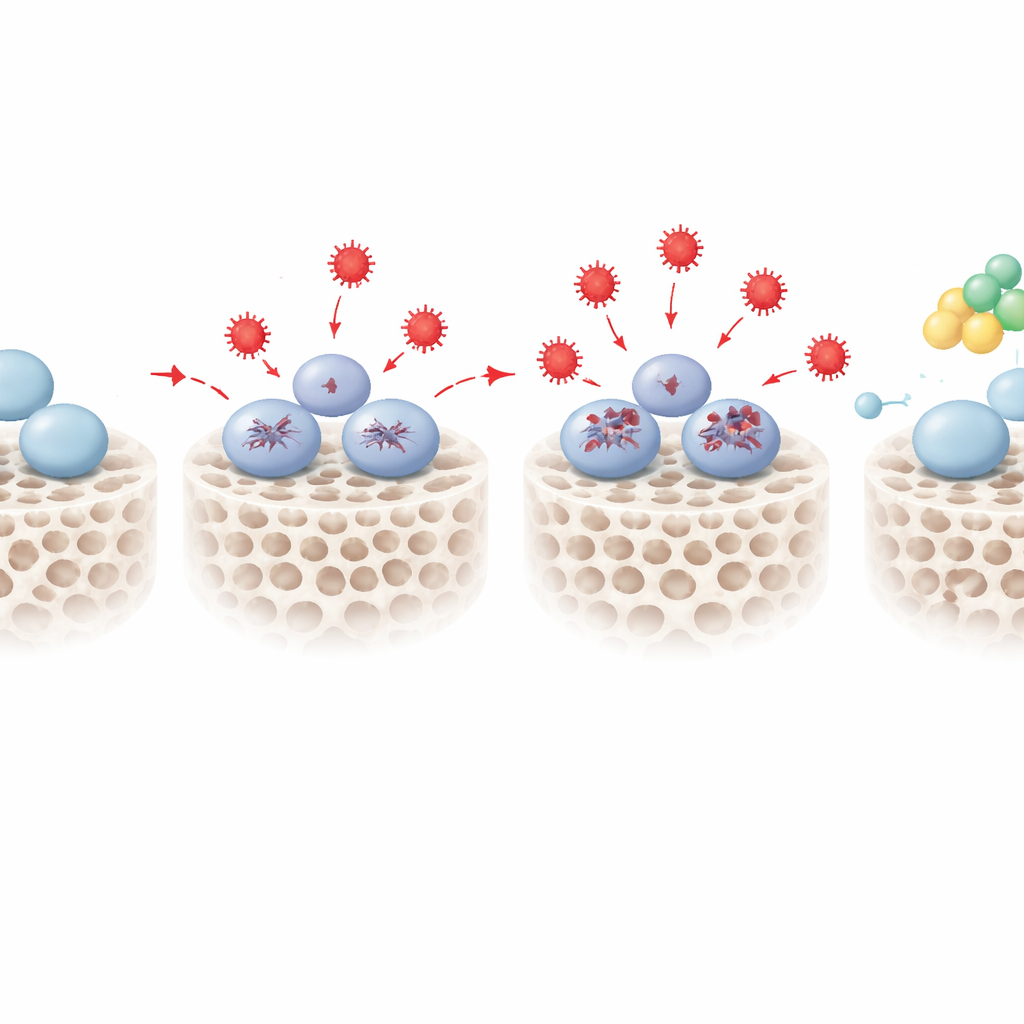
العثور على مفتاح وقائي يُدعى PENK
من خلال تراكب خرائط الرنا والبروتين، ضيق الفريق نطاق البحث إلى 18 جزيئًا تغيّروا باستمرار في الخلايا المجهدة وكانوا مرتبطين بكل من استجابات الإجهاد وتكوين العظم. برز جزيء واحد: البروجِنينكِفالين أو PENK، المعروف كمقدمة لببتيدات أفيونية طبيعية. تحت الإجهاد التأكسدي ارتفعت مستويات PENK بشكل يتناسب مع الجرعة. عندما قلل العلماء من مستوى PENK جينيًا، ازدادت صعوبة الخلايا الجذعية المجهدة في تكوين العظم، إذ أظهرت نشاطًا إنزيميًا مبكرًا أضعف وترسبًا معدنيًا أقل. وعندما عززوا مستوى PENK حصل العكس: حتى تحت نفس ظروف الإجهاد التأكسدي، استعادت الخلايا جزءًا كبيرًا من قدرتها على بناء مصفوفة عظمية متكلسة. أشارت تحليلات مسارات إضافية إلى أن PENK قد يعمل عن طريق ضبط مسارات أيضية معينة، بما في ذلك أيض السفنغوليبيدات، التي تربط توازن الأكسدة/الاختزال بقرارات الخلايا الجذعية حول الحفاظ على إمكاناتها أو التوجُّه نحو مصير عظمي.
ما يعنيه هذا لإصلاح العظام في المستقبل
تُظهر هذه الدراسة أن الإجهاد التأكسدي بمفرده يكفي لتعطيل قدرة خلايا نخاع العظم البشرية على تكوين العظم، وتحدد PENK كعامل وقائي داخلي يساعدها على مقاومة هذا الأذى. للقراء غير المتخصصين، الرسالة واضحة: نجاح علاجات العظام المعتمدة على الخلايا الجذعية لن يعتمد فقط على الخلايا ذاتها، بل أيضًا على البيئات المجهدة التي توضع فيها والمفاتيح الجزيئية التي تساعدها على التكيّف. من خلال إبراز PENK كهدف واعد، تشير الدراسة إلى احتمالات عقاقير أو طرق جينية مستقبلية يمكنها تدعيم إصلاح العظام لدى المرضى الذين تنغمس أنسجتهم في الإجهاد التأكسدي، من كبار السن إلى المصابين بأمراض أيضية أو التهابية مزمنة.
الاستشهاد: Dong, W., Zheng, Y., Zhou, Y. et al. Multi-omics identification of key targets for the osteogenic differentiation of human bone marrow mesenchymal stromal cells under oxidative stress. Sci Rep 16, 8215 (2026). https://doi.org/10.1038/s41598-026-39818-4
الكلمات المفتاحية: تجدد العظام, الإجهاد التأكسدي, الخلايا الجذعية الميزانشيمية, التميُّز العظمي, PENK