Clear Sky Science · ar
الفعالية المضادة للبكتيريا لمتشعبات بولي-أميدوأمين الجيل الرابع المحمّلة بالأموكسيسيلين في مكافحة المكورات العنقودية الذهبية المقاومة للميثيسيلين
لماذا تهم هذه الجسيمات الصغيرة
تعدّ الإصابات المقاومة للأدوية واحدة من أكبر التهديدات للطب الحديث، ما يجعل الأمراض التي كانت روتينية في السابق أصعب وأكثر خطورة في العلاج. ومن بين أسوأ المسببات المكورات العنقودية الذهبية المقاومة للميثيسيلين (MRSA)، وهي بكتيريا يمكن أن تحوّل التهابات الجلد البسيطة أو الإجراءات الطبية إلى حالات تهدّد الحياة. تستكشف هذه الدراسة طريقة ذكية لإعادة فعالية مضاد حيوي يومي، الأموكسيسيلين، عبر تغليفه داخل ناقلات نانوية مصممة خصيصًا تُدعى المتشعبات. وتشير النتائج إلى أن التعبئة الذكية للأدوية قد تعيد الحياة إلى مضادات حيوية قديمة ضد بعض الجراثيم الأكثر عنادًا لدينا. 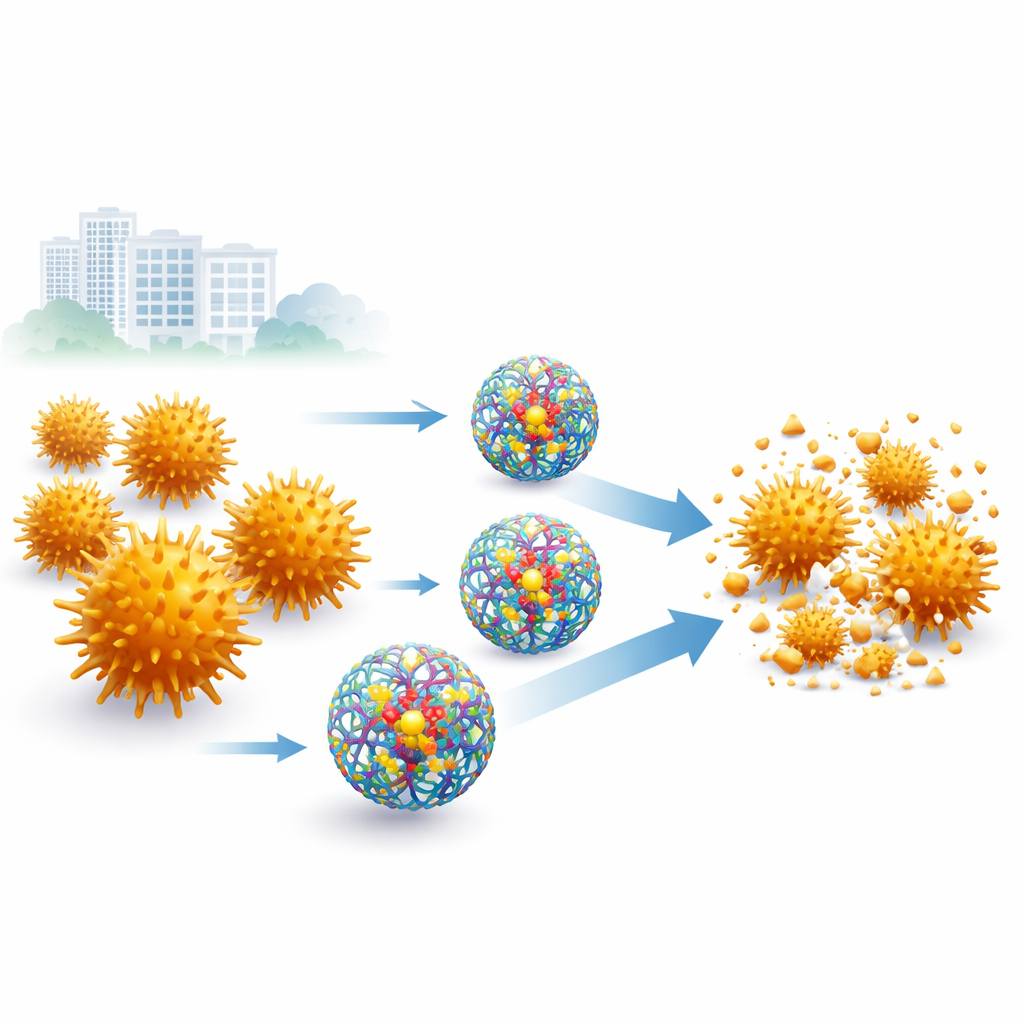
جرثوم عنيد لا يختفي
MRSA هو شكل من أشكال المكورات العنقودية الذهبية تطوّر قدرة على التحمل ضد العديد من المضادات الحيوية الشائعة الاستخدام، بما في ذلك مجموعة البيتا-لاكتام التي ينتمي إليها الأموكسيسيلين. يسبب طيفًا من الأمراض، من التهابات الجلد والأنسجة الرخوة إلى التهابات العظام والقلب والمرتبطة بالأجهزة الطبية، ويرتبط بمعدلات عالية من المضاعفات والوفاة، خاصة لدى كبار السن. تعود نجاحات MRSA إلى مقاومته الجينية للأدوية وكذلك قدرته على إنتاج سموم وبناء طبقات واقية لزجة تُسمى الأغشية الحيوية، التي تحمي تجمعات البكتيريا وتجعلها أصعب في القتل بمعدل يصل إلى ألف مرة. وبما أن تطوير مضادات حيوية جديدة بطيء ومكلف، يبحث الباحثون عن طرق أكثر ذكاءً لتوصيل الأدوية الموجودة بفعالية أكبر.
ناقلة توصيل بحجم نانوي
ركز الفريق على المتشعبات، وهي جزيئات متفرعة شبيهة بالأشجار يمكن هندستها على المستوى النانوي. استخدموا متشعب بولي-أميدوأمين من الجيل الرابع (PAMAM G4) قابل للذوبان في الماء ويمكنه حمل جزيئات أخرى في داخله. عبر خلط هذا المتشعب مع الأموكسيسيلين بنسبة واحد إلى واحد، شكّلوا جسيمات نانوية تم احتواء المضاد الحيوي فيها بدلًا من تركه معرضًا. أظهرت الاختبارات المخبرية المفصّلة أن الجسيمات الناتجة كانت بحجم حوالي 219 نانومتر — أصغر بكثير من معظم الخلايا — مع توزيع حجمي موحّد، وشحنة سطحية مستقرة، وكفاءة تحميل دوائي عالية تبلغ حوالي 90%. كشفت المجهر الإلكتروني أن المتشعبات الفارغة والمحمّلة بالمضاد على حدّ سواء شكّلت جسيمات تكاد تكون كروية، مما يؤكد أن التحضير كان منظّمًا جيدًا. 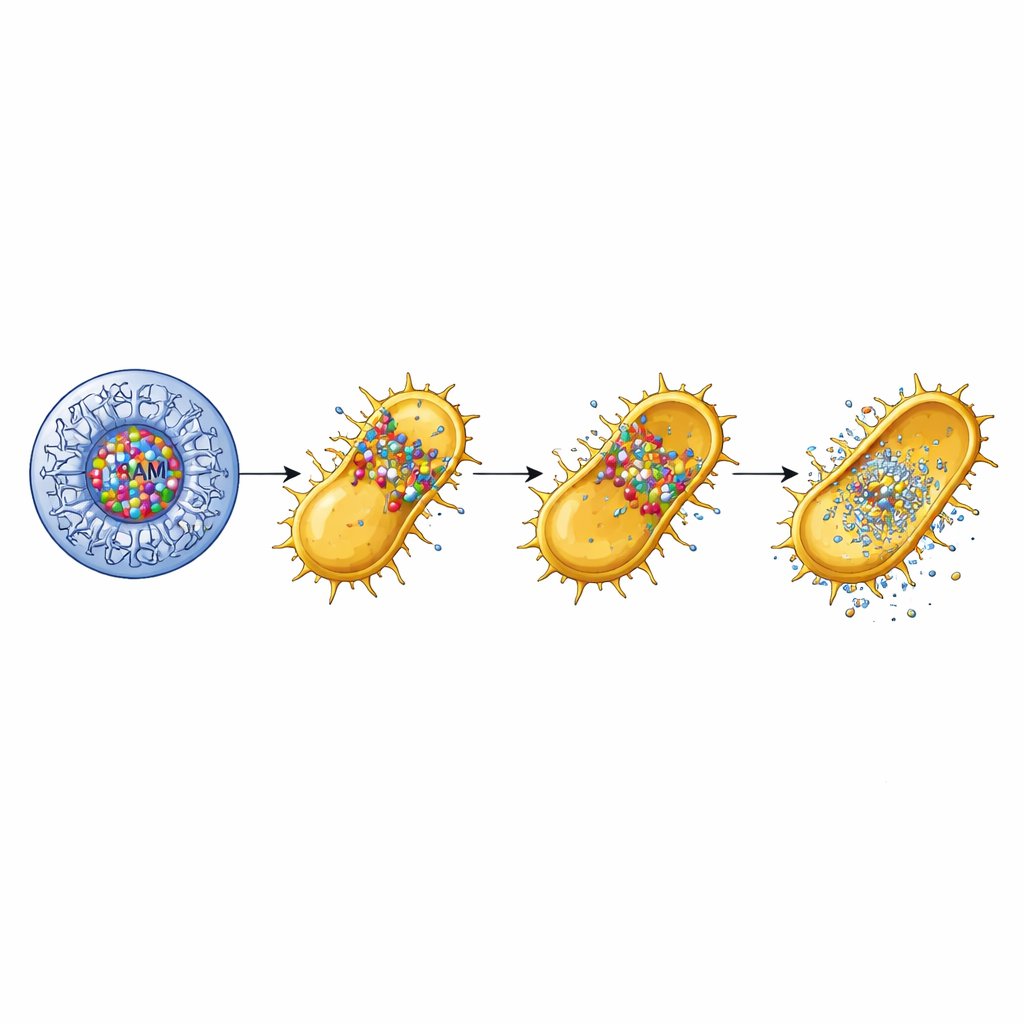
إطلاق بطيء وضربة أقوى
لفهم كيف غيّرت هذه التعبئة سلوك الأموكسيسيلين، درس الباحثون كيفية تسرب الدواء من المتشعبات في محلول ملحي على مدى ثماني ساعات. بالمقارنة مع الأموكسيسيلين الحر، الذي أطلق حوالي ثلث محتواه فقط في تلك الفترة، أطلقت التركيبة القائمة على المتشعب أكثر من 80% بطريقة تدريجية ومطوّلة. وهذا يعني أن المضاد الحيوي يمكن أن يبقى متاحًا لفترة أطول بدلًا من أن يُغسل بسرعة. عندما اختبر الفريق التركيبة ضد MRSA في تجارب النمو، أوقف الأموكسيسيلين المحمّل على المتشعب نمو البكتيريا عند تركيزات منخفضة نسبيًا، بينما بالكاد أبطأ الأموكسيسيلين الحر النمو وكان للمتشعب الفارغ تأثيرات متواضعة فقط. أظهرت اختبارات الأطباق المعيارية التي تقيس مناطق التثبيط الواضحة حيث لا تستطيع البكتيريا النمو، مناطق تثبيط أكبر بكثير للجسيمات النانوية المركبة مقارنة بأي من المكوّنات بمفردها، مما يدل على تعزيز قوي للقوة المضادة للبكتيريا.
تعطيل أسلحة البكتيريا
بعيدًا عن القتل البسيط للبكتيريا، فحص الباحثون ما إذا كانت الجسيمات النانوية قادرة أيضًا على تقليل قُدرة MRSA المرضية — أي قابليته لإحداث الضرر. تنتج MRSA سمومًا تحدث ثقوبًا في خلايا الدم الحمراء، عملية تُسمى التحلّل الدموي، والتي تساعدها على اقتحام الأنسجة والانتشار. وجدت الدراسة أن لا الأموكسيسيلين وحده ولا المتشعب الفارغ استطاعا إيقاف هذا النشاط. مع ذلك، عندما تم احتواء الأموكسيسيلين داخل متشعب G4، تمت منع التحلّل الدموي تمامًا عبر جميع الجرعات المختبرة. كما نظر الفريق في الأغشية الحيوية، وهي تجمعات بكتيرية لزجة تلتصق بالأسطح وتقاوم العلاج. قلّلت جسيمات G4-الأموكسيسيلين من تكوّن الأغشية الحيوية بنحو 70%، مقارنة بنحو 20% فقط للمتشعب الفارغ ولا تأثير يذكر من الأموكسيسيلين الحر. تشير هذه النتائج إلى أن التشكيل النانوي لا يقتصر على قتل MRSA بكفاءة أعلى فحسب، بل يزيل أيضًا أدوات مهمة تستخدمها البكتيريا للبقاء وإلحاق الضرر بالمضيف.
ماذا قد يعني هذا للعلاجات المستقبلية
مجتمعة، تشير النتائج إلى أن تعبئة الأموكسيسيلين داخل متشعبات PAMAM G4 تحوّل دواءً كان إلى حدّ كبير غير فعّال ضد MRSA إلى عامل مضاد للبكتيريا ومضاد للمرضية قوي. توفّر الجسيمات النانوية الدواء بطريقة مطوّلة، وتساعده على الوصول إلى البكتيريا والتأثير فيها بشكل أكثر فعالية، وتقلّل السلوكيات الخطرة مثل إطلاق السموم وتكوّن الأغشية الحيوية. وبينما أُجريت هذه الدراسة في المختبر ولا تزال هناك حاجة لمزيد من الدراسات حول الثبات والجرعات والسلامة في الحيوانات، فإنها تشير إلى استراتيجية واعدة: استخدام ناقلات نانوية ذكية لإعادة تدوير مضادات حيوية مألوفة لمواجهة الإصابات المقاومة للأدوية الحديثة، مما قد يمنحنا وقتًا ثمينًا في الكفاح ضد MRSA والمكروبات الخارقة ذات الصلة.
الاستشهاد: Alenazi, N., Alhabardi, S.A., Binsuwaidan, R. et al. The antibacterial effectiveness of fourth-generation poly-amidoamine dendrimers-loaded with amoxicillin in combating methicillin-resistant Staphylococcus aureus. Sci Rep 16, 9242 (2026). https://doi.org/10.1038/s41598-026-39752-5
الكلمات المفتاحية: MRSA, مقاومة المضادات الحيوية, الجسيمات النانوية, المتشعبات, الأموكسيسيلين