Clear Sky Science · ar
الالتهاب المزمن يعزز تقدم سرطان المعدة عبر قص CX3CL1 بوساطة ADAM10
لماذا يهم التهيج المعدي طويل الأمد
يعيش كثير من الناس لسنوات مع تهيج مزمن في المعدة ناجم عن عدوى أو النظام الغذائي أو مشاكل صحية أخرى. هذا التهيج المستمر ذو المستوى المنخفض، المعروف بالالتهاب المزمن، هو عامل خطر صامت لسرطان المعدة، أحد أكثر السرطانات فتكًا على مستوى العالم. تسأل الدراسة الملخّصة هنا سؤالًا محددًا: كيف يدفع الالتهاب المزمن الأورام المعدية المبكرة إلى النمو السريع والانتشار؟ من خلال تتبع إشارة كيميائية واحدة وإنزيم يفعلها، يكشف الباحثون عن نقطة ضعف محتملة قد تستهدفها العلاجات المستقبلية.
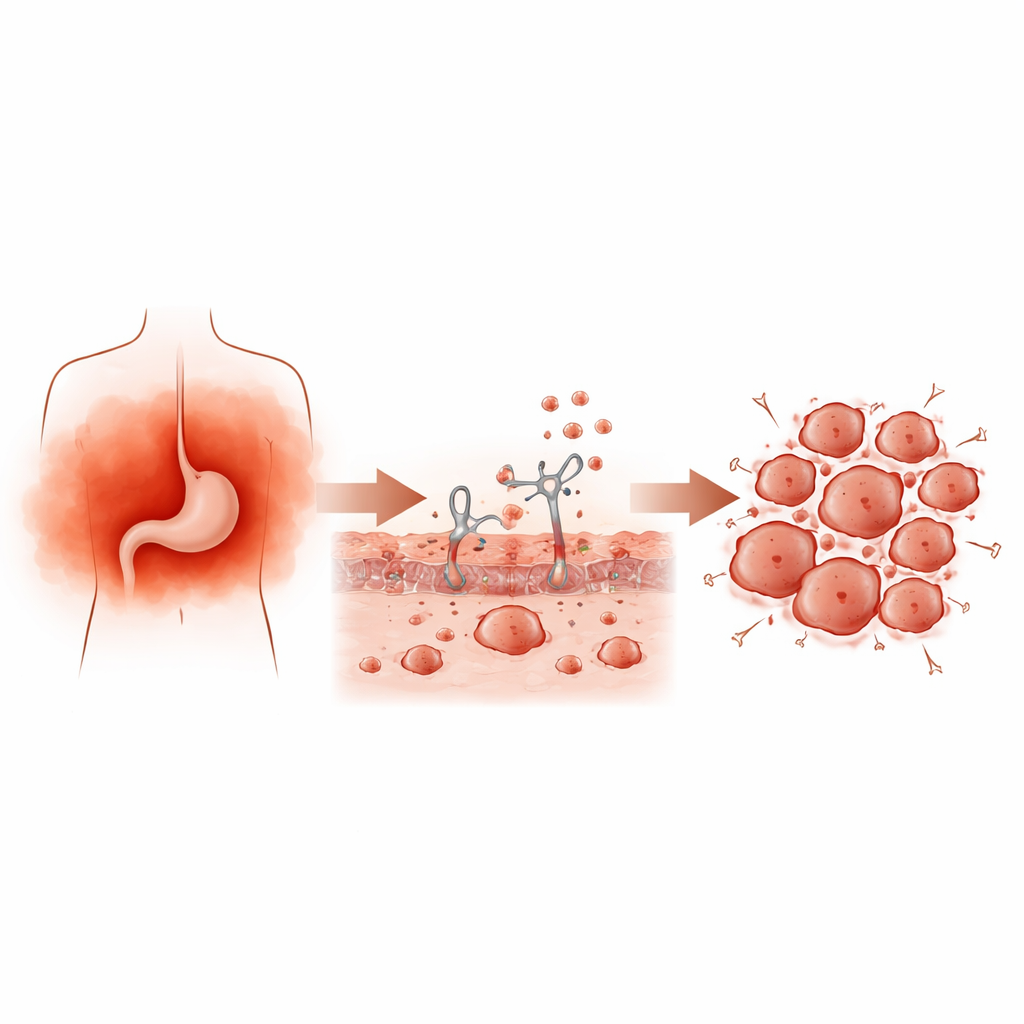
من التهيج إلى أورام أسرع نموًا
لمحاكاة الالتهاب طويل الأمد، عرض الفريق الفئران مرارًا لمواد تثير الاستجابات المناعية، ثم زرعوا خلايا سرطان معدة تحت الجلد. بالمقارنة مع الحيوانات الضابطة، طورت الفئران المصابة بالتهاب مزمن أورامًا أكبر وأثقل مليئة بخلايا منقسمة وتسريبات للخلايا المناعية. في تجارب زراعة الخلايا، جعل مصل الدم المأخوذ من فئران ذات مستويات مختلفة من الالتهاب خلايا سرطان المعدة البشرية تنمو وتشكل مستعمرات بشكل أكثر نشاطًا. توضح هذه النتائج مجتمعة أن الإشارات الالتهابية المتداولة في الجسم يمكن أن تسرّع نمو الورم مباشرة.
البحث عن الإشارة المسببة للمشكلة
كانت الخطوة التالية معرفة أي من جزيئات الرسول الالتهابي هو الأكثر ضررًا. باستخدام مصفوفة بروتينية واسعة، قارن الباحثون العديد من السيتوكينات في أورام الفئران الملتهبة وغير الملتهبة فوجدوا تسعة منها ارتفعت بوضوح. ومن خلال مطابقة بيانات مرضى عامة، ركزوا على مرشح واحد مميز: CX3CL1، وهي كيموكين تساعد في توجيه الخلايا المناعية. كانت مستويات CX3CL1 أعلى في أورام المعدة مقارنةً بالنسيج المعدي الطبيعي، وارتفعت بشكل خاص في الأورام المتقدمة، وكانت مرتبطة ببقاء أقل لدى المرضى. أكدت القياسات في أورام الفئران أن الالتهاب المزمن رفع مستويات CX3CL1 موضعيًا، مما يوحي بأن هذه الإشارة الواحدة قد تفسر جزئيًا الصلة بين الالتهاب ونتائج أسوأ.
أي الخلايا ترسل وتتلقى الإشارة؟
باستخدام تسلسل الرنا أحادي الخلية، رسم الباحثون خارطة نشاط الجينات خلية بخلية داخل الأورام. اكتشفوا أن CX3CL1 يُنتج بشكل أساسي بواسطة خلايا السرطان نفسها بدلاً من الخلايا المناعية أو الداعمة المحيطة. وُجد مستقبلها المشارك، CX3CR1، على عدة أنواع خلوية، لكن تحت الالتهاب المزمن أصبح أكثر بروزًا على خلايا الورم. توسع عدد فرعي محدد من الخلايا السرطانية في الأورام الملتهبة وأظهر تعبيرًا عاليًا لـ CX3CL1 وعلامات رفع إنتاج البروتين والنمو. في الاختبارات المخبرية، أدى إضافة CX3CL1 المنقى مباشرة إلى خلايا سرطان المعدة إلى زيادة بقائها وتكوين المستعمرات وحركتها. أضعف إيقاف CX3CR1 هذه التأثيرات، مما يشير إلى أن خلايا السرطان كانت ترسل وتستجيب لهذه الإشارة المحفزة للنمو.
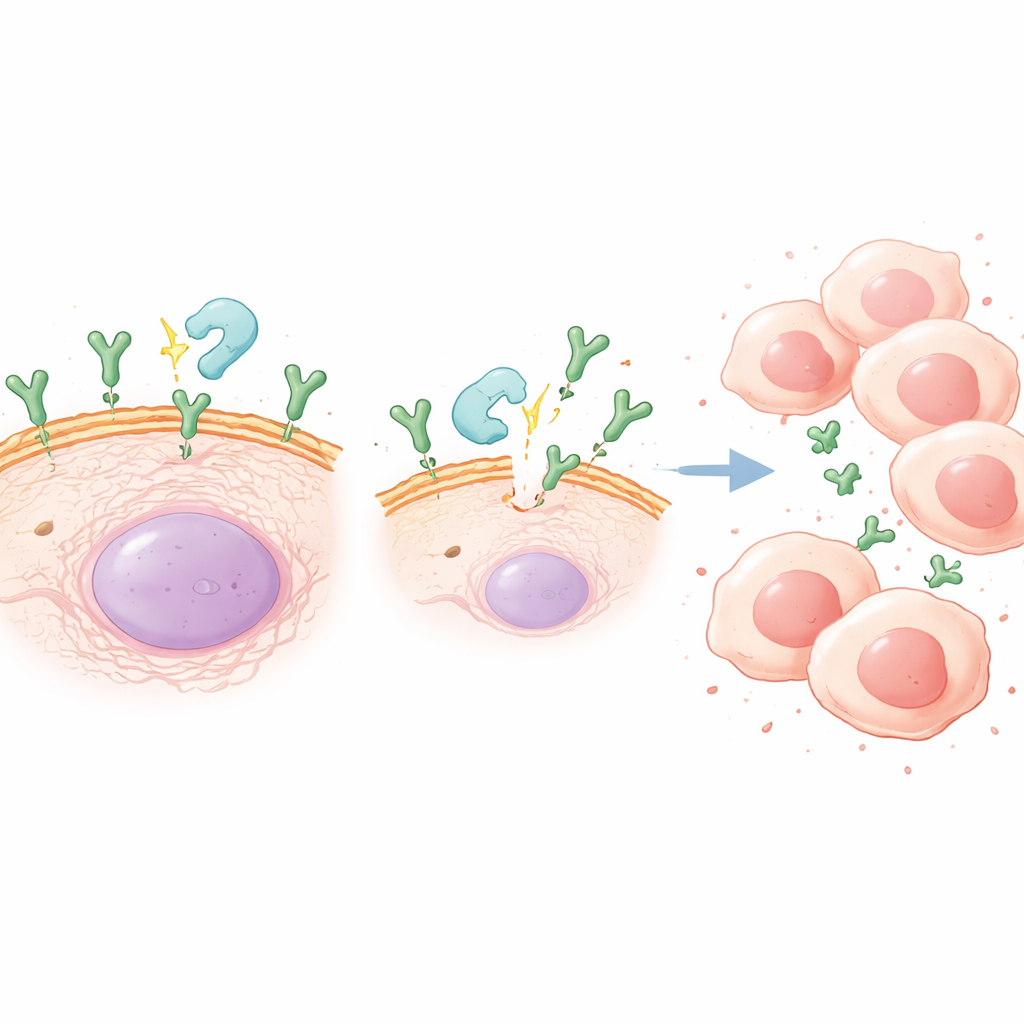
الإنزيم الذي يفاقم الخطر
يوجد CX3CL1 بشكل مرتبط بغشاء الخلية وبشكل ذائب يمكنه الانتشار في النسيج. يتكوّن الشكل الذائب عندما يقطع إنزيم يدعى ADAM10 النسخة المربوطة بالغشاء. وجدت الدراسة أن الالتهاب المزمن رفع مستويات ADAM10 في أورام الفئران وفي خلايا سرطان المعدة المعرضة لمحفز التهابي في المختبر. عندما عالج الباحثون الخلايا بمثبط لـ ADAM10، انخفضت كمية CX3CL1 الذائب في السائل المحيط، وانعكست الزيادات المرتبطة بالالتهاب في نمو الخلايا السرطانية وحركتها إلى حد كبير. في الفئران المصابة بالالتهاب المزمن، أبطأ حجب ADAM10 تقدم الورم وخفض مستويات CX3CL1 في الأورام، مما يعزز الفكرة أن خطوة «القص» التي يؤديها هذا الإنزيم حاسمة.
ماذا يعني هذا لمرضى مشاكل المعدة المزمنة
تجسم هذه الدراسة سلسلة بسيطة من الأحداث: يشغّل الالتهاب المستمر داخل وحول المعدة ADAM10 في خلايا سرطان المعدة؛ ثم يقوم ADAM10 بقطع المزيد من CX3CL1 إلى صورته الذائبة، والتي بدورها تعود لتؤثر على خلايا السرطان فتساعدها على التكاثر والهجرة. للمختصر، يشبه ذلك بيئة متهيجة تعلم الخلايا السرطانية أن تصرخ وتستمع إلى رسالة تدفعها للنمو. وبما أن كلًا من ADAM10 وCX3CL1 جزيئتان يمكن التعرف عليهما ويثيران اهتمام تطوير الأدوية، فإن محور ADAM10/CX3CL1 الموصوف هنا يقدم هدفًا ملموسًا للعلاجات التي تهدف إلى إبطاء أو منع تقدم سرطان المعدة المدفوع بالالتهاب.
الاستشهاد: Song, Z., Liu, Y., Wang, Z. et al. Chronic inflammation promotes gastric cancer progression via ADAM10-mediated cleavage of CX3CL1. Sci Rep 16, 9169 (2026). https://doi.org/10.1038/s41598-026-39743-6
الكلمات المفتاحية: سرطان المعدة, الالتهاب المزمن, الكيموكينات, البيئة الدقيقة للورم, ADAM10