Clear Sky Science · ar
التعرّض للكادميوم يسبب تليف الكلى عن طريق تثبيط مسار الإشارة hsa_circ_0075684/miR-363-3p/KLF4
لماذا تهديد معدني خفي مهم
الكادميوم معدن سام يتسلل بهدوء إلى حياتنا عبر الغذاء ودخان السجائر والتلوث الصناعي. بمجرد دخوله الجسم يبقى لعقود، ولديه قدرة خاصة على التراكم في الكليتين. تتعمق هذه الدراسة في كيفية تسبب التعرض طويل الأمد للكادميوم في ندب أنسجة الكلى وتحدّد دائرة جزيئية صغيرة قد تكشف الخطر مبكراً — مما يفتح أملًا في الوقاية من مرض الكلى المزمن بدلاً من علاجه في مرحلة متأخرة.
التلف البطيء للكلى
تعمل الكليتان كمرشحات للجسم، فتزيل الفضلات من الدم. لكن الكادميوم يتراكم في هذه المرشحات على مدى سنوات عديدة ويرتبط بقوة بمرض الكلى المزمن. يشير المؤلفون إلى أن حالات مرض الكلى المزمن تتزايد عالمياً، ولا توجد طريقة فعالة لإزالة الكادميوم بمجرد تثبته في الكليتين. بدلاً من التركيز على التنظيف، يجادلون بضرورة إيجاد طرق لاكتشاف الإضرار وقطعها مبكراً — لا سيما عملية التليف، حيث تُستبدل الأنسجة الصحية تدريجياً بأنسجة ندبية صلبة تعطل وظيفة الكلية.
رسائل RNA الصغيرة ومفتاح الحماية
ركّز الباحثون على جزيء تنظيمي صغير يُسمى miR-363-3p، وهو جزء من عائلة شظايا RNA القصيرة التي تضبط نشاط الجينات. أظهرت أعمالهم السابقة ارتفاع هذا الـ RNA في عمال المصانع الذين يعانون من تسمم طويل الأمد بالكادميوم. باستخدام قواعد بيانات جينية عامة واسعة، بحثوا عن دائرة تنظيمية أوسع حول miR-363-3p في نسيج الكلى المعرض للكادميوم. حدّدوا مسارًا ثلاثيًا: RNA دائري (hsa_circ_0075684) يمكنه «امتصاص» miR-363-3p، وجزيء miR-363-3p نفسه، وبروتين يسمى KLF4 يساعد في حماية خلايا الكلية من التليف. يبدو أن هذا الثلاثي يعمل كمفتاح جزيئي يحافظ على ضبط التليف.
من خلايا في طبق إلى فئران في المختبر
لاختبار هذه الفكرة، عرض الفريق خلايا أنابيب كلية بشرية لجرعات متزايدة من الكادميوم. مع ارتفاع مستويات الكادميوم، أظهرت الخلايا علامات كلاسيكية للتليف: ارتفعت البروتينات المرتبطة بالندب، بينما انخفض بروتين يساعد الخلايا على الالتصاق والحفاظ على البنية الطبيعية. في الوقت نفسه ارتفعت مستويات miR-363-3p، بينما انخفض كل من KLF4 والـ RNA الدائري. أظهرت التجارب الجينية أن miR-363-3p يرتبط مباشرةً بـ KLF4 ويخفض إنتاجه، وأن الـ RNA الدائري عادةً ما يقيّد miR-363-3p ويمنعه من كتم KLF4. عندما عزّز العلماء miR-363-3p، ارتفعت بروتينات التليف وهبط KLF4؛ وعندما حجبوا miR-363-3p أو زادوا مستوى الـ RNA الدائري، تعافى KLF4 وتراجعت مؤشرات التليف، حتى بوجود الكادميوم.
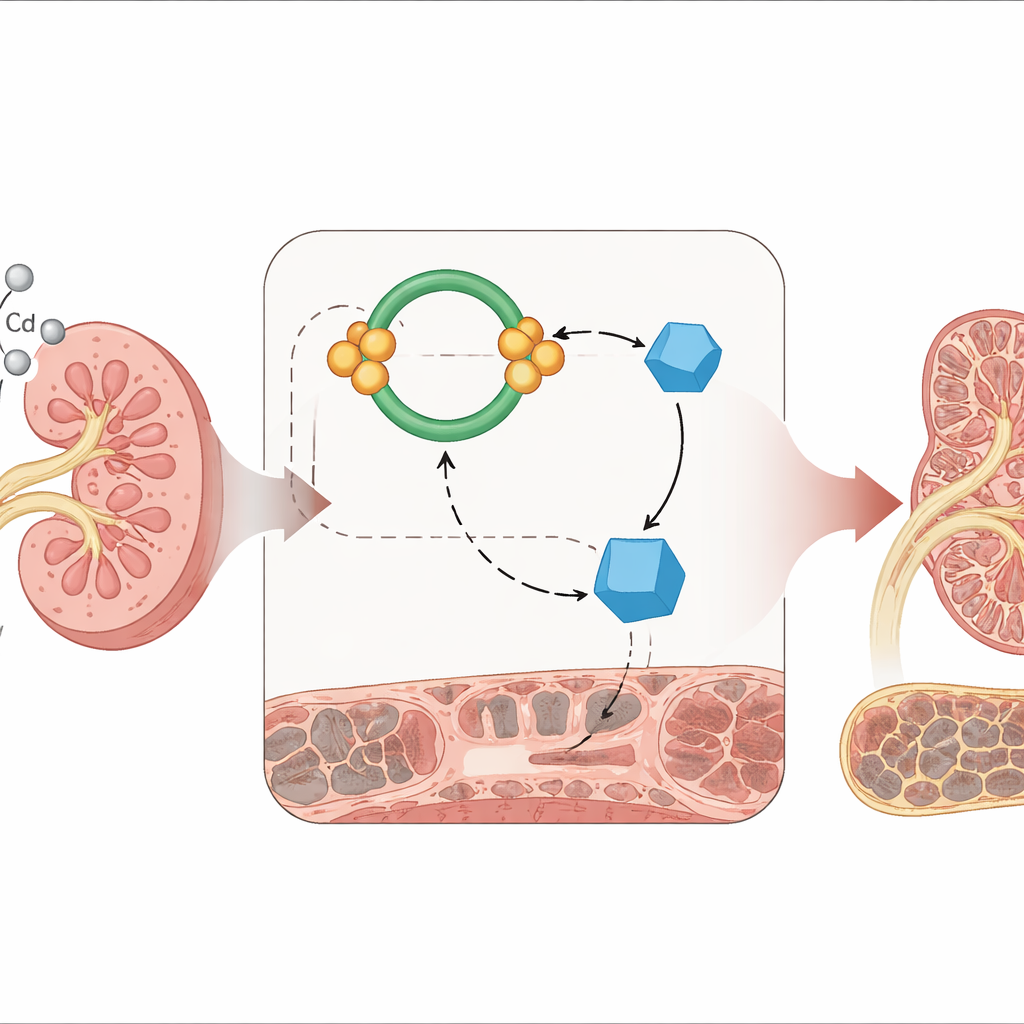
تأكيد الضرر في كِلى حية
ثم انتقل الباحثون إلى نموذج فأر ليروا ما إذا كانت هذه النمطية الجزيئية تظهر أيضاً في حيوانات حية. أُعطيت الفئران الكادميوم عن طريق الفم لمدة ثلاثة أشهر بجرعات اختيرت لتقليد التعرض البيئي طويل الأمد. تحت الميكروسكوب، أظهرت كُلى الفئران المعاملة بالكادميوم تغيّرات ليفية واضحة — ألياف الكولاجين المصبوغة باللون الأزرق تملأ المسافات بين الأنابيب. وجدت الاختبارات الكيميائية الحيوية نتائج مطابقة لنتائج مزروعات الخلايا: ارتفعت بروتينات التندب، وانخفض البروتين الحامي KLF4، وزادت مستويات miR-363-3p في الكليتين، مما يدعم الفكرة أن هذا المسار نشط خلال الضرر البطيء للواقع الميداني للكادميوم.
ماذا يعني هذا لحماية الكلى
تشير النتائج مجتمعة إلى أن الكادميوم يعزز تندب الكلى عن طريق تعطيل توازن دقيق بين RNA دائري وميكروRNA وبروتين حامي. عندما يقلل الكادميوم من مستوى الـ RNA الدائري وKLF4، يتحرر miR-363-3p لدفع الخلايا نحو التليف. للقراء غير المتخصصين، الرسالة الأساسية هي أن التحولات الجزيئية المبكرة — قبل ظهور الأعراض بفترة طويلة — قد تخدم يوماً ما كمنبهات تحذيرية في اختبارات الدم أو البول للأشخاص المعرضين للكادميوم. وبينما يلزم المزيد من العمل السريري، خاصةً في المرضى البشر، يشير هذا المسار المرسوم حديثاً إلى أدوات مستقبلية ممكنة لاكتشاف وإبطاء تلف الكلى الناتج عن الكادميوم قبل أن يحدث تندب لا رجعة فيه.
الاستشهاد: Zhou, J., Huang, Y., Li, G. et al. Cadmium exposure induces renal fibrosis by inhibiting hsa_circ_0075684/miR-363-3p/KLF4 signaling pathway. Sci Rep 16, 8754 (2026). https://doi.org/10.1038/s41598-026-39715-w
الكلمات المفتاحية: التعرّض للكادميوم, تليف الكلى, الميكرو RNA, علم السموم البيئي, مرض الكلى المزمن