Clear Sky Science · ar
التأثير البيولوجي النسبي المعتمد على الجرعة والزمن للبروتون في خلايا دماغية داخل المخ مختلفة
لماذا تهم هذه الدراسة عن إشعاع الدماغ
مع ظهور مراكز العلاج بالبروتونات في مستشفيات أكثر، يُخبر العديد من المرضى أن حزم البروتون يمكن أن تضرب الأورام بقوة أكبر مع الحفاظ بشكل أفضل على أنسجة المخ السليمة مقارنةً بالإشعاع التقليدي بالأشعة السينية (الفوتونات). لكن ما مدى لطف البروتونات على الدماغ الحي فعلاً، وهل يتغير هذا التفوق مع مرور الوقت؟ استخدمت هذه الدراسة نموذجًا حيوانيًا مفصلاً لتتبع كيف تستجيب أنواع مختلفة من خلايا الدماغ للإشعاع البروتوني مقابل الفوتوني على مدى أسابيع، مقدمًة دلائل قد تؤثر على كيفية علاج أورام الدماغ بأمان وحماية القدرات الإدراكية والذاكرة.
إلقاء نظرة داخل مجتمع خلايا الدماغ
الدماغ ليس إسفنجة متجانسة من النسيج العصبي؛ إنه مجتمع من الخلايا المتخصصة التي تتفاعل مع الإصابات بطرق مميزة. ركز الباحثون على ثلاثة لاعبين رئيسيين في الأرانب: الخلايا العصبية، التي تعالج الإشارات وتشكل أساس الذاكرة؛ الخلايا الشحمية (oligodendrocytes)، التي تعزل الألياف العصبية لكي تنتقل الإشارات بسرعة؛ والمايكروغليا، وهي خلايا المناعة المقيمة في الدماغ. استهدفت الفرق كامل الدماغ إما بإشعاع بروتوني أو فوتوني عند عدة مستويات جرعة تقارب إلى حد ما العلاجات السريرية القوية، ثم فحصت منطقتين حاسمتين للتفكير ونقل المعلومات — الحُصين (hippocampus) والمِهاد (thalamus) — على مدار شهرين.
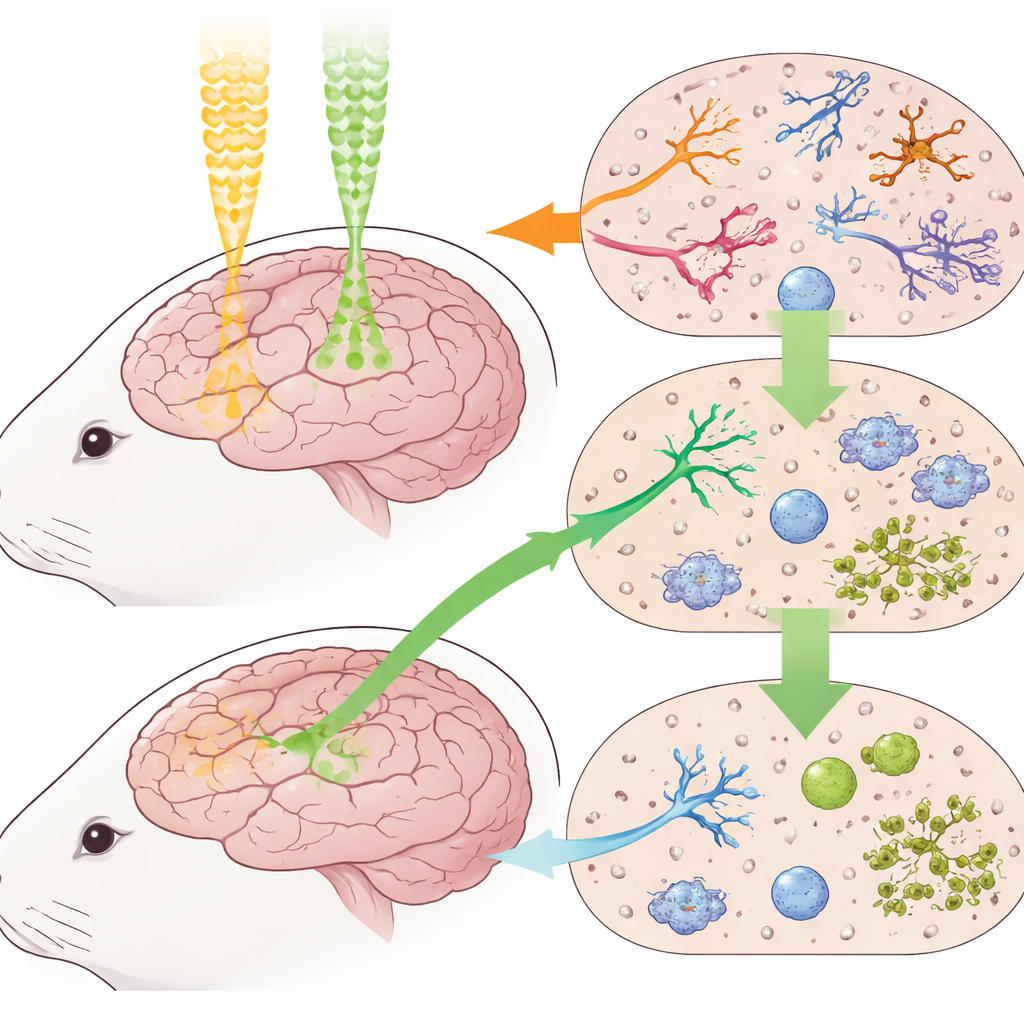
كيف أُجريت التجارب
تلقت مجموعات من الأرانب جرعات دماغية مفردة قدرها 10، 20، 30، أو 40 غراي من الإشعاع، إما كفوتونات أو كبروتونات، بينما لم تتلقَ مجموعة الضبط أي إشعاع. ثم ذُبحت الحيوانات بعد 2، 4، 6، أو 8 أسابيع، وعُولجت أدمغتها إلى شرائح رقيقة. استُخدمت صبغات نسيجية قياسية لعدّ الخلايا العصبية التالفة مقابل تلك التي تبدو سليمة، بينما أظهرت صبغات مضادّة خاصة الألياف العصبية والخلايا الشحمية والمايكروغليا المنشّطة. باستخدام هذه العدّات، طَبَّق الفريق نموذجًا رياضيًا شائع الاستخدام للاستجابة للإشعاع لحساب ما يُسمى بالفعالية البيولوجية النسبية (RBE) — وهو مقياس لمدى فعالية البروتونات مقارنةً بالفوتونات — لكل نوع خلية، وجرعة، ونقطة زمنية.
ما الذي حدث للخلايا العصبية وخلايا الدعم
أصاب الإشعاعان الخلايا العصبية بوضوح، وتراكمت الأضرار مع الوقت. ومع ذلك، من الأسبوع الرابع إلى الثامن بعد العلاج، أظهرت الأدمغة المعرضة للإشعاع البروتوني بقاءً أعلى للخلايا العصبية وألياف عصبية أفضل حفظًا مقارنة بتلك المعرضة لنفس الجرعات المسماة من الفوتونات، لا سيما عند جرعات 10 و20 و30 غراي. خلصت الخلايا الشحمية إلى قصة مشابهة: عند الجرعات المتواضعة والنقاط الزمنية المتأخرة، كانت أعدادها غالبًا أعلى في الأدمغة المعالجة بالبروتونات مقارنةً بتلك المعالجة بالفوتونات، مما يوحي بأن المادة البيضاء العازلة قد تتحمل تعرض البروتونات بشكل أفضل إلى حد ما. عند ترجمة هذه الملاحظات إلى قيم RBE، وقعت الفعالية طويلة المدى للبروتون على الخلايا العصبية والشحمية عمومًا أقل من القيمة المفترضة شائعًا 1.1، وأحيانًا بفارق كبير، ما يعني أن نسيج الدماغ الحقيقي قد يتحمل جرعات فيزيائية بروتونية أعلى مما تفترض قواعد التخطيط الحالية المتحفظة.
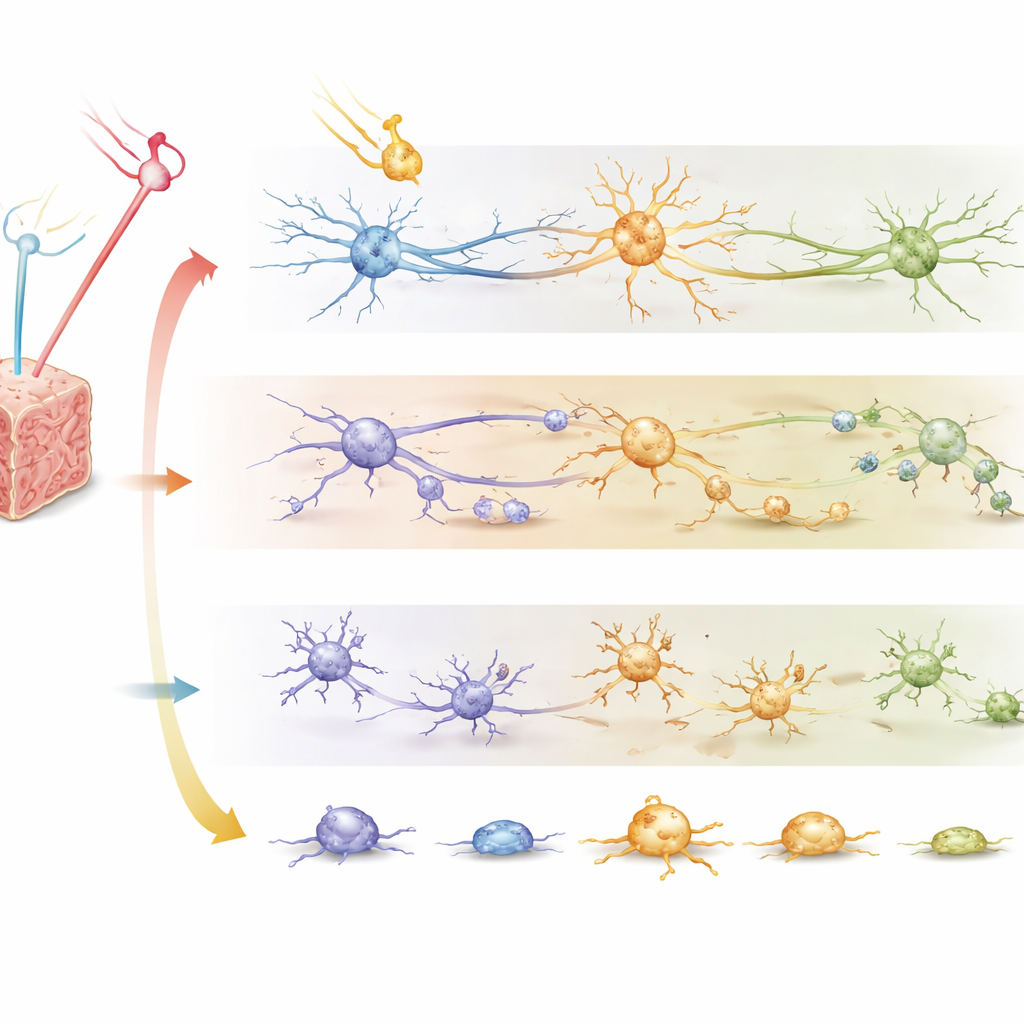
استجابة المناعة الدماغية تبرز صورة مختلفة
تصرفت المايكروغليا بشكل مختلف. تصبح خلايا المناعة هذه "منشطة" عند اكتشافها للإصابة، فتتغير شكلها وتطلق جزيئات التهابية يمكن أن تساعد أو تضر. عبر معظم الجرعات والأزمنة، ارتفعت نسبة تنشيط المايكروغليا مع زيادة الجرعة ثم خفتت ببطء خلال الأسابيع لكلا نوعي الإشعاع. ومع ذلك، في ظروف معينة — وأبرزها بعد أربعة أسابيع من جرعة بروتونية متوسطة النطاق — حفزت البروتونات تنشيطًا مايكروغليًا أقوى ملحوظًا مقارنة بالفوتونات. عندما احتسب الباحثون RBE لعلامة الاستجابة المناعية هذه، تجاوزت العديد من القيم 1.1، على عكس نمط الخلايا العصبية والخلايا الشحمية. وهذا يوحي بأنه بينما قد تحمي البروتونات الخلايا العصبية وخلايا الدعم، فإنها قد تثير رد فعل التهابي أكثر حدة، وهو سيف ذو حدين قد يؤثر على كلٍ من الآثار الجانبية ونجاح العلاجات المدمجة مع المناعة.
ما معنى هذا لعلاجات الدماغ المستقبلية
بالنسبة للمرضى والأطباء، الخلاصة أن التأثير البيولوجي للعلاج بالبروتون في الدماغ ليس رقمًا ثابتًا بل هدفًا متغيرًا يعتمد على نوع الخلية والجرعة والوقت بعد العلاج. في هذا النموذج الأرنبّي، كانت الخلايا العصبية وشركاؤها العازلون أفضل حالًا في نهاية المطاف تحت الإشعاع البروتوني مقارنة بالفوتونات، ما يدعم فكرة أن الدماغ قد يتحمل بأمان جرعات بروتونية أعلى قليلًا أو أشدّ شكلًا مما تفترض المعايير المحافظة الحالية. وفي الوقت نفسه، يشير ارتفاع تنشيط المايكروغليا إلى أن البروتونات قد تعيد تشكيل بيئة المناعة الدماغية بطرق معقدة، مما قد يفتح أبوابًا لتركيبات أذكى مع العلاجات المعتمدة على المناعة. مجتمعة، تدفع هذه النتائج نحو تخطيط إشعاعي أكثر تخصيصًا يتجاوز مجرد الجرعة وينظر في كيفية عيش وموت وإصلاح خلايا الدماغ المختلفة بعد العلاج البروتوني مقابل الفوتوني.
الاستشهاد: Wang, X., Guo, Y., Zhang, J. et al. Dose- and time-dependent relative biological effect of proton in different intracerebral cells. Sci Rep 16, 8984 (2026). https://doi.org/10.1038/s41598-026-39669-z
الكلمات المفتاحية: العلاج بالبروتونات, إشعاع الدماغ, الخلايا العصبية, المايكروغليا, آثار جانبية للإشعاع