Clear Sky Science · ar
استهداف أنواع عصبية محددة في دماغ الرئيسيات غير البشرية باستخدام سم مناعي مصلَّد مُعاد تركيبه مخصص لـ CD25 المأخوذ من فأر
لماذا تهم هذه الدراسة الدماغية
فهم كيف تتحكم مجموعات محددة من خلايا الدماغ في الحركة والعاطفة والسلوك أمر أساسي لعلاج اضطرابات مثل مرض باركنسون والتوحد. لكن الدماغ يمثل غابة كثيفة من الخلايا المتداخلة، ومعظم الأدوات تقطع العديد من الأشجار دفعة واحدة. تقدم هذه الدراسة طريقة لإزالة نوع مختار فقط من الخلايا العصبية في دماغ القرد مع حد أدنى من الأضرار الجانبية، مما يفتح الباب لتجارب أكثر دقة حول كيفية تشكيل الحلقات العصبية لسلوكيات واعتلالات محددة.
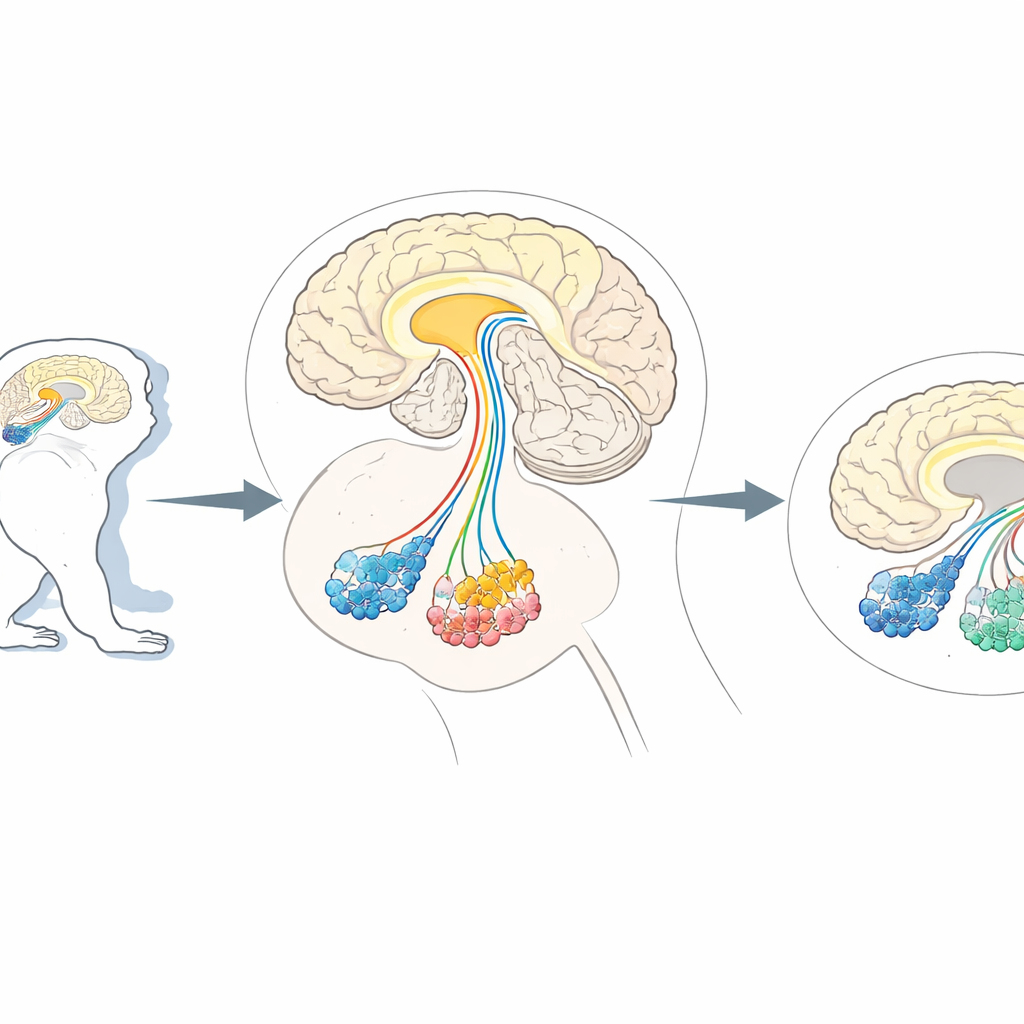
حاجة إلى "تقليم" خلوي دقيق للدماغ
غالبًا ما يلجأ الباحثون إلى الرئيسيات غير البشرية، مثل المارموسيت والماكاك، لأن أدمغتها منظمة بشكل مشابه لأدمغتنا. هذه الحيوانات نماذج لا تقدر بثمن للحالات التي تؤثر على وظائف الدماغ العليا، من مشاكل الحركة الشبيهة بالباركنسونية إلى تغيّرات شبيهة بالتوحد في السلوك الاجتماعي. تستطيع الأساليب الحالية كتم أو تنشيط مسارات محددة، لكن إزالة نوع واحد فقط من الخلايا العصبية في هذه الأدمغة المعقدة دون الإضرار بالآخرين بقيت صعبة. أظهرت أعمال سابقة في الفئران خدعة: تم تعديل خلايا منتقاة لتعرض علامة سطحية خلوية بشرية تُسمى CD25، يمكن للتوكسين المصمَّم التعرف عليها وقتل تلك الخلايا المعلَّمة فقط. مع ذلك، تتواجد هذه العلامة طبيعيًا في خلايا الجهاز المناعي وربما في خلايا دماغ الرئيسيات، ما يرفع خطر أن يهاجم السم الأهداف الخاطئة في القرود.
تصميم مشرط جزيئي أكثر أمانًا
انطلق المؤلفون لبناء مشرط جزيئي جديد مخصص للاستخدام في الرئيسيات. بدلاً من استهداف النسخة البشرية من CD25، ركزوا على النسخة الفأرية، وهي أقل تشابهًا بكثير مع CD25 الطبيعي الموجود في القرود. بدأوا بتمنيع أرنب ببروتين CD25 الفأري واستخدموا طريقة قائمة على رقائق لاصطياد خلايا أرنب مفردة أنتجت أجسامًا مضادة ترتبط بقوة بـ CD25 الفأري لكن ليس بالشكل البشري. من بين هذه حددوا جسمًا مضادًا مميزًا سمّوه RMAb-52، ذو قوة ارتباط عالية جدًا. ثم جمعوا الأجزاء الأساسية من هذا الجسم المضاد مع شظية سامة من بكتيريا Pseudomonas لإنشاء بروتين "سم مناعي" مهندس واحد، سمُّوه anti-mCD25-PE38.
اختبار الأداة
في تجارب داخل أنابيب الاختبار، ارتبط السم المناعي الجديد بـ CD25 الفأري بشكل أقوى بكثير مقارنةً بـ CD25 البشري، مؤكِّدًا انتقائيته. عند تطبيقه على خلايا مزروعة مُهندَسة لتحمل CD25 الفأري، قلّل السم بشكل حاد من بقائها بجرعات منخفضة جدًا، بينما ترك الخلايا الحاملة لـ CD25 البشري سليمة. بعد ذلك انتقل الفريق إلى المارموسيت الحي. باستخدام ناقل فيروسي خاص يسافر رجعيًا على طول الألياف العصبية، نقلوا جين CD25 الفأري إلى الخلايا العصبية المنتجة للدوبامين التي ترسل إشارات من منطقة عميقة في الدماغ تُسمى المادة السوداء إلى الجسم المخطط، وهو مسار حاسم للتحكم في الحركة. وبعد أن منحوا الفيروس وقتًا لتشغيل العلامة في هذه الخلايا، حقنوا بروتين anti-mCD25-PE38 مباشرة في منطقة منتصف الدماغ المستهدفة.
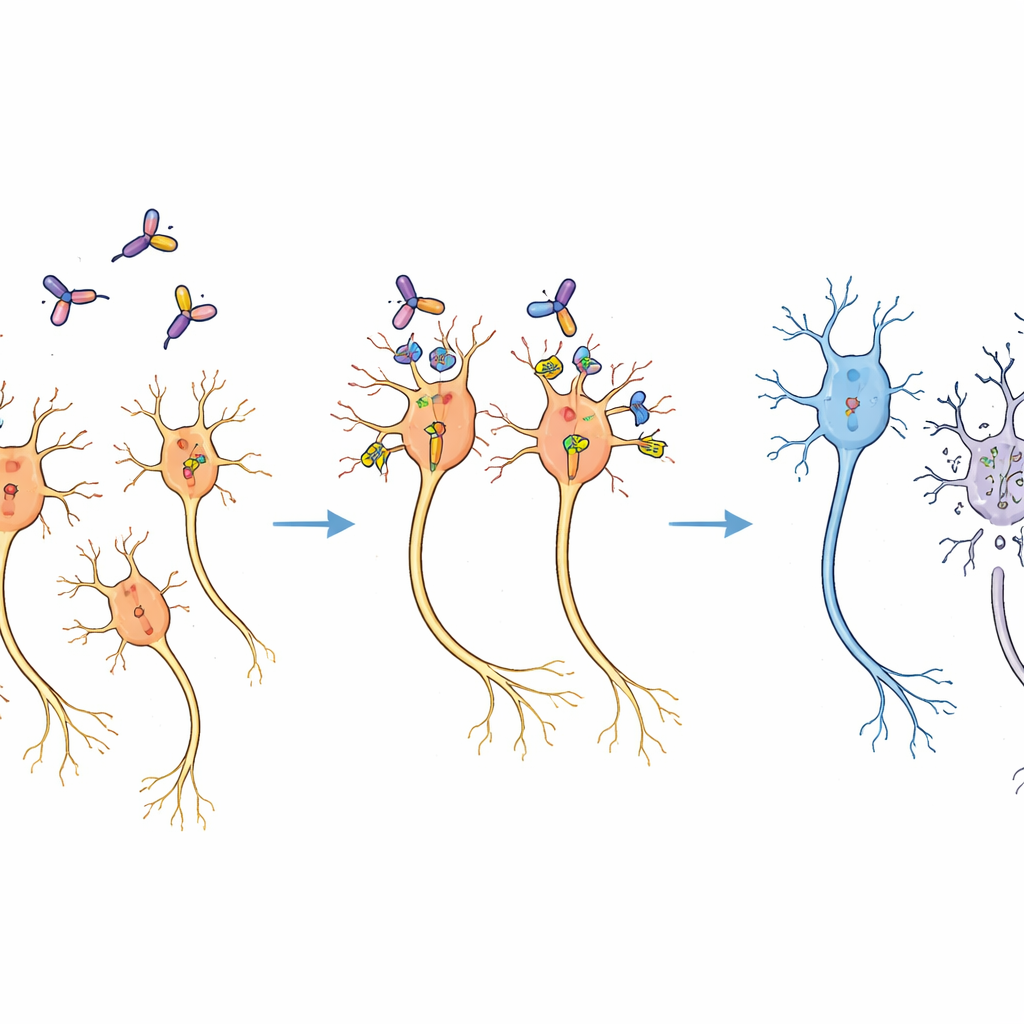
فقدان انتقائي دون تلف واسع النطاق
بعد أسبوعين من العلاج، سردت شرائح دماغ المارموسيتين قصة واضحة. في الجهة التي تلقت السم المناعي، انخفض عدد خلايا الدوبامين إلى نحو ثلثي العدد في الجهة غير المعالجة، كما أظهر ذلك التلوين لإنزيم يصنع الدوبامين. ومع ذلك بدا النسيج الدماغي المحيط طبيعيًا تحت المجهر، ولم تظهر مناطق دماغية أخرى تلقت الناقل الفيروسي خسارة خلوية واضحة. كانت التجارب التمهيدية قد حدّدت بالفعل نطاق جرعات يتجنب إصابة النسيج غير النوعي، والجرعة المختارة وقعت بسهولة ضمن هذا النطاق الآمن. نمط الخسارة طابق الانتشار المتوقع للفيروس والسم، مما يشير إلى أن الخلايا العصبية أُزيلت بشكل انتقائي لأنها جُهِزت لعرض CD25 الفأري، لا لأن السم كان يضر الخلايا بشكل عشوائي.
ما يعنيه هذا لبحوث الدماغ المستقبلية
للقارئ العادي، الرسالة الأساسية هي أن الباحثين صنعوا زر حذف انتقائي للغاية لمجموعات عصبية مختارة في أدمغة الرئيسيات. من خلال الجمع بين نظام توصيل فيروسي رجعي وسم مناعي مخصص للفأر، يمكنهم إزالة مسارات محددة — على سبيل المثال، دوائر الدوبامين المرتبطة بمرض باركنسون — مع الحفاظ على الخلايا المجاورة. تتجنب هذه الاستراتيجية تفاعلات متقاطعة خطرة مع CD25 الخاص بالحيوان ويجب أن تكون مفيدة بشكل خاص عندما يكون هذا المستقبل الطبيعي موجودًا أو مرتفعًا في المرض. على المدى الطويل، سيساعد هذا النهج العلماء في رسم خريطة كيف تساهم المسارات الفردية في توصيلات الدماغ في الحركة واتخاذ القرار والأعراض النفسية، مما يقربنا من علاجات مستهدفة تضبط الحلقات المعطوبة بدلًا من التأثير على الدماغ بأكمله بصورة عامة.
الاستشهاد: Kobayashi, T., Kato, S., Kimura, S. et al. Targeting of specific neuronal types in the non-human primate brain by using a murine CD25-specific recombinant immunotoxin. Sci Rep 16, 8247 (2026). https://doi.org/10.1038/s41598-026-39662-6
الكلمات المفتاحية: علوم الأعصاب في الرئيسيات غير البشرية, استهداف بالسموم المناعية, خلايا الدوبامين العصبية, دوائر دماغ المارموسيت, نماذج مرض باركنسون