Clear Sky Science · ar
العامل المستحث بنقص الأكسجين 1α يمارس أدوارًا مزدوجة في تقدم سرطان المثانة من خلال تنظيم التكوّن الوعائي والغزو بواسطة TIMP3
لماذا تهم الأورام الفقيرة بالأكسجين
تنمو الخلايا السرطانية غالبًا بسرعة تتجاوز خلالها إمدادها الدموي، مما يترك أجزاء من الورم محرومة من الأكسجين. هذا المحيط منخفض الأكسجين، أو نقص الأكسجة، يضطر الخلايا إلى تفعيل برامج بقاء قد تجعل السرطان أصعب على العلاج. في سرطان المثانة — وهو ورم شائع في الجهاز البولي — اشتبه العلماء منذ زمن طويل أن أحد هذه البرامج المستشعرة للأكسجين، الذي يتحكم به بروتين يُسمى HIF-1α، يساعد أساسًا الأورام على النمو والانتشار. تفحص هذه الدراسة الموضوع عن كثب وتكشف مفاجأة: في ظل ظروف معينة، قد يؤدي خفض مستوى HIF-1α فعليًا إلى جعل خلايا سرطان المثانة أكثر عدوانية، ويقع بروتين ثانٍ، TIMP3، في قلب هذا التناقض.
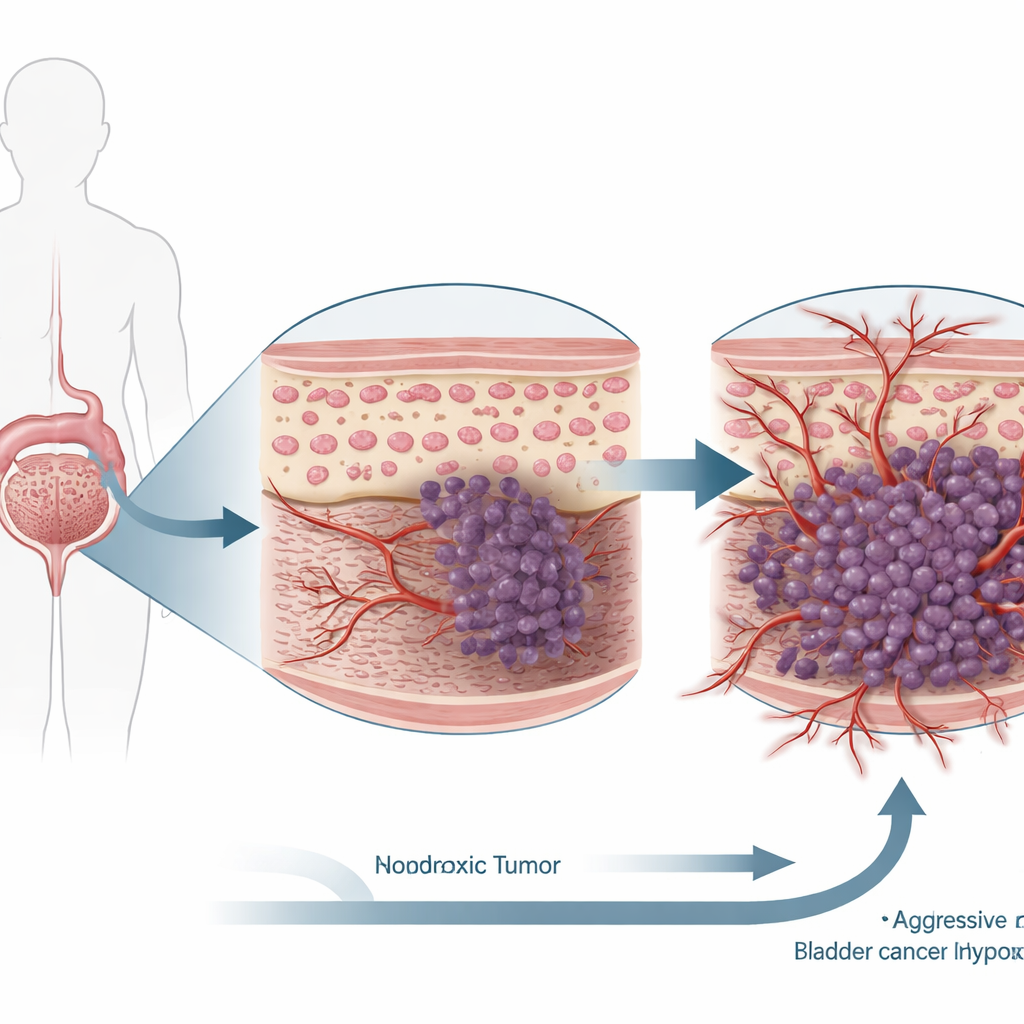
نظرة أعمق على خلايا سرطان المثانة
عمل الباحثون مع سطرَي خلايا بشريتين معروفتين لسرطان المثانة وعَرّضوها إما لمستويات أكسجين طبيعية أو لنقص أكسجة، محاكيًا الجيوب منخفضة الأكسجين داخل الأورام الحقيقية. ثم استخدموا أدوات وراثية لتقليل HIF-1α في هذه الخلايا وقياس كيف أثّر هذا التغيير على السلوكيات الأساسية للسرطان: مدى سرعة تكاثر الخلايا، ومدى قابليتها للموت، ومدى قدرتها على الحركة، والغزو عبر حاجز، وتشجيع تكوّن أوعية دموية جديدة. وبالتوازي، فحصوا عينات أورام المثانة من المرضى لمقارنة مستويات HIF-1α وTIMP3 في النسيج السرطاني مقابل نسيج المثانة الطبيعي المجاور.
انقلاب دور مفاجئ تحت نقص الأكسجة
أكدت عينات المرضى أن مستوى HIF-1α أعلى بالفعل في أورام المثانة مقارنة بالنسيج الطبيعي، بما يتوافق مع سمعته كعامل يعزز الورم. ومع ذلك، في تجارب الخلايا تحت نقص الأكسجة، أدى تقليل HIF-1α إلى نتيجة عكسية عما قد يتوقعه كثيرون. عندما تم قمع HIF-1α بينما كان الأكسجين نادرًا، نمَت الخلايا السرطانية أسرع مع مرور الوقت، وكانت أقل احتمالًا للخضوع للموت المبرمج، وأصبحت أفضل في الهجرة والغزو عبر حواجز نموذجية. كما أنها أفرجت عن إشارات شجعت خلايا الأوعية الدموية على تشكيل شبكات أنبوبية أكثر كثافة واتساعًا، وهي سمة مميزة لزيادة إمداد الورم بالدم. باختصار، بانخفاض HIF-1α في بيئة منخفضة الأكسجين، تصرفت خلايا سرطان المثانة بشكل أكثر خباثة.
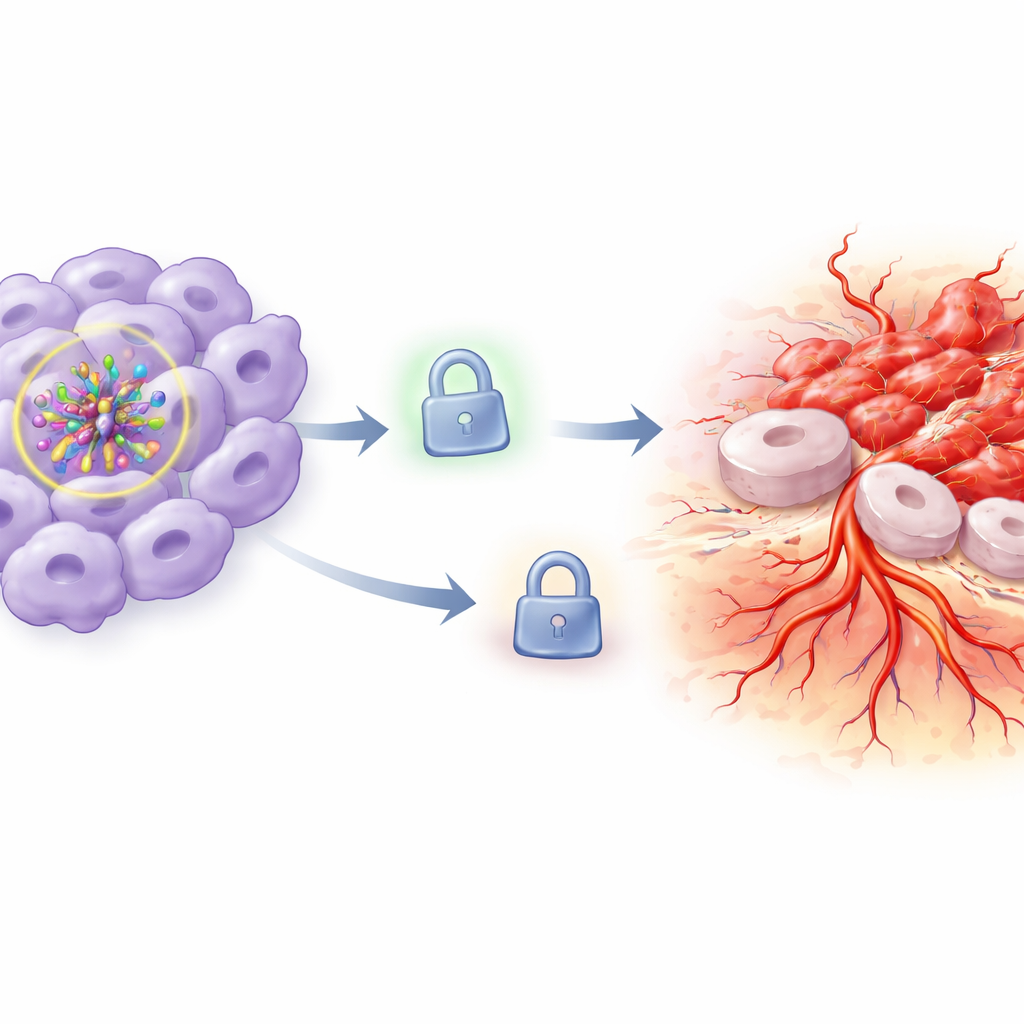
الفرامل المفقودة أمام انتشار الورم
لفهم سبب حدوث ذلك، ركز الفريق على TIMP3، وهو بروتين يعمل عادة كفرامل على تكسير النسيج وتكوين أوعية جديدة عن طريق حجب الإنزيمات التي تقطع المصفوفة المحيطة. في الخلايا التي انخفض فيها HIF-1α والمحفوظة تحت أكسجين طبيعي، ظلت مستويات TIMP3 مرتفعة نسبيًا. لكن عندما انخفض مستوى الأكسجين، هبط بروتين TIMP3 بشكل حاد. يتماشى هذا الفقدان لـTIMP3 مع الزيادة الملحوظة في الغزو وتكوّن الأوعية: مع ضعف الفرامل، تمكنت الخلايا السرطانية من إعادة تشكيل محيطها والتوسع بسهولة أكبر. ثم قلب الباحثون الوضع بفرض إنتاج زائد لـTIMP3 في الخلايا بينما كان HIF-1α ما يزال منخفضًا تحت نقص الأكسجة. استعادة TIMP3 عكست السلوك العدواني جزئيًا أو بشكل شبه كامل: قلّ تكاثر الخلايا، وزاد موتها، وانخفضت حركتها وغزوها، وتحفّزت أنابيب وعائية أقل وطولًا أقل.
ماذا يعني هذا للعلاجات المستقبلية
تشير هذه النتائج إلى أن لـHIF-1α شخصية مزدوجة في سرطان المثانة. من ناحية، تكون مستوياته الإجمالية أعلى في الأورام ويساهم في دفع برامج معروفةً مفضلة للسرطان. ومن ناحية أخرى، تحت نقص الأكسجة الشديد يبدو أنه يساعد في الحفاظ على الحضور الوقائي لـTIMP3. قد يؤدي إزالة HIF-1α في هذا السياق بطريق الخطأ إلى خفض TIMP3 وإطلاق سلوكيات أكثر غزوًا وتحفيزًا لتكوّن الأوعية. بالنسبة للعلاج، يعني ذلك أن حجب HIF-1α ببساطة قد ينعكس عليه ما لم يجد الأطباء طرقًا أيضًا للحفاظ على TIMP3، أو فرامل مشابهة، في مكانها. يبرز هذا العمل أهمية فهم ليس الهدف الواحد فحسب، بل الشبكة الأوسع من الضوابط والتوازنات التي تشكل كيفية استجابة الورم لبيئته القاسية الفقيرة بالأكسجين.
الاستشهاد: Wang, X., Guo, J., Zhang, R. et al. Hypoxia-inducible factor 1α exerts dual roles in bladder cancer progression through TIMP3-mediated regulation of angiogenesis and invasion. Sci Rep 16, 8425 (2026). https://doi.org/10.1038/s41598-026-39635-9
الكلمات المفتاحية: سرطان المثانة, نقص أكسجة الورم, HIF-1α, TIMP3, تكوّن الأوعية الدموية