Clear Sky Science · ar
حل التناقض بين المحاكاة والنتائج التجريبية لاستخدام جسيمات الذهب النانوية في العلاج بالبروتونات
لماذا تهم جسيمات الذهب الصغيرة في علاج السرطان
العلاج بالبروتونات هو شكل متقدّم من العلاج الإشعاعي يمكنه استهداف الأورام بدقة مع حماية الأنسجة السليمة المحيطة. في السنوات الأخيرة، حاول العلماء دمج هذا العلاج مع جزيئات ذهب نانوية دقيقة لزيادة فاعلية قتل الخلايا السرطانية. تُظهر التجارب أن هذا المزيج غالباً يقضي على عدد أكبر من خلايا الورم مقارنةً بالبروتونات وحدها—لكن محاكيات الحاسوب واجهت صعوبة في تفسير السبب. تتناول هذه الورقة ذلك اللغز طويل الأمد وتشير إلى فاعل رئيسي مختلف عما افترضه كثير من الباحثين.
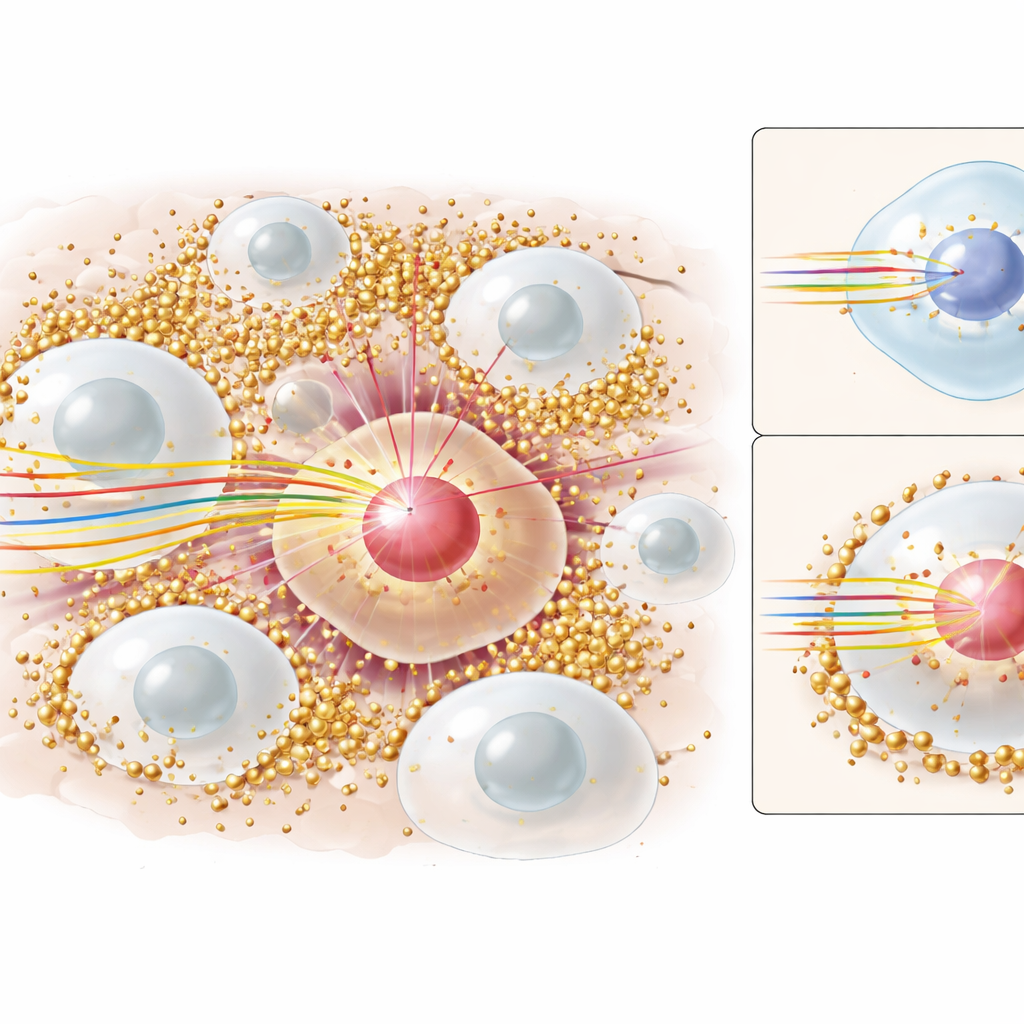
القصة القديمة: لوم الإلكترونات السريعة
جسيمات الذهب النانوية معروفة بالفعل في علاجات الأشعة السينية وأشعة غاما، حيث تعزز الضرر أساساً عن طريق انبعاث سحابات من الإلكترونات النشطة طاقياً. تنتقل تلك الإلكترونات لمسافات قصيرة وتكسر الحمض النووي في الخلايا القريبة. لسنواتٍ، افترض كثيرون أن نفس القصة تنطبق على العلاج بالبروتونات: تصطدم البروتونات بالذهب، وتطير إلكترونات إضافية، وتتعرض الخلايا السرطانية للأذى. لكن كان هناك مشكلة. ظلّت النماذج الحاسوبية التفصيلية التي تتعقب كل جسيم وطاقة—وهي النوع المستخدم في هذه الدراسة—تتنبأ بزيادة طفيفة جداً في الجرعة المتلقاة في نواة الخلية من هذه الإلكترونات، خاصة لأن معظم الجسيمات النانوية توجد في الجزء الخارجي من الخلية، وليس داخل النواة حيث يقع الحمض النووي. في المقابل، أظهرت التجارب المخبرية مع الخلايا زيادات واضحة في موت الخلايا وفاعلية العلاج بوجود الذهب. ببساطة، الأرقام لم تتطابق.
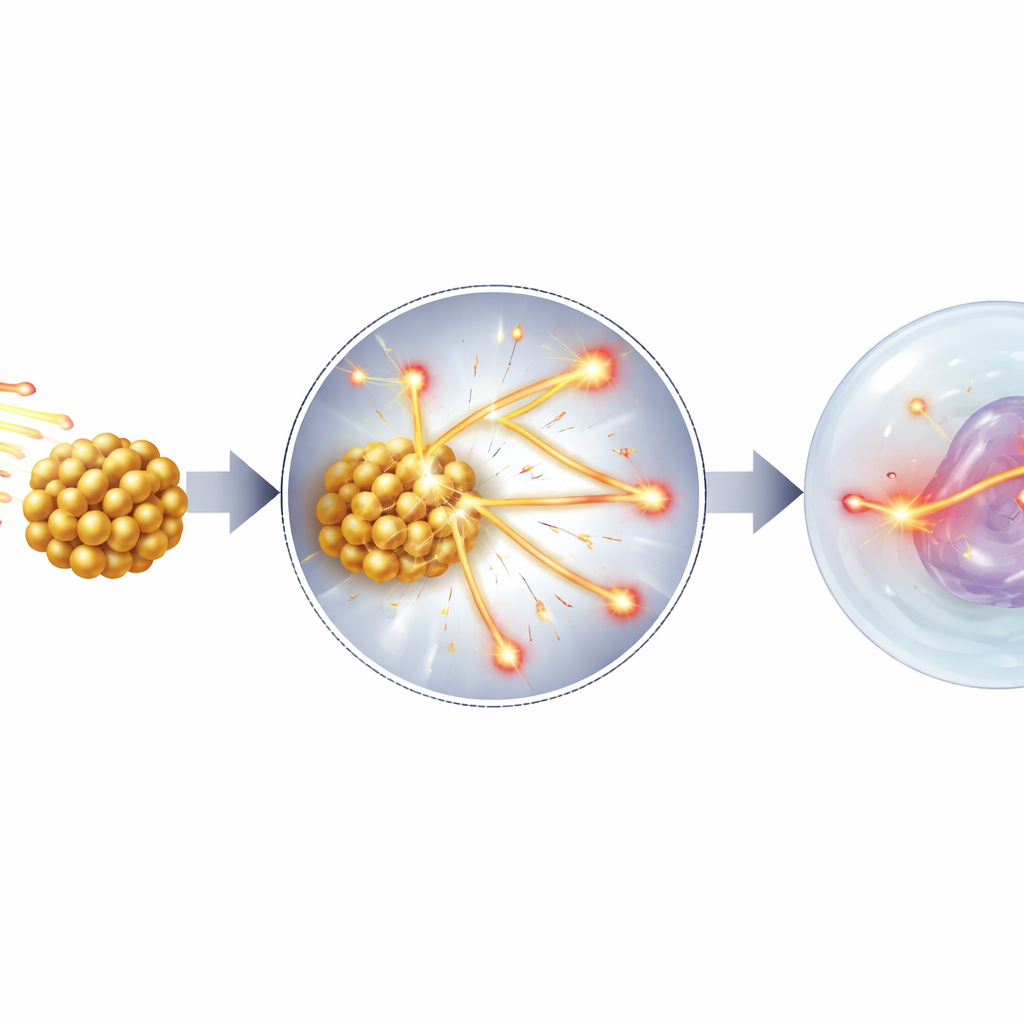
الصورة الجديدة: إبطاء البروتونات نفسها
تقترح هذه الدراسة وتختبر آلية رئيسية مختلفة: بدلاً من العمل كبواعث رئيسية للإلكترونات، تتصرف جسيمات الذهب النانوية كعوائق صغيرة تُبطئ البروتونات. عندما يمر بروتون عبر منطقة تحتوي على معادن ذات كثافة عالية ورقم ذري مرتفع مثل الذهب أو الحديد، يخضع لعدد كبير من التصادمات الصغيرة مع تلك الذرات الثقيلة. كل تصادم يسحب طاقة أكثر مما يحصل في نسيج عادي، فتتباطأ البروتونات بسرعة أكبر ويزداد فقدانها للطاقة لكل وحدة مسافة—ما يُعرف في الفيزياء بنقل الطاقة الخطي (LET). تكون المسارات ذات LET العالي أكثر إلحاقاً بالضرر بالحمض النووي لأنها تخلق تجمعات كثيفة من الكسور التي تكافح الخلية لإصلاحها. باستخدام محاكيات مونتي كارلو التفصيلية عبر حزمة Geant4، يظهر المؤلف أن الذهب وغيره من الجسيمات النانوية الثقيلة يعززون بشكل كبير عدد البروتونات البطيئة وذات LET العالي التي تصل إلى نواة الخلية، حتى وإن كان طول المسار في مقياس الميكرومتر، أبعد بكثير من مدى الإلكترونات منخفضة الطاقة التي نُسب إليها التقليدياً الدور.
مزامنة المحاكاة مع تجارب الخلايا الحقيقية
لاختبار صحة هذه الصورة الجديدة، تعيد الدراسة إنشاء عدة تجارب خلوية منشورة عُولجت فيها أورام بأشعة بروتونية مع جزيئات نانوية مختلفة (ذهب، حديد، وبلاتين) بأحجام وتركيزات متنوعة. لكل حالة، تحسب المحاكاة مقدار الجرعة الإضافية التي تتلقاها النواة—ملخّصةً كنسبة تعزيز الجرعة—ثم توظف ذلك في صيغة قياسية في علم الأحياء الإشعاعي تربط الجرعة المُسَلَّمة ببقاء الخلايا. يغيّر هذا النهج المنحنى المعتاد الذي يصف كم من الخلايا تبقى أو تموت بعد جرعة معينة من الإشعاع. في معظم التجارب التي فُحصت، توافقت منحنيات البقاء المتوقعة مع الجسيمات النانوية مع البيانات المقاسة بشكل وثيق، غالباً ضمن خطأ يقارب واحد بالمئة. في الوقت نفسه، تُظهر المحاكاة أن جرعة الإلكترونات في النواة بالكاد تتغير عند إضافة الجسيمات النانوية، بينما تزداد بوضوح سريان (Fluence) البروتونات الأبطأ والأكثر ضرراً. تبقى بعض الاختلافات الطفيفة، ويُعزوها المؤلف إلى عدم اليقين في كيفية إعداد بعض التجارب أو الإبلاغ عنها، لكن الاتجاه العام يدعم بشدة تفسير إبطاء البروتونات.
الحدود والاستثناءات ومتى يفيد الذهب أكثر
تستعرض الورقة أيضاً الحالات التي لا تبدو فيها الجسيمات النانوية مفيدة كثيراً. بالنسبة لحزم البروتون منخفضة الطاقة جداً التي تتوقف ضمن بضعة طبقات خلوية فقط، لا توجد مسافة كافية لاصطدام البروتونات بعدد كبير من الجسيمات النانوية وإبطائها بشكل ملموس، لذلك لا يُرى تعزيز قوي في الفاعلية. وبالمثل، فإن بعض أشكال الجسيمات النانوية المعقدة أو الهندسات التجريبية الموصوفة بشكل ضعيف يصعب تكرارها في المحاكاة، وقد يفسر ذلك بعض الحالات الشاذة حيث تختلف النماذج عن القياسات. يشير المؤلف إلى أنه إذا دخلت جسيمات بالغة الصغر النواة فعلياً، فقد تضيف انبعاث الإلكترونات والتفاعلات الكيميائية مع جزيئات الخلية إلى التأثير. ومع ذلك، عبر العديد من شروط العلاج الواقعية، النمط السائد متسق: مزيد من إبطاء البروتونات في مناطق غنية بالذهب يؤدي إلى ضرر أكثر تركيزاً في النواة.
ماذا يعني هذا لرعاية السرطان في المستقبل
لغير المتخصصين، الرسالة الأساسية هي أن جسيمات الذهب النانوية في العلاج بالبروتونات تعمل أقل كمسدسات إلكترونية صغيرة وأكثر كفرامل غير مرئية تحول البروتونات السريعة واللطيفة نسبياً إلى ضاربين أبطأ وأقوى تماماً في المكان الذي يهمّ أكثر—حمض نووي خلية الورم. من خلال توضيح هذه الآلية وإظهار أنها قادرة على إعادة إنتاج بيانات بقاء الخلايا الحقيقية بدقة، تساعد الدراسة في حل صراع طويل بين النظرية والتجربة. يمكن أن يوجّه هذا الفهم تصميمات أذكى للعلاجات القائمة على الجسيمات النانوية، مثل اختيار المواد والأحجام والتركيزات التي تزيد من إبطاء البروتونات قرب نوى الأورام مع تقليل الآثار الجانبية. على المدى الطويل، قد يجعل ذلك العلاج بالبروتونات أكثر دقة وقوة، مما يوفر نتائج أفضل للمرضى ذوي الأورام الصعبة العلاج.
الاستشهاد: Tabbakh, F. Resolving the contradiction between simulation and experimental results of using gold nanoparticles in proton therapy. Sci Rep 16, 8012 (2026). https://doi.org/10.1038/s41598-026-39621-1
الكلمات المفتاحية: العلاج بالبروتونات, جسيمات الذهب النانوية, زيادة التأثر الإشعاعي, العلاج الإشعاعي للسرطان, طب النانو