Clear Sky Science · ar
مراكبات جديدة من بنزيميدازول-ألكان سلفونات كمثبطات كولينستراز مع تحقق معملي ومحاكاة حاسوبية
لماذا تهم هذه الدراسة الذاكرة والشيخوخة
يتسبب مرض ألزهايمر في تآكل تدريجي للذاكرة والاستقلالية وجودة الحياة لملايين الأشخاص حول العالم، ومع ذلك فإن الأدوية المتاحة اليوم تخفف الأعراض في الغالب دون إبطاء التلف الأساسي. تستكشف هذه الدراسة عائلة جديدة من الجزيئات المُحضّرة في المختبر المصممة لحماية مادة كيميائية دماغية رئيسية مشاركة في التعلم والذاكرة بشكل أفضل، مع مكافحة الإجهاد التأكسدي الضار في الوقت نفسه. من خلال دمج ميزات عدة أنواع ناجحة من الأدوية في بنية واحدة، يسعى الباحثون للاقتراب خطوة نحو علاجات أكثر فعالية لمرض ألزهايمر.
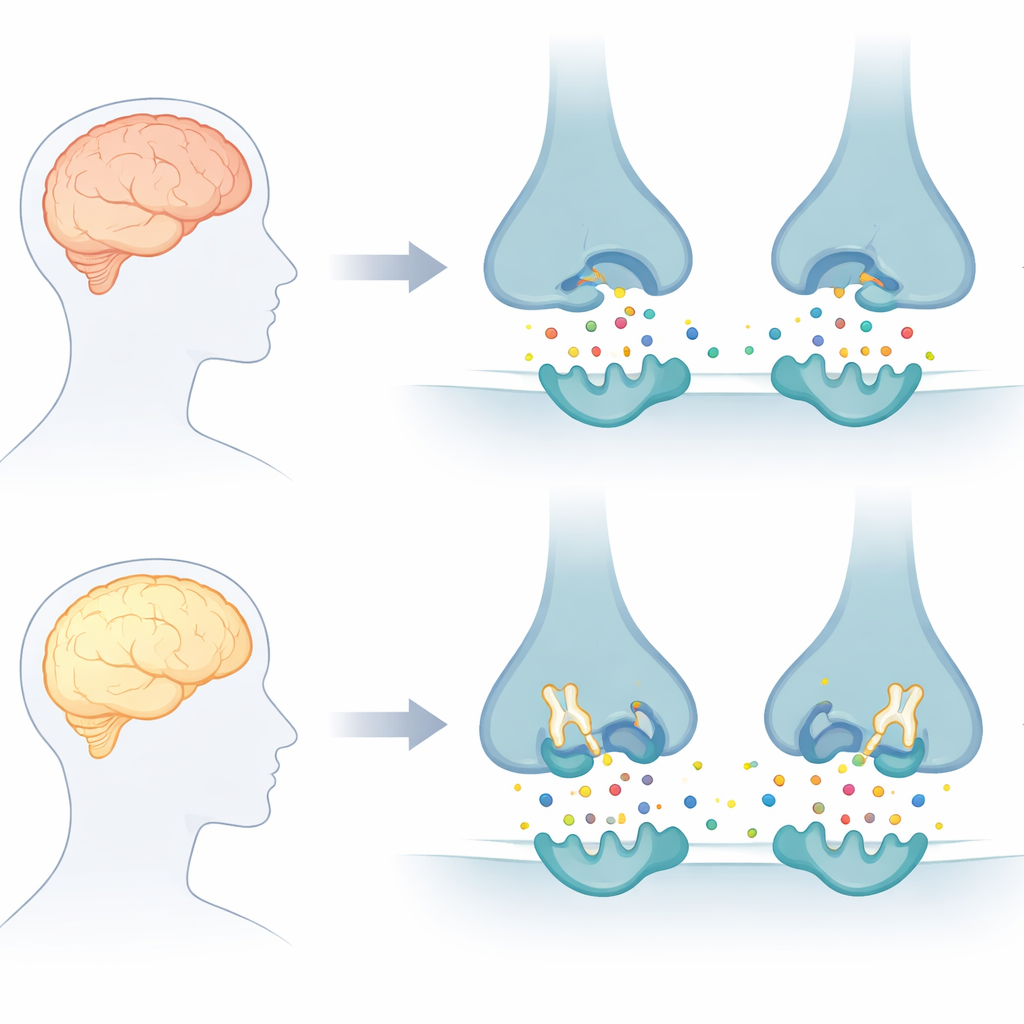
الإشارة الدماغية التي تتلاشى بسرعة كبيرة
تتواصل الخلايا الدماغية السليمة باستخدام نواقل كيميائية، ومن أهمها الأسيتيل كولين. في مرض ألزهايمر، يتم تحطيم الأسيتيل كولين بسرعة كبيرة بواسطة إنزيمين، استيل كولينستراز وبوتيرويل كولينستراز، مما يساهم في فقدان الذاكرة والارتباك. تهاجم الأدوية الحالية في الغالب إنزيمًا واحدًا فقط ولوقت محدود، ولهذا تقدم راحة عرضية قصيرة الأمد بدلاً من حماية طويلة الأمد. ركز مؤلفو هذه الورقة على تصميم مثبطات "مزدوجة" يمكنها استهداف كلا الإنزيمين معًا وقد تمنح الأسيتيل كولين فرصة أفضل لأداء وظيفته.
بناء مفتاح جزيئي أذكى
لتصميم هذه المثبطات المزدوجة، استخدم الفريق استراتيجية تسمى التهجين الجزيئي: جمعوا أجزاء من ثلاث فئات من اللبنات الكيميائية المعروفة بتفاعلها الجيد مع إنزيمات الكولينستراز. شملت هذه الأجزاء حلقة بنزيميدازول الموجودة غالبًا في الأدوية، ومجموعة سلفونات قادرة على الارتباط بقوة بمجاورات الإنزيم، وواصل هيدرازون يساعد على توصيل الأجزاء بشكل مرن. وكانت النتيجة سلسلة من المركبات ذات الصلة، المرمزة من 4a إلى 4r، والتي تم تأكيد هياكلها بعناية باستخدام تقنيات كيميائية معيارية مثل مطيافية الأشعة تحت الحمراء والرنين المغناطيسي النووي.
اختبار تثبيط الإنزيم والقدرة المضادة للأكسدة
تم فحص المركبات الجديدة أولاً في تجارب أنبوبية لمعرفة مدى قدرتها على إبطاء عمل إنزيمي الكولينستراز. أظهرت معظم أعضاء السلسلة تأثيرات تثبيط متوسطة إلى قوية، لكن خمسة منها — وهي 4b و4h و4i و4q و4r — تميزت بقدرتها على تثبيط استيل كولينستراز. عندما قاس الباحثون قيم الفعالية بدقة أكبر، طابقت عدة من هذه الجزيئات أو تفوقت حتى على دونيبيزيل، أحد الأدوية الرئيسية الموصوفة حاليًا لمرض ألزهايمر. كما فحص الفريق ما إذا كانت أفضل المثبطات قادرة على تحييد الجذور الحرة، وهي جزيئات غير مستقرة تضر بالخلايا الدماغية. أظهرت المركبات 4q و4r نشاطًا مضادًا للأكسدة قويًا عبر عدة اختبارات، مقتربة أو متفوقة على أداء مرجع مضاد الأكسدة فيتامين C.
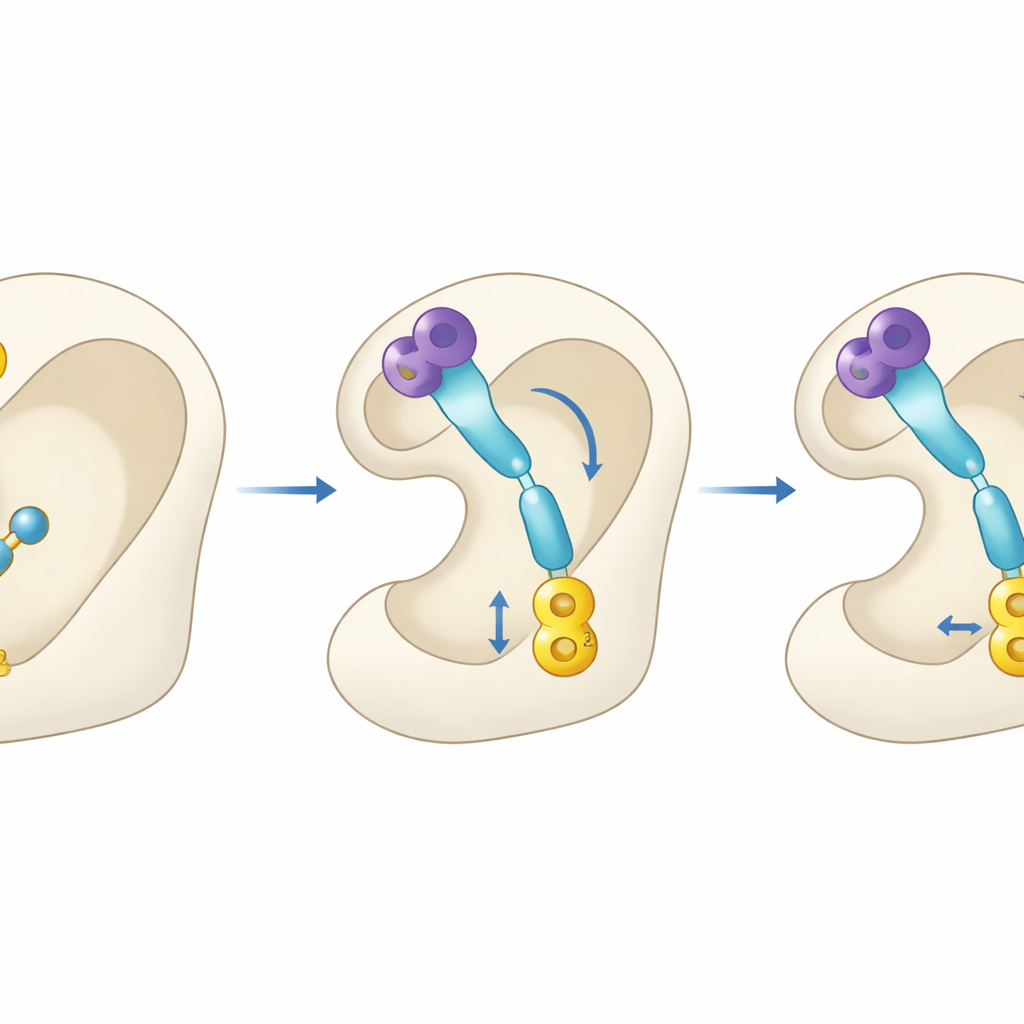
التجسس داخل قفل الإنزيم
بما أن هذه الاختبارات أُجريت خارج الجسم، لجأ العلماء إلى النمذجة الحاسوبية للتنبؤ بكيفية تصرف الجزيئات كأدوية محتملة. باستخدام أدوات محاكاة مستخدمة على نطاق واسع، قدروا خواص الامتصاص والتوزيع والتمثيل الغذائي، ثم حاكوا كيف قد تتناسب المركبات مع البنية ثلاثية الأبعاد لاستيل كولينستراز. أشارت دراسات الالتحام إلى أن جزء البنزميدازول من كل جزيء يستقر قرب فتحة الإنزيم الخارجية، بينما يصل الطرف الحامل للسلفونات عميقًا إلى المركز التحفيزي حيث يُحلل الأسيتيل كولين عادةً. ومن الملاحظ أن 4q و4r شكلا عدة تفاعلات موَلدَةٍ للاستقرار داخل جيب الإنزيم وأظهرا قوة ارتباط محسوبة أعلى من دونيبيزيل نفسه، مما يعكس أدائهما القوي في التجارب الأنبوبية.
ماذا يعني هذا لعلاجات ألزهايمر المستقبلية
تُظهر النتائج مجتمعة أن هذه الفئة الجديدة من مراكبات بنزيميدازول-ألكان سلفونات يمكنها تثبيط استيل كولينستراز بقوة، وتُظهر سلوكًا مضادًا للأكسدة ذا فائدة، وترتبط بمستهدفها الإنزيمي بطريقة تتوافق مع مبادئ تصميم الأدوية الحالية. وعلى الرغم من أن هذه الجزيئات لا تزال بعيدة عن أن تُستخدم في المرضى — فلم تُختبر بعد على حيوانات أو بشر — فإنها تقدم مخططًا واعدًا لأجيال قادمة من علاجات ألزهايمر التي تجمع بين تثبيط الإنزيم والحماية من الإجهاد التأكسدي. مع المزيد من التنقيح والاختبارات البيولوجية، قد يساهم بعض أعضاء هذه العائلة يومًا ما في أدوية تحفظ الذاكرة والتفكير بشكل أفضل في الدماغ المسن.
الاستشهاد: Omar, M.A., Al-Ashmawy, A.A.K., Abd El Salam, H.A. et al. New benzimidazole-alkanesulfonate conjugates as cholinesterase inhibitors with in vitro and in silico validation. Sci Rep 16, 8946 (2026). https://doi.org/10.1038/s41598-026-39534-z
الكلمات المفتاحية: مرض ألزهايمر, مثبطات استيل كولينستراز, مشتقات بنزيميدازول, مركبات مضادة للأكسدة, تصميم الأدوية