Clear Sky Science · ar
تأثير العلاج الكيميائي النِّئابي على وظيفة الخلايا الجذعية المتوسطة المستمدة من النسيج الدهني وتأثيراتها المعدّلة على الأرومات الليفية لدى مرضى الأورام
لماذا هذا مهم لنجاة مرضى السرطان
يعاني كثير من الأشخاص الذين خضعوا لعلاجات السرطان لاحقًا من جروح تلتئم ببطء ومضاعفات بعد الجراحة. وفي الوقت ذاته، يبحث الأطباء بشكل متزايد في طرق للاستفادة من خلايا الإصلاح المأخوذة من دهن المريض نفسه لمساعدة الأنسجة على التعافي. تطرح هذه الدراسة سؤالًا عمليًا وملحًا: بعد العلاج الكيميائي، هل تظل تلك الخلايا الإصلاحية صالحة للاستخدام، وإن لم تكن كذلك، فأي الخلايا تتأثر أكثر؟
مساعدو الجسم الخفيون في الإصلاح
لا يقتصر النسيج الدهني لدينا على مخزون للطاقة. فهو يضم مجموعة غنية من خلايا الإصلاح المتعددة الاستخدامات المسماة الخلايا الداعمة المتوسطة المشتقة من النسيج الدهني، أو AD-MSCs. هذه الخلايا لا تبقى خاملة؛ بل تفرز خليطًا من جزيئات الإشارة التي يمكن أن تهدئ الالتهاب، وتحفز تكون أوعية دموية جديدة، وتشجع الخلايا المجاورة على النمو وإعادة بناء الأنسجة التالفة. فوق النسيج الدهني، في الجلد، تعيش الأرومات الليفية — خلايا عاملة تهاجر إلى الجروح وتفرز الكولاجين، وهو البروتين الذي يوفر هيكلًا متينًا للنسيج الجديد. معًا، تساعد AD-MSCs والأرومات الليفية في تحديد مدى تعافي الجلد بعد الإصابة أو الجراحة.
اختبار خلايا إصلاح الدهون قبل العلاج وبعده
جمع الباحثون عينات صغيرة من الجلد والدهون من 66 مريضًا يخضعون للجراحة، بعضهم تلقى علاجًا كيميائيًا مسبقًا والبعض الآخر لم يتلقّه. من النسيج الدهني، عزلوا AD-MSCs وتحققوا من أن هذه الخلايا لا تزال تشبه خلايا الإصلاح الحقيقية: حملت علامات سطحية متوقعة وكان بإمكانها التمايز إلى خلايا تشبه العظم والغضروف والدهون في المختبر. ومن الجلد، عزلوا الأرومات الليفية. ثم قارن الفريق كيف نمت AD-MSCs والأرومات الليفية من مرضى تعرضت خلاياهم للعلاج الكيميائي ومن لم تتعرض لنمطية الانقسام الخلوي، وإفراز جزيئات الإشارة، والتعبير عن الجينات المرتبطة بالتئام الجروح والتجدد.
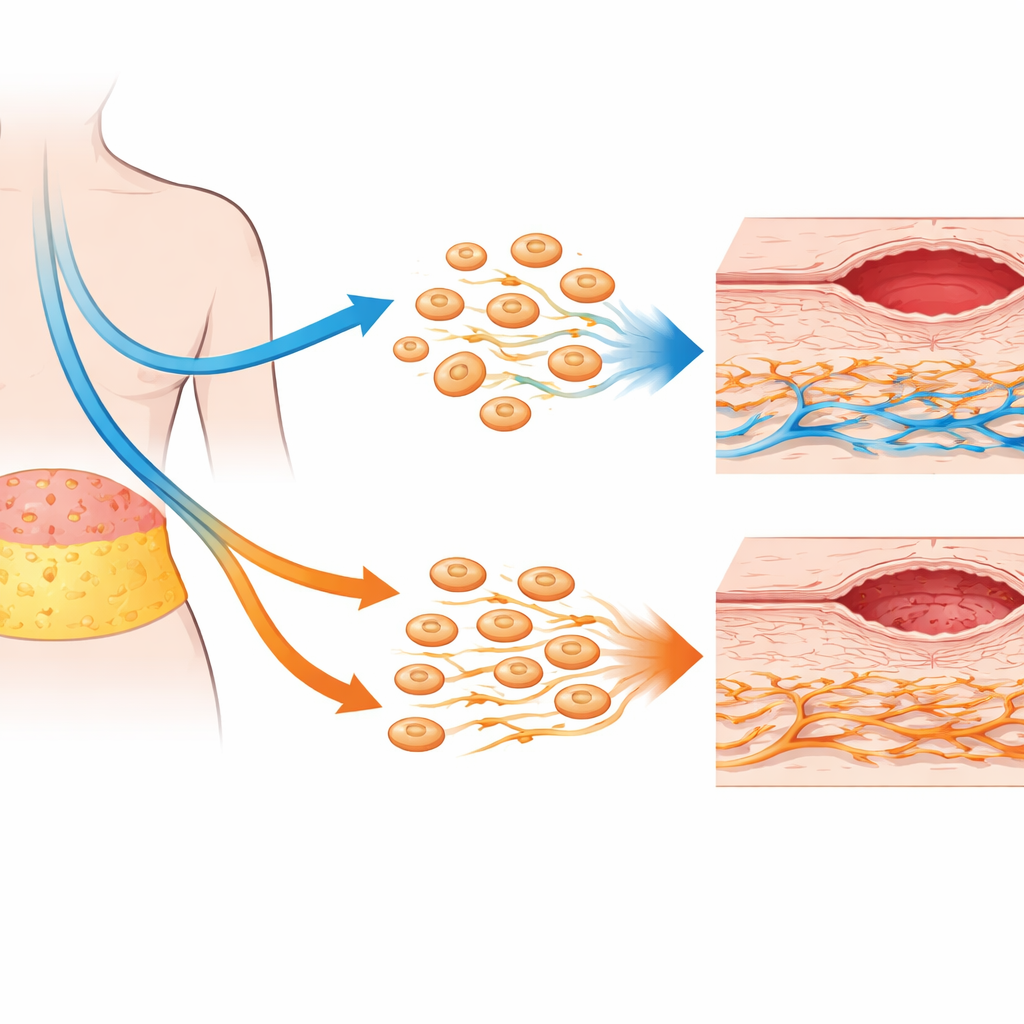
خلايا إصلاح الدهون تظل قوية بشكل مفاجئ
على عكس المخاوف من أن العلاج الكيميائي قد يضعف قدرة AD-MSCs، وجدت الدراسة أن خلايا الإصلاح المشتقة من الدهون كانت مرنة إلى حد كبير. لم تتغير علاماتها المميزة الأساسية أو نمط نموها أو نمط البروتينات الإشارية التي تفرزها بشكل جوهري بسبب العلاج الكيميائي السابق. أظهر نشاط الجينات المرتبطة بالنمو والتجديد الذاتي والتئام الجروح تغيّرات طفيفة وغير معبرة إحصائيًا. في الواقع، بدت AD-MSCs المستخرجة من مرضى عولجوا كيميائيًا أنها تتمتع بنشاط ميتوكوندري طفيف أعلى، وهو ما يشير إلى أيض أقوى بدلًا من ضرر. في تجارب التشارك في المزرعة — حيث تتشارك AD-MSCs والأرومات الليفية نفس الوسط لكن دون اتصال مباشر — استمرت AD-MSCs في تعزيز سلوكيات معيّنة لدى الأرومات الليفية، مثل الحركة الموجهة نحو إشارات الإصلاح، وخصوصًا في العينات المأخوذة من مرضى لم يتلقوا علاجًا كيميائيًا.
بناة الجلد يتحملون وطأة العلاج الكيميائي
كانت الصورة مختلفة تمامًا للأرومات الليفية. أظهرت الخلايا المأخوذة من جلد مرضى خضعوا للعلاج الكيميائي علامات واضحة على تراجع الحيوية البيولوجية. كانت قدرتها على الهجرة إلى خدش يشبه "الجرح" على طبق الاستزراع محدودة بشكل كبير، وكان إنتاجها للكولاجين أقل ميلاً. تحوّل نمط جزيئات الإشارة التي أفرزتها نحو ملف أكثر التهابيًا وأقل تجديدًا، كما انخفض تعبير العديد من الجينات المرتبطة بإشارات النمو ومستقبلاتها والإمكانات التجديدية. حتى عند تعايش هذه الأرومات الليفية مع AD-MSCs الخاصة بها في نفس الوسط، بقيت معظم وظائفها — الحركة، وإنتاج الكولاجين، والنشاط الجيني المفيد — مخفوضة مقارنة بالأرومات الليفية المأخوذة من مرضى لم يخضعوا للعلاج الكيميائي.
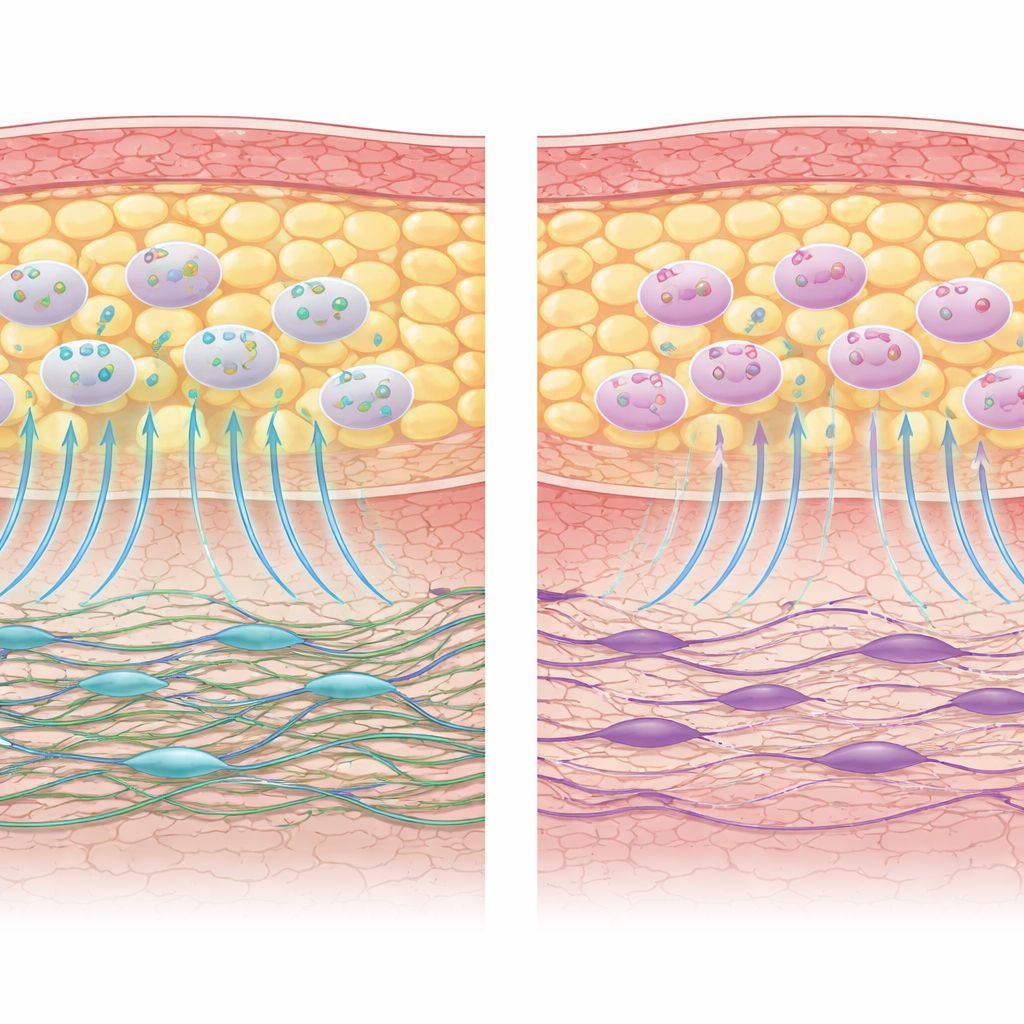
ماذا يعني هذا لعلاجات الشفاء مستقبلًا
بالنسبة للقارئ العام، تخلص هذه الدراسة إلى أن العلاج الكيميائي لا يبدو أنه يدمر مخزون خلايا الإصلاح المستمدة من الدهون في الجسم، لكنه يضعف بنّائي الجلد الأماميين — الأرومات الليفية — ويجعلهم أقل قدرة على التدخل السريع في الجروح وإعادة بناء نسيج قوي. وبما أن AD-MSCs تظل وظيفيًا سليمة، فإنها تبقى مرشحة واعدة للاستخدام في الإجراءات الترميمية، ورعاية الجروح، وزراعة الدهون بعد علاج السرطان. مع ذلك، قد يحد الوضع المتضرر للأرومات الليفية من مدى الفائدة التي يمكن أن تقدمها هذه الخلايا الشبيهة بالجذعية بمفردها. يقترح المؤلفون أن العلاجات المستقبلية قد تحتاج إلى دعم جانبي الشراكة الإصلاحية معًا: الحفاظ على صحة الأرومات الليفية أو استعادتها مع الاستفادة من AD-MSCs القوية، ومن الأفضل اختبار ذلك في نماذج أكثر تعقيدًا تشبه الجسم لتلتقط بيئة الشفاء الحقيقية لدى الناجين من السرطان.
الاستشهاد: Skoniecka, A., Słonimska, P., Tymińska, A. et al. Impact of neoadjuvant chemotherapy on the functionality of adipose-derived mesenchymal stromal cells and their modulatory effects on fibroblasts in oncology patients. Sci Rep 16, 8614 (2026). https://doi.org/10.1038/s41598-026-39457-9
الكلمات المفتاحية: العلاج الكيميائي, التئام الجروح, الخلايا الجذعية المشتقة من الدهون, الأرومات الليفية, الطب التجديدي