Clear Sky Science · ar
نموذج تعلم تحليلي مدفوع بالجينات لتشخيص سرطان الثدي بدقة
لماذا يهم هذا البحث للمرضى والعائلات
أصبح سرطان الثدي الآن أكثر أنواع السرطان تشخيصًا لدى النساء على مستوى العالم، والمرضى الذين تظهر عليهم نفس ملامح المرض على الورق قد تكون لديهم نتائج سريرية مختلفة تمامًا. تبيّن هذه الدراسة كيف أن أنماط النشاط في آلاف الجينات، مقترنة بنظام ذكاء اصطناعي مصمم بعناية، يمكن أن تساعد الأطباء على التمييز بشكل أكثر موثوقية بين الحالات السرطانية وشدتها المحتملة — باستخدام بيانات مرضى حقيقية فقط ومجموعة مضغوطة من الجينات الرئيسية.
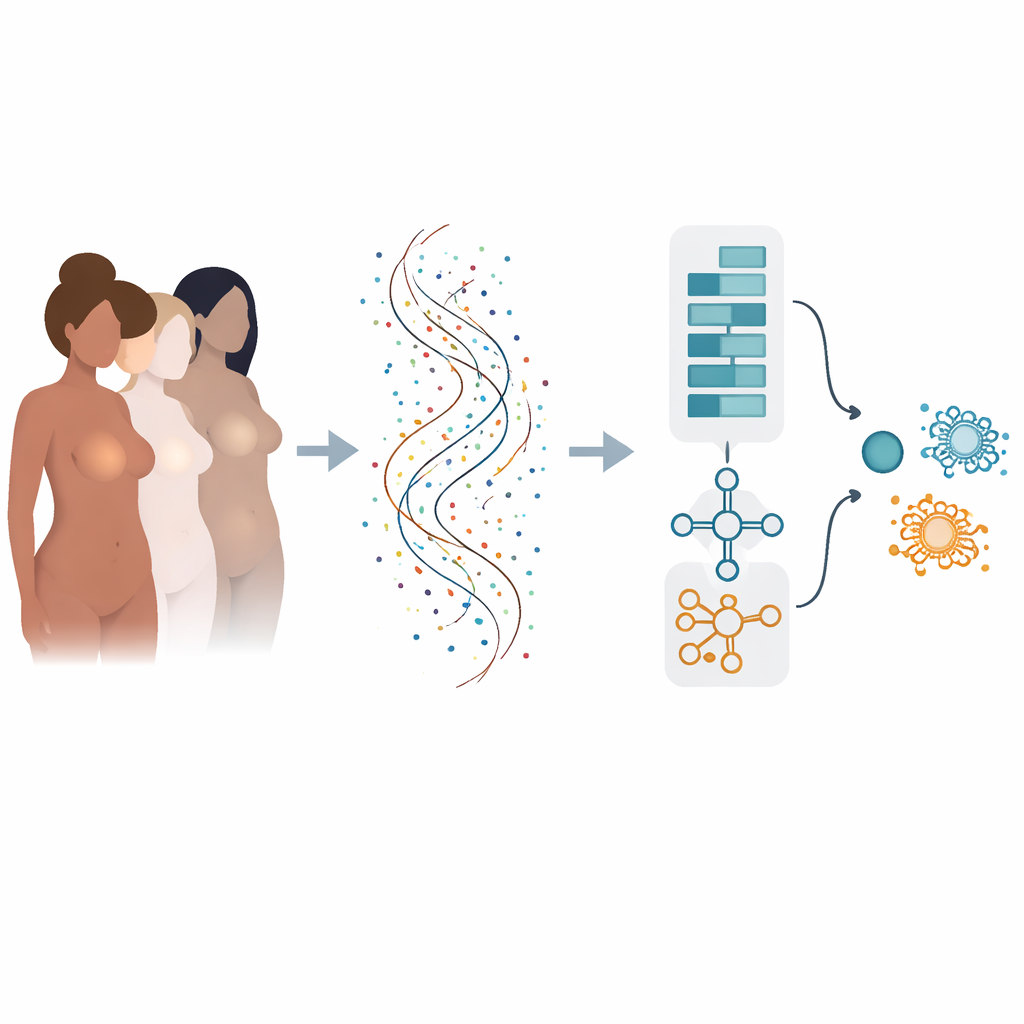
من عوامل خطر كثيرة إلى لغة الجينات
يتشكل خطر الإصابة بسرطان الثدي بفعل العديد من العوامل: تغيرات جينية موروثة، هرمونات، وزن الجسم، نمط الحياة، والمزيد. وبعد ظهور السرطان، يتحدد سلوكه بالجينات التي تُشغَّل أو تُطفأ داخل كل ورم. تتيح تقنيات التسلسل الحديثة قياس نشاط عشرات الآلاف من الجينات دفعة واحدة، لكن تحويل هذا البحر من الأرقام إلى إجابات واضحة بنعم أو لا للتشخيص والتنبؤ بالمآل يمثل تحديًا. الطرق الحاسوبية التقليدية غالبًا ما تنظر إلى الجينات واحدة تلو الأخرى وقد تغفل كيفية تفاعل مجموعات الجينات معًا، أو قد تعمل جيدًا على مجموعة بيانات واحدة وتفشل عند اختبارها في مجموعة أخرى.
تعليم نموذج ثنائي الدماغ لقراءة أنماط الجينات
بنَى المؤلفون نموذج تعلم عميق «هجيني» يعمل قليلاً مثل دماغين متخصصين يتعاونان. جزء واحد، مستوحى من تحليل الصور، يفحص قائمة مرتبة من الجينات لاكتشاف الأنماط المحلية — مجموعات من الجينات التي يشير نشاطها المشترك إلى السرطان. والجزء الآخر يتعامل مع نفس الجينات كسلسلة، متعلمًا كيف تؤثر الجينات «المدفعة» المبكرة والجينات «اللاحقة» عبر الترتيب على بعضها البعض. من خلال الجمع بين هاتين النظرتين، يستطيع النموذج التقاط العلاقات قصيرة المدى وطويلة المدى داخل البصمة الجينية للورم.
استخلاص مجموعة ثابتة من الجينات الإشارية
بدلًا من إدخال جميع 17,815 جينًا مقاسًا في النموذج، صمّم الفريق خط سير صارم «خالٍ من التسريب» لاختيار الأكثر معلوماتية فقط. باستخدام مقياس معياري للارتباط داخل حلقات تحقق متكررة، رتّبوا الجينات مرارًا حسب مدى مطابقة نشاطها لحالة السرطان. ثم احتفظوا فقط بالجينات التي صعدت باستمرار إلى القمة عبر جميع تقسيمات التدريب، مما أدى إلى توقيع مستقر مكوَّن من 236 جينًا. كما رسم الباحثون خرائط لتفاعلات هذه الجينات مع بعضها، مبينين أن العديد منها يشكل شبكات مترابطة مرتبطة بنمو الورم، الأيض، المناعة، وبيئة الأنسجة المحيطة — دليل على أن المجموعة المختارة تعكس بيولوجيا حقيقية وليس ضوضاء عشوائية.
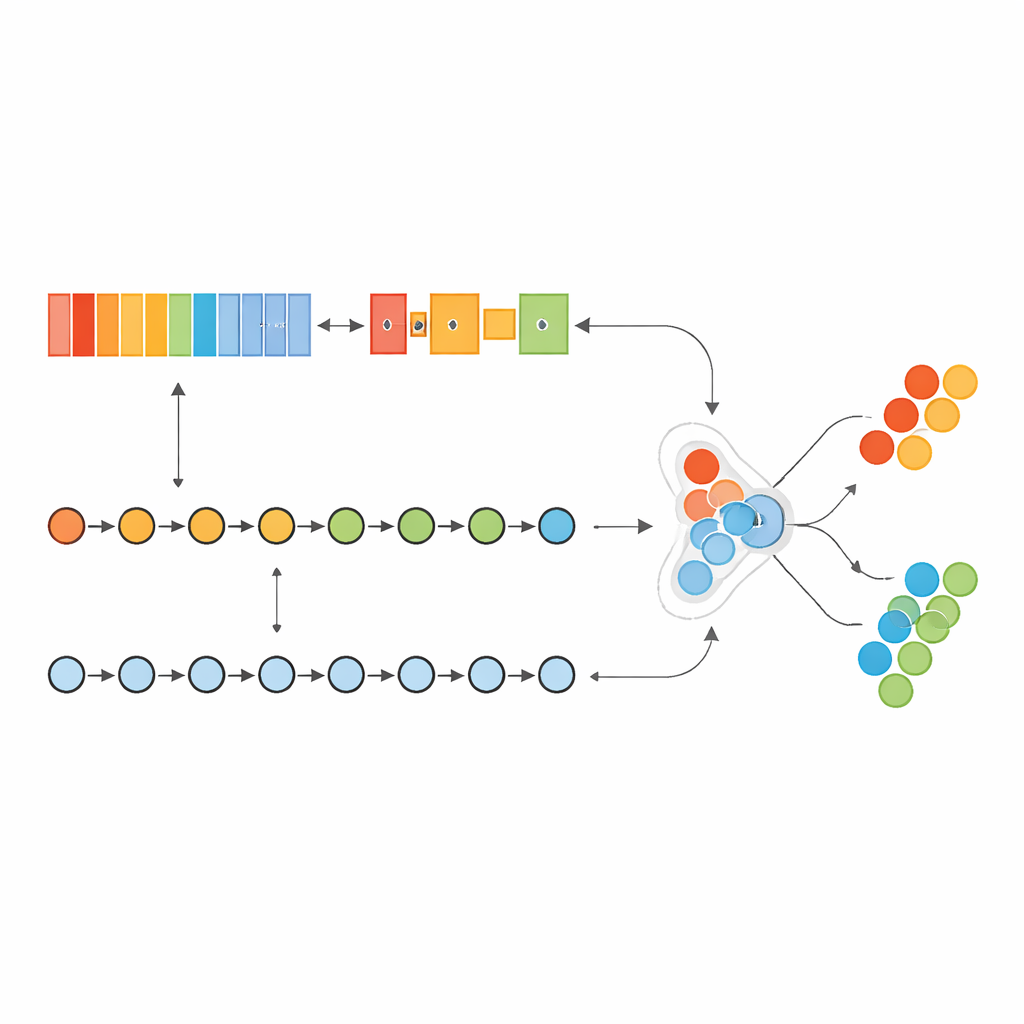
اختبار النموذج
تدرّب النظام الهجين وضُبط على عينات سرطان الثدي من مشروع أطلس جينوم السرطان (The Cancer Genome Atlas) ثم تم تحديه بمجموعة بيانات منفصلة تمامًا تُعرف باسم METABRIC. ولمعالجة حقيقة أن عينات السرطان تفوق بكثير العينات الطبيعية، لم ينشئ المؤلفون بيانات اصطناعية؛ بل ضبطوا مدى «اهتمام» النموذج بالأخطاء على الفئة النادرة. بعد بحث آلي عن الإعدادات الأفضل، حقق النموذج درجات قريبة من الكمال على مجموعة البيانات الأساسية، مُمَيِّزًا تقريبًا كل حالات السرطان بشكل صحيح ومُحدثًا عددًا ضئيلًا جدًا من التنبيهات الخاطئة. والأهم من ذلك، ظل الأداء مرتفعًا جدًا ومستقرًا عندما طُبِّق النموذج على مجموعة METABRIC الخارجية، ما يشير إلى أن النهج قد يعمم الخارج عن نطاق دراسة أو مستشفى واحد.
ما يعنيه هذا للرعاية المستقبلية
ببساطة، يقدم هذا العمل نظام ذكاء اصطناعي مُتقنًا مكوَّنًا من جزئين يقرأ رمزًا جينيًا مضغوطًا من 236 جينًا ليميّز العينات الثديية السرطانية عن غير السرطانية بدقة وثبات ملحوظين، حتى في ظروف ضوضاء عالية. ومع أن الدراسة الحالية تنظر فقط إلى نشاط الجينات وتستخدم بيانات مرضى سابقة، فإن منهجياتها تضع أساسًا لأدوات مستقبلية قد تدمج أنواع بيانات متعددة — مثل صور الأنسجة وطبقات جزيئية إضافية — وتقدم تفسيرات واضحة حول الجينات المسهمة في كل توقع. ومع مزيد من التحقق في دراسات سريرية مستقبلية استباقية، قد يصبح مثل هذا النظام عمودًا فقريًا عامًا لتشخيص سرطان الثدي بدقة، مساعدًا الأطباء على تفصيل العلاج باستخدام «توقيع» جيني مميز لكل ورم مريض.
الاستشهاد: Hesham, F., Abbassy, M.M. & Abdalla, M. Gene driven analytical learning model for accurate breast cancer diagnosis. Sci Rep 16, 8155 (2026). https://doi.org/10.1038/s41598-026-39430-6
الكلمات المفتاحية: تشخيص سرطان الثدي, تعبير الجينات, التعلم العميق, CNN-BiLSTM, طب دقيق