Clear Sky Science · ar
اكتشاف مركبات مضادة للفيروسات محتملة وتسريع اكتشاف علاجات ضد فيروس جدري القردة
لماذا يهم هذا البحث الآن
لقد تحوّل جدري القردة، الذي يُطلق عليه الآن غالبًا اسم mpox، من عدوى استوائية نادرة إلى مصدر قلق عالمي، مع تسجيل تفشيات في عدة قارات خلال السنوات الأخيرة. على خلاف كوفيد-19، لا يوجد حتى الآن دواء مصمّم خصيصًا لإيقاف هذا الفيروس. يستخدم هذا البحث أدوات حاسوبية متقدمة للبحث عن جزيئات صغيرة جديدة قد تُعطّل الفيروس في أهم نقطة: قدرته على الاختفاء من أمام جهازنا المناعي. إذا أكدت التجارب المعملية فاعليتها، فقد تصبح هذه المركبات المرشحة نقطة انطلاق لفئة جديدة من الأدوية المضادة للفيروسات.
كيف يخفي الفيروس نفسه من دفاعاتنا
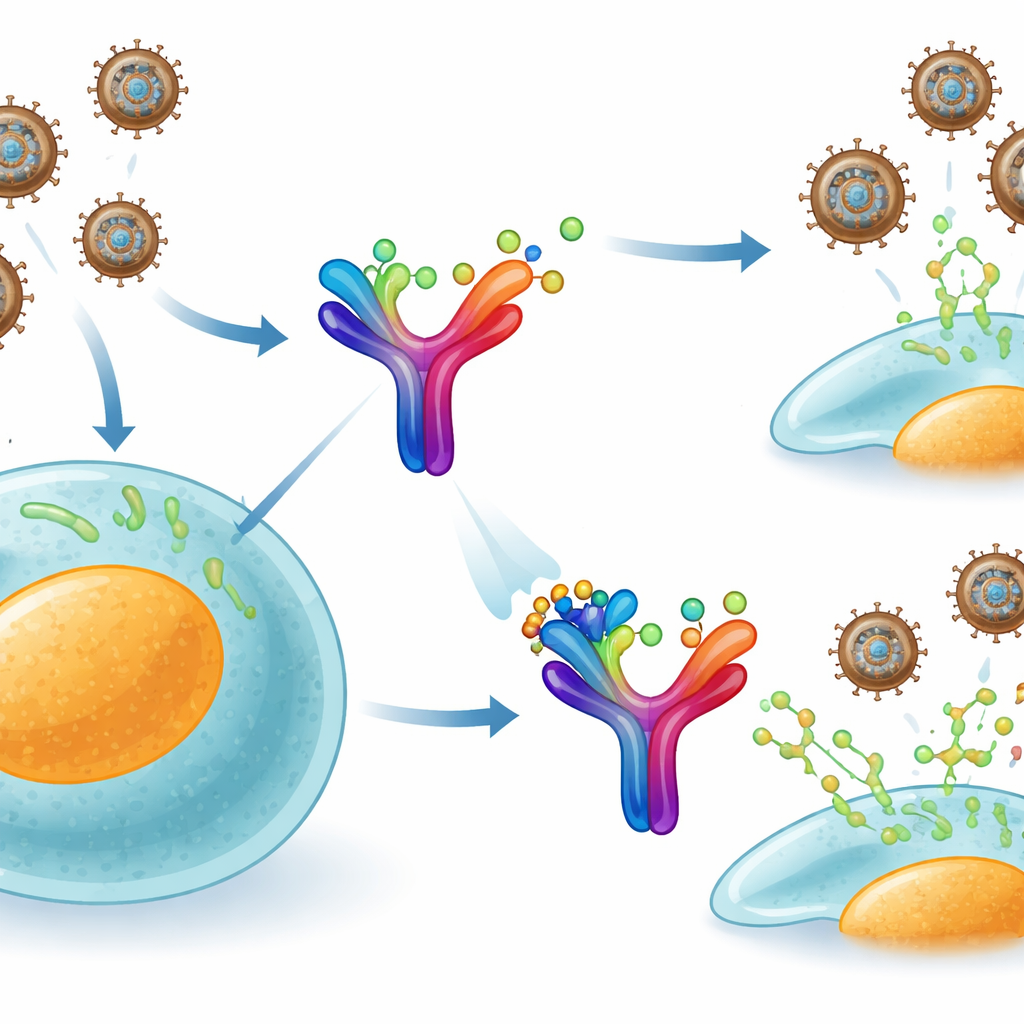
ينتمي فيروس جدري القردة إلى نفس العائلة الموسعة لفيروس الجدري، ويستخدم حيلة ذكية للتهرب من الجهاز المناعي. تُفرز خلايانا بروتينًا إشارياً يُسمى إنترفيرون-غاما، الذي ينبه الخلايا المجاورة ويشغّل دفاعات مضادة للفيروسات. لكن الفيروس يصنع بروتينًا سريًا يُفرز خارج الخلايا المصابة، يُدعى B8R، والذي يقلّد بشكل وثيق مستقبل إنترفيرون-غاما الخاص بنا ويقبض على هذه الإشارات المناعية قبل أن تصل إلى هدفها الحقيقي. بفعاليته تلك يعمل كالإسفنج، ماصًا رسائل التنبيه في الجسم ويمنع استجابه مضادة كاملة للفيروس.
استخدام الحواسيب لتصميم علاجات أذكى
قد يستغرق الاكتشاف التقليدي للأدوية سنوات عديدة ويتطلب موارد هائلة. هنا لجأ الباحثون إلى تصميم الأدوية بمساعدة الحاسوب لتسريع العملية. وبما أنه لا يوجد هيكل ثلاثي الأبعاد تجريبي لبروتين B8R، فقد استخدموا أولًا أدوات مبنية على AlphaFold للتنبؤ بشكله الذري وفحصوا جودة النموذج بعناية. وبوجود بنية ثلاثية الأبعاد موثوقة، أجروا فحصًا افتراضيًا لمكتبة تضم 5000 جزيء صغير. استُخدمت قواعد تصف ما يجعل المركب ذا خصائص دوائية (مثل الحجم والشكل والذوبانية) لترشيح المرشحين الضعيفين، مما ترك 2890 مركبًا واعدًا للاختبار التفصيلي ضد نموذج بروتين B8R.
العثور على "مفتاح" كيميائي واعد
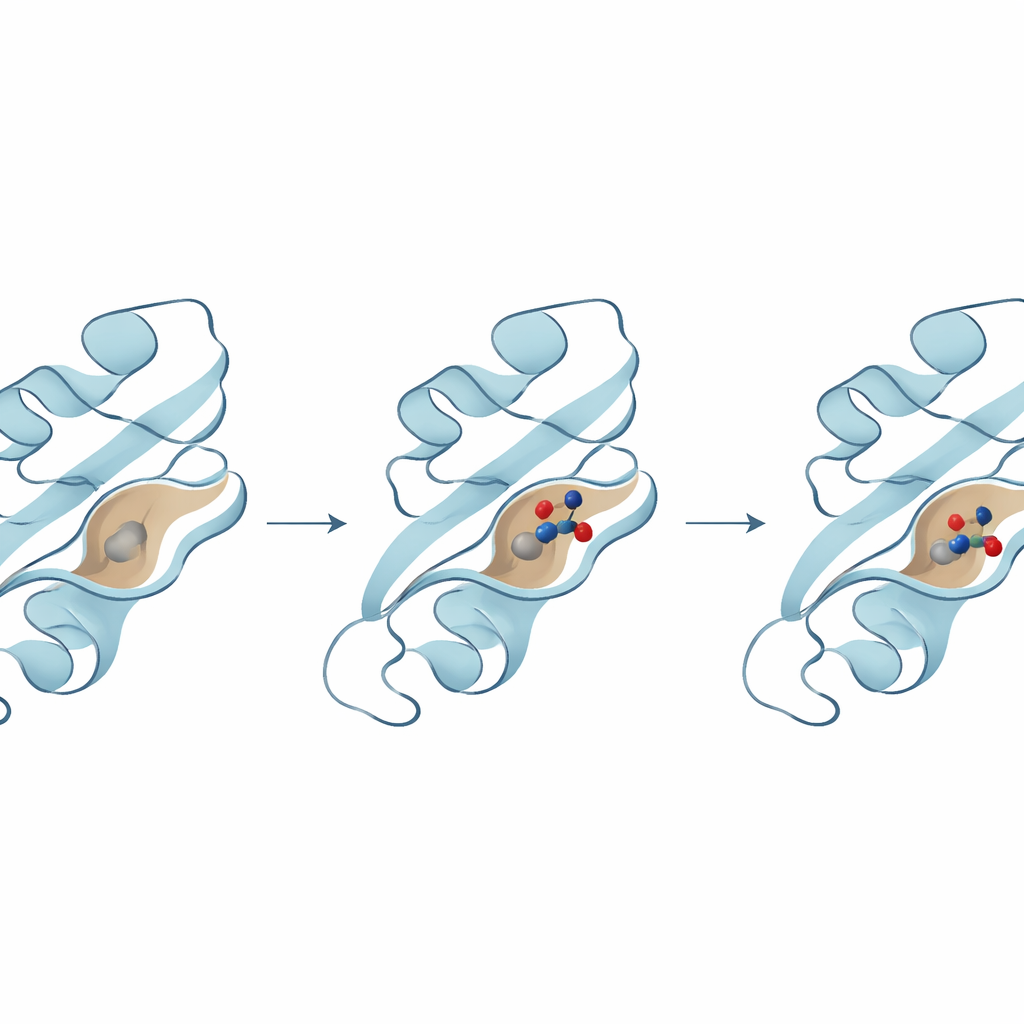
كانت الخطوة التالية اختبار أي الجزيئات يمكن أن تتناسب بإحكام داخل جيب مهم على سطح B8R، حيث يتفاعل عادةً مع إنترفيرون-غاما. استخدمت المجموعة تقنية الإرساء الجزيئي، وهي تقنية تجرب مليارات الوضعيات الممكنة لجزيء داخل جيب البروتين وتقيم مدى قوة ارتباطه. برز ثلاثة مرشحين في القمة، كل منهم توقع أن يشكل تفاعلات قوية مع أحماض أمينية رئيسية في الجيب. وأظهر أحد المركبات تحديدًا أقوى طاقة ارتباط وأقام عدة تلامسات مثبتة مع بقايا حرجة تساعد على تثبيته في مكانه، ما يوحي بأنه قد يكون فعّالًا بشكل خاص في حجب نشاط B8R.
مراقبة حركة الجزيئات عبر الزمن
البروتينات وجزيئات الأدوية ليست جامدة؛ فهي تتحرك وتنثني وتتنفس في الوسط المائي. لالتقاط هذا، أجريت محاكيات ديناميكا جزيئية طويلة — أفلام افتراضية تمتد لمئات النانوثواني — لرؤية كيف تصرف كل زوج بروتين–مركب مع مرور الوقت. كشفت هذه المحاكيات أن المركب الأفضل أداءً بقي غارقًا عميقًا في جيب B8R، مع تعدّل طفيف للبروتين حوله بينما ظل مستقرًا هيكليًا. بالمقابل، تجولت المركبان الأخريان أكثر، وانتقلا إلى جيوب بديلة أو أظهرا تقلبات أكبر، ما يشير إلى ارتباط أضعف أو أقل موثوقية. وأظهرت تحليلات إضافية للمرونة والطاقة والحركات على نطاق واسع نفس النتيجة: مركب واحد أنتج باستمرار المعقد الأكثر استقرارًا والأكثر ملاءمة طاقيًا.
ماذا قد يعني ذلك للعلاجات المستقبلية
لا يدّعي البحث أنه اكتشف دواءً نهائيًا، ولم تُجرَ بعد تجارب في الخلايا أو الحيوانات. بل يقدم نقطة انطلاق قوية مدفوعة بالبيانات: جزيء صغير محدد يبدو مُشكلًا بشكل مثالي ليقف داخل بروتين B8R الخاص بجدري القردة وقد يستعيد نظام إنذار الإنترفيرون في الجسم. عبر استهداف استراتيجية الفيروس في التملص المناعي بدلًا من آليات تكاثره، يقدم هذا النهج زاوية جديدة للعلاج المضاد للفيروسات. ويقترح المؤلفون أن المركب القيادي يجب اختباره الآن في المختبر لقياس قدرته على حجب B8R وكبح عدوى mpox مباشرة. وإذا نجحت تلك الاختبارات، قد يمهد ذلك الطريق لعلاج موجه يساعد الجهاز المناعي على رؤية الفيروس وإيقافه بفاعلية أكبر.
الاستشهاد: Ahmad, F., Navid, A., Irfan, M. et al. Discovery of potential antiviral compounds and accelerating the therapeutic discovery against monkeypox virus. Sci Rep 16, 8306 (2026). https://doi.org/10.1038/s41598-026-39427-1
الكلمات المفتاحية: مضاد جدري القردة, تملص من الجهاز المناعي, اكتشاف الأدوية, النمذجة الحاسوبية, إشارات الإنترفيرون