Clear Sky Science · ar
تحسين الخلايا الوحيدية THP-1-CAR باستخدام إشارة CD32a للبلع لتحفيز الخلايا التائية بمحددات مستهدفة
تعليم الجهاز المناعي حيل جديدة
تعيد Therapies الخلوية الحديثة برمجة الخلايا المناعية لصيد السرطان، لكن معظمها يعتمد على الخلايا التائية التي قد تواجه صعوبات في بيئة الأورام الصلبة القاسية. يتوجه هذا البحث بدلاً من ذلك إلى مدافع قوي آخر — البلعمات (البلعميات)، «آكِلات» الجسم المحترفة — ويتساءل كيف يمكن إعادة توصيلها بحيث لا تبتلع الخلايا أو الفيروسات الضارة بكفاءة أكبر فحسب، بل تستدعي أيضاً الخلايا التائية لهجوم مستمر ومحدد أكثر. تكشف الدراسة قواعد تصميم لبناء مستقبلات مُخْتَلَطة المضادّة للمستضد (CAR) أفضل للبلعمات يمكن تطبيقها على كل من العدوى مثل كوفيد‑19 والأورام الصلبة الصعبة العلاج.
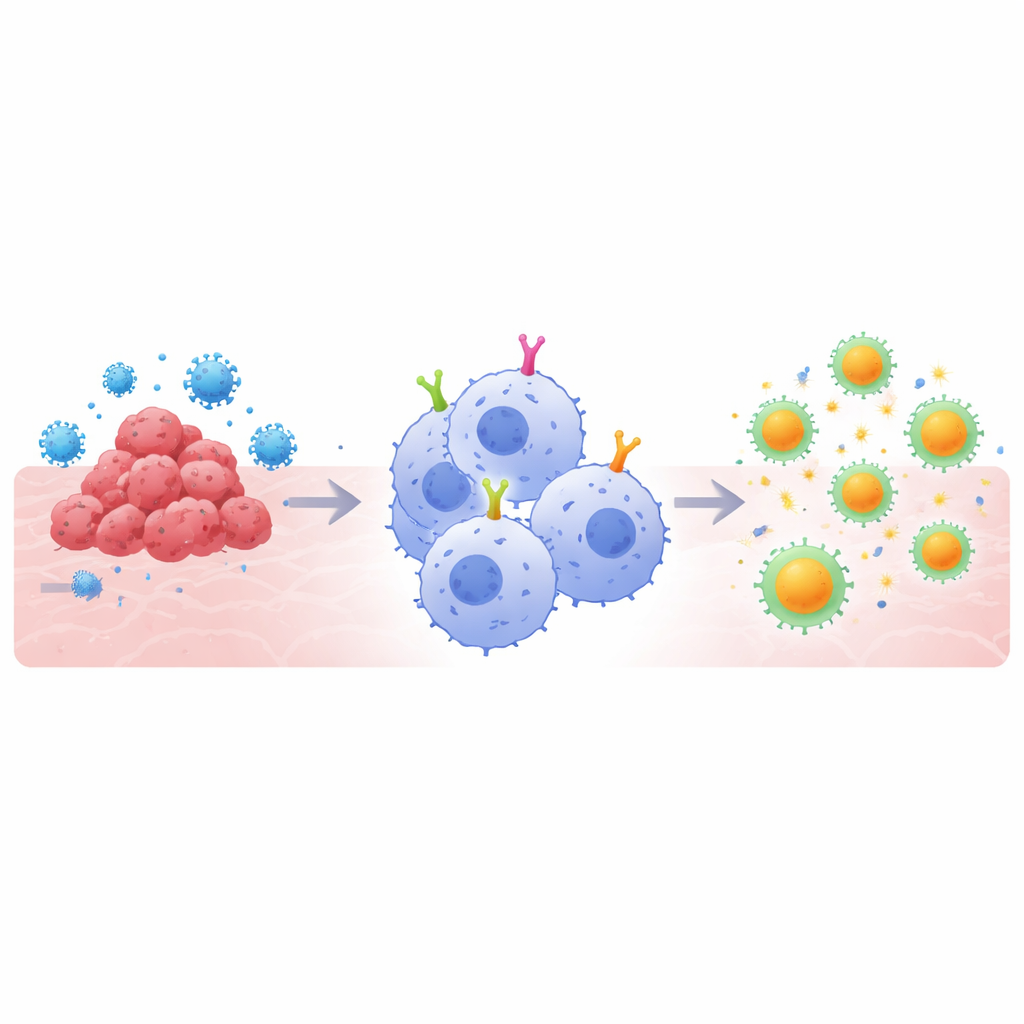
لماذا تهم خلايا «المأكولات الفائقة»
تعمل العلاجات المبنية على CAR عن طريق تزويد الخلايا المناعية بمستقبلات سطحية مُصمَّمة تتعرف على هدف محدد، مثل بروتين ورمي أو سبايك فيروسي. غير أن نسخ الخلايا التائية أحدثت تحولاً في علاج بعض سرطانات الدم، لكنها تواجه عقبات أمام الأورام الصلبة وفي بعض العدوى. تقدم البلعمات زاوية مختلفة: فهي تبتلع التهديدات طبيعياً وتفككها إلى أجزاء يمكن عرضها على الخلايا التائية، جاعلةً بذلك حلقة وصل بين فروع المناعة «الفطرية» و«المكتسبة». ومع ذلك، صُمِّمت معظم تركيبات CAR في الأصل للخلايا التائية، وليس للبلعمات. افترض المؤلفون أنه للاستفادة الكاملة من مزايا البلعمات، يجب تكييف الأجزاء الإشارية الداخلية في CAR — المقاطع التي تخبر الخلية ماذا تفعل بمجرد ارتباط الهدف — خصيصاً لتلك الخلايا الآكلة.
إيجاد أفضل توصيل داخلي للإشارة
قارن الفريق بشكل منهجي عدة مجالات إشارية داخلية داخل CARs أُدخلت في سلالة خلوية وحيدة النواة بشرية (THP‑1) يمكن تحويلها إلى بلعمات. ركزوا على مجالات مأخوذة من مستقبلات تدفع عادة البلاغة والالتهاب: CD3ζ (الوحدة التقليدية للخلايا التائية)، CD32a (مستقبل يربط الأهداف المغطاة بالأجسام المضادة)، مكونات CR3 CD11b وCD18 (مستقبلات المكمل الأساسية)، وTLR4 (مستشعر للخطر الميكروبي). باستخدام حبات وفيروسات زائفة مغطاة ببروتين سبايك لـ SARS‑CoV‑2، قيست مدى قدرة كل تصميم CAR على تمكين الخلايا من ابتلاع الأهداف، وإنتاج جزيئات التهابية، ومن ثم تنشيط خلايا CD8 التائية البشرية التي سبق أن تعرضت للفيروس. ثم نُقلت التصاميم الأكثر واعدة إلى CARs تستهدف الميسوثيلين، وهو بروتين يتم إفرازه بكثرة في العديد من الأورام الصلبة، لمعرفة ما إذا كانت نفس القواعد سارية في سياق السرطان.
بناء «مآكِلات» أفضل ومعزّزات إشارية
برز نمط واضح: قادت CARs المعتمدة على CD32a بلعاً أقوى وأسرع باستمرار مقارنة بتلك التي تستخدم المجال التقليدي CD3ζ، على الرغم من أن CD3ζ يحمل المزيد من المحفزات الإشارية التقليدية. بعبارة أخرى، كانت «ملاءمة» الإشارة مع آلية البلعمات أكثر أهمية من قوة الإشارة وحدها. لم تُضف قطع مشتقة من CR3 (CD11b أو CD18) على رأس CD32a قدرة بلع إضافية في معظم الظروف، لكنها رفعت مستويات السيتوكينات الالتهابية الرئيسية مثل TNF‑α وIL‑1β. ذهبت التركيبات المحتوية على TLR4 أبعد في تعزيز الإشارات الالتهابية ورفع علامة السطح CD86 المرتبطة بقدرة تحفيز الخلايا التائية، رغم أن ذلك صاحبه مقايضات: مستويات أقل من CAR على سطح الخلية وانخفاض طفيف في البلع.
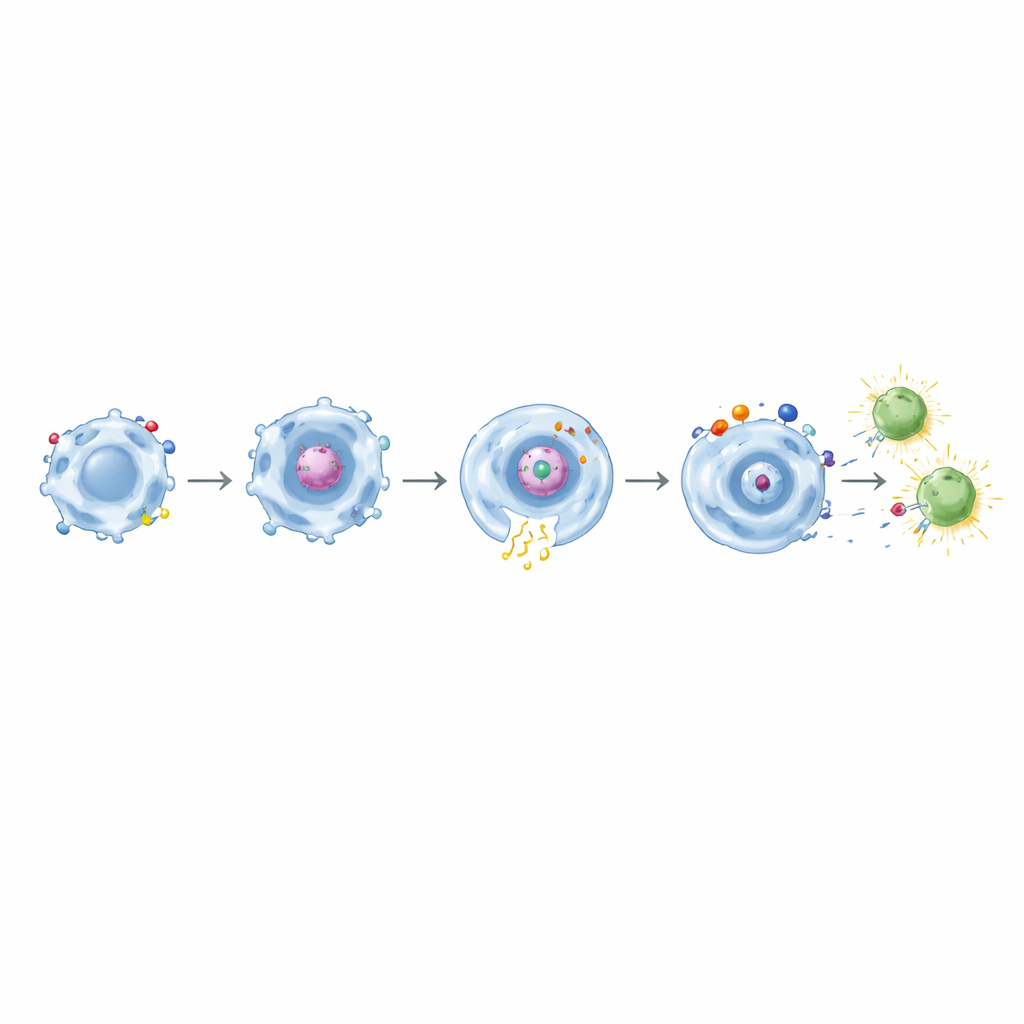
من الأكل إلى تعليم الخلايا التائية
وبشكل حاسم، بعد أن ابتلعت البلعمات الحاملة لـ CARs المعتمدة على CD32a بروتين السبايك، كانت قادرة على تنشيط خلايا CD8 التائية الذاكرية من أشخاص تم تطعيمهم سابقاً ضد كوفيد‑19. أظهرت هذه الخلايا التائية علامات تنشيط مبكرة وأنتجت جزيئات فعالة مثل الإنترفيرون‑γ وTNF‑α. ازداد التأثير قوةً مع CARs ذات المجال المزدوج التي اقترنت CD32a مع CD11b أو CD18 أو TLR4. عند اختبار تصاميم مماثلة تستهدف الميسوثيلين ضد خلايا ورمية معدّلة هندسياً، أظهرت مرة أخرى بلعاً دقيقاً معتمدًا على الهدف مصحوبًا بإشارات التهابية معززة. من بينها، تميزت مجموعة CD32a+TLR4 كـ «ناقوس نسيجي» قوي، معززة بفعالية إفراز السيتوكينات وCD86 مع الحفاظ على بلع محدد للورم.
ما الذي قد يعنيه هذا للعلاجات المستقبلية
للمراقب العادي، تُظهر هذه الدراسة أن هندسة البلعمات ليست مشكلة بحجم واحد يناسب الجميع. من خلال تبديل ودمج الوحدات الإشارية الداخلية، يمكن للعلماء تشكيل خلايا تركز إما على تنظيف فعال للخلايا المريضة أو تعمل كمكبرات مناعية تعيد تشكيل البيئة القمعية للورم وتستدعي الخلايا التائية. برزت CARs المعتمدة على CD32a كأساس قوي لمثل هذه التصاميم، متفوقة على الوحدات التقليدية الخاصة بالخلايا التائية داخل البلعمات وعاملة عبر الأهداف الفيروسية والورمية على حد سواء. على الرغم من أن هذه النتائج مستمدة من نماذج مخبرية وستحتاج إلى تأكيد في الخلايا الأولية البشرية والحيوانات، فإنها تقدم مخططًا لطرق علاجية من الجيل التالي لـ CAR macrophages قد تتعامل بشكل أفضل مع الأورام الصلبة والعدوى المستمرة عن طريق توحيد الابتلاع السريع مع تنشيط دقيق للخلايا التائية.
الاستشهاد: Hong, J., Lee, S., Kim, Y. et al. Optimization of THP-1-CAR monocytes utilizing CD32a signaling phagocytosis for antigen-specific T cell activation. Sci Rep 16, 8175 (2026). https://doi.org/10.1038/s41598-026-39406-6
الكلمات المفتاحية: الخلايا الكارِّية البلعمية (CAR macrophages), إشارة CD32a, البلع, العلاج المناعي للأورام الصلبة, تنشيط الخلايا التائية