Clear Sky Science · ar
تكامل تحليلات متعددة الأومن يحدد الجين المرتبط بضرر الحمض النووي CLSPN كعلامة حيوية في سرطان المعدة
لماذا يهم هذا البحث
يبقى سرطان المعدة من أخطر السرطانات في العالم، ويرجع ذلك جزئياً إلى أنه غالباً ما يُكتشف في مراحل متأخرة ويفتقر إلى مؤشرات إنذار مبكر موثوقة. يتعمق هذا البحث في "آثار الخدش" الجينية التي يتركها ضرر الحمض النووي، ويحدد جيناً يُدعى CLSPN كعلامة واعدة قد تساعد الأطباء على اكتشاف سرطان المعدة مبكراً، وفهم مدى عدوانيته، وربما تخصيص العلاج بدقة أكبر.
البحث عن إشارات الخطر في أورام المعدة
انطلق الباحثون من فكرة بسيطة: إذا كان ضرر الحمض النووي يساهم في دفع سرطان المعدة، فقد تحمل الجينات المشاركة في التعامل مع ذلك الضرر دلائل مهمة حول من يمرض وكيف يتطور المرض لديهم. لاختبار ذلك، جمعوا عدة مجموعات بيانات كبيرة. شملت هذه بيانات تسلسل الرنا الشامل (bulk RNA sequencing) الذي يقيس نشاط الجينات المتوسط عبر عينات الورم الكاملة؛ وتسلسل الرنا على مستوى الخلية الواحدة، الذي يفحص آلاف الخلايا الفردية واحدة تلو الأخرى؛ ونقل المواضع التعبيري (spatial transcriptomics) الذي يعيد خريطة نشاط الجينات إلى شريحة النسيج. كما جمعوا قائمة مطولة من الجينات المرتبطة بالفعل بضرر الحمض النووي. باستخدام هذه الموارد، تحققوا أي الجينات المرتبطة بضرر الحمض النووي ترتبط أكثر بسرطان المعدة وببقاء المرضى على قيد الحياة.
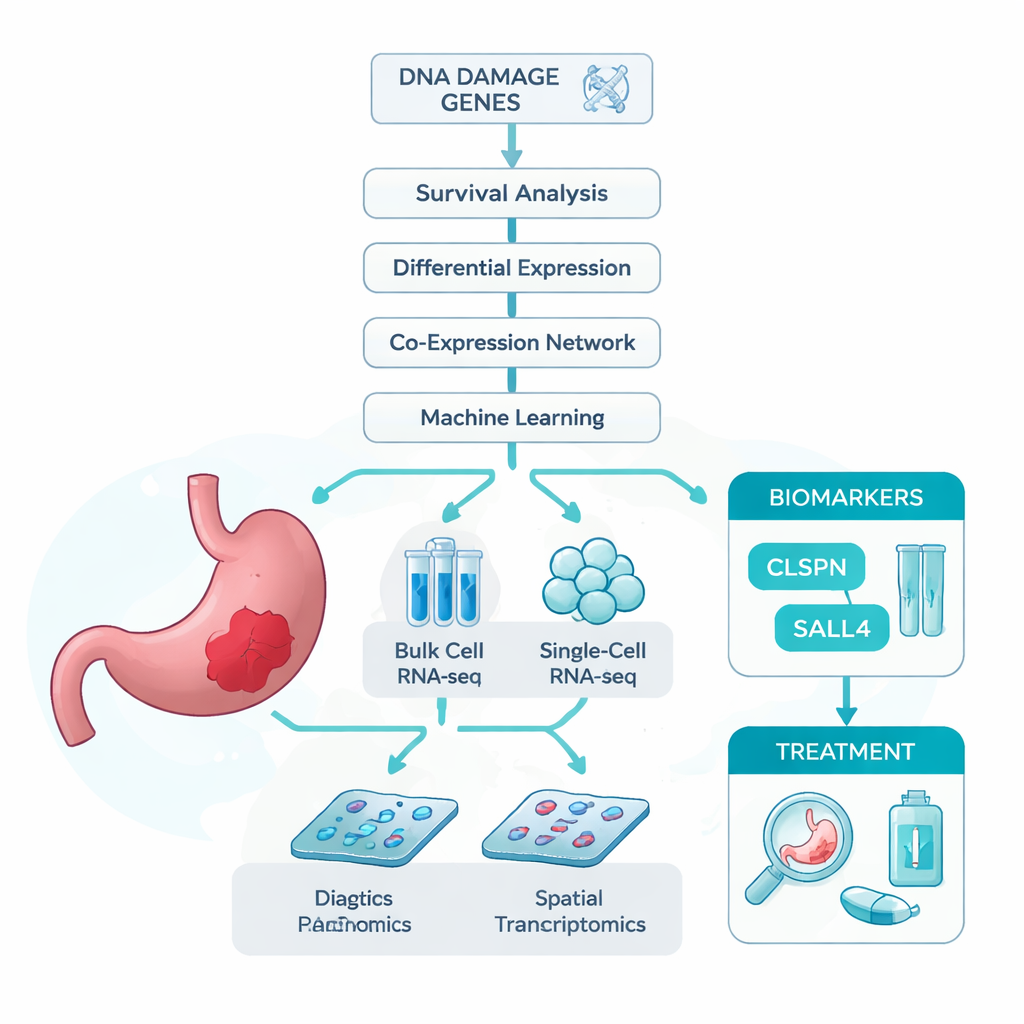
استخدام خوارزميات ذكية للعثور على الجينات الرئيسية
نظراً لأن آلاف الجينات تتغير في السرطان، لجأ الفريق إلى مجموعة من الأدوات الإحصائية وتعلم الآلة لتضييق المجال. أولاً قاموا بترشيح الجينات التي كانت مُنظَّمة بشكل خاطئ في الأورام وكانت مرتبطة بوضوح بزمن بقاء المرضى. ثم جمعوا الجينات حسب سلوكها المشترك في الارتفاع والانخفاض، وراجعوا ذلك مع قائمة جينات ضرر الحمض النووي. أنتج هذا الفحص متعدد المراحل 13 جيناً مرشحاً قوياً. ولمعرفة أي هذه الجينات كانت الأكثر أهمية لتمييز الورم عن النسيج الطبيعي، دربوا سبعة نماذج مختلفة من تعلم الآلة، كل منها يقوم بترتيب الجينات حسب فائدتها للتصنيف. عبر كل النماذج، برزا جينان—CLSPN وSALL4—بشكل متكرر، مع دقة تقارب أو تفوق 97% ومساحات تحت منحنى ROC تفوق 0.96، مما يشير إلى أن لهذه الجينات إمكانات تشخيصية ممتازة.
التركيز على CLSPN داخل الورم
من بين الجينين القياديين، تميّز CLSPN كالأكثر إفادة إجمالاً، لذا فحصه المؤلفون بمزيد من التفصيل. في بيانات الخلية الواحدة التي شملت أكثر من 30,000 خلية، كان CLSPN أكثر نشاطاً بكثير في خلايا الورم منه في الخلايا الطبيعية المجاورة أو الخلايا المساندة، ما يشير إلى دور مخصص للورم. أظهرت الخرائط المكانية لمقاطع الأنسجة المرضية نمطاً مماثلاً: تركز تعبير CLSPN في مناطق اعتبرها الأطباء المرضيون مناطق سرطانية. عندما قسم الفريق خلايا الورم إلى مجموعات "ذات CLSPN مرتفع" و"ذات CLSPN منخفض"، أظهرت المجموعة المرتفعة نشاطاً أقوى في المسارات المرتبطة بنسخ الحمض النووي والانقسام الخلوي والإصلاح—عمليات يمكن أن تغذي النمو غير المنضبط عند فرط نشاطها أو انحرافها. أشارت تحليلات الزمن الكاذب (pseudotime)، التي تعيد بناء كيفية تغير الخلايا على خط زمني مفترض، إلى أنه مع تقدم خلايا الورم، تميل مستويات CLSPN إلى الارتفاع، مما يوحي بأن زيادة تنظيم CLSPN قد تكون جزءاً من التحول نحو حالة أكثر خبيثة.
روابط بالجهاز المناعي واستجابة العلاج
استكشفت الدراسة أيضاً كيف يرتبط CLSPN بمحيط الورم وبالعلاجات المحتملة. أظهرت الأورام ذات التعبير الأعلى عن CLSPN تركيبات مختلفة من الخلايا المناعية، لا سيما البالعات والخلایا التائية وبعض خلايا NK، مما يوحي بأن CLSPN قد يساهم في تشكيل بيئة مثبطة للمناعة. أشارت نماذج حساسية الأدوية إلى أن السرطانات ذات CLSPN الأعلى قد تكون أكثر عرضة لعدة كيماويات وعوامل مستهدفة، إذ رُبطت مستويات CLSPN الأعلى بجرعات متوقعة أقل مطلوبة لكبح النمو. والمهم أنه عندما صبغ المؤلفون عينات نسيجية فعلية من 70 مريضاً، كانت مستويات بروتين CLSPN أعلى بوضوح في السرطان مقارنة بالمعدة الطبيعية وارتبطت بأورام أكبر، تغلغل أعمق، انتشار إلى الغدد اللمفاوية، وبقاء عام أقصر.
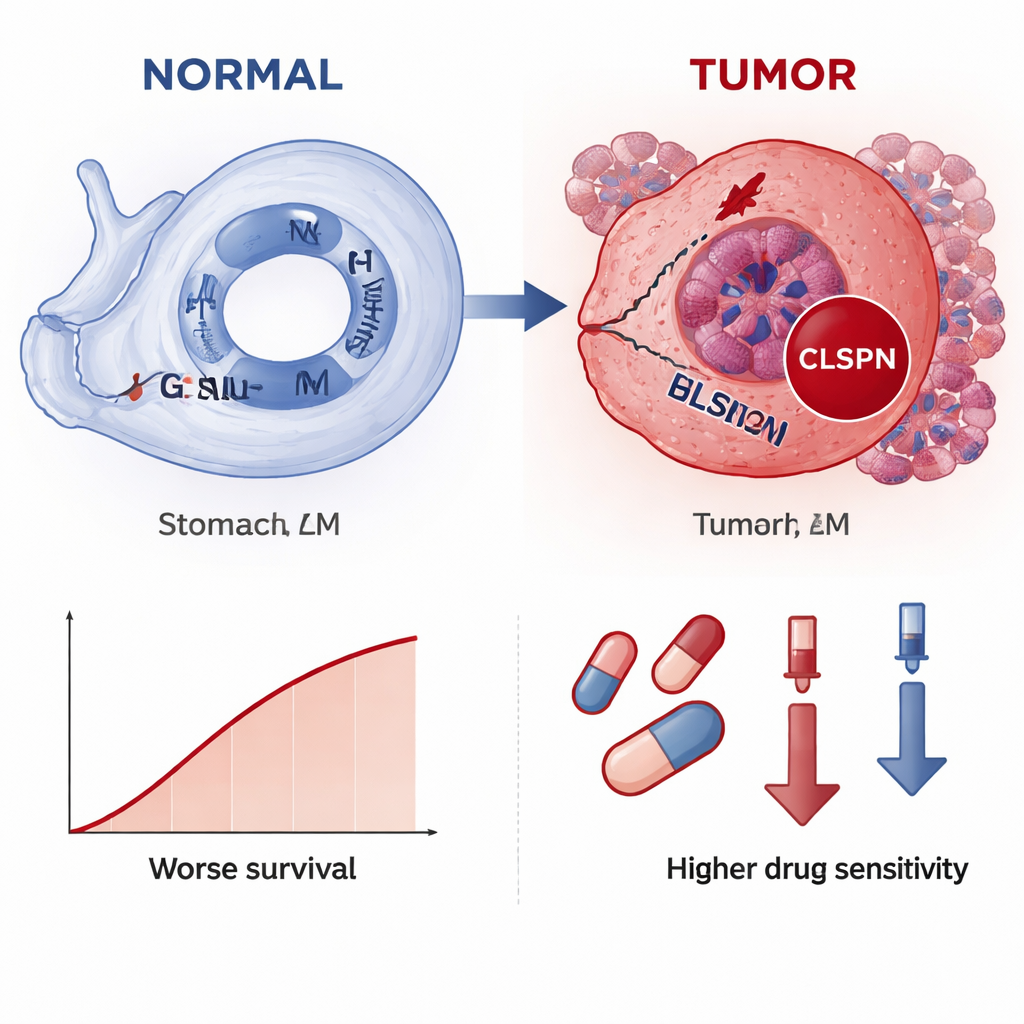
ما قد يعنيه هذا للمرضى
بعبارات بسيطة، تشير الدراسة إلى أن CLSPN يتصرف كضوء تحذير أحمر لسرطان المعدة: يشتغل في الغالب في خلايا الورم، يزداد لمعانه في المرض المتقدم، ويشير إلى مخاطر أعلى لنتائج سلبية. وبما أنه يمكن الكشف عنه على مستوى الرنا وأيضاً بطرق التلوين القياسية في المستشفى، قد يصبح CLSPN علامة حيوية عملية تساعد الأطباء المرضيين على تأكيد سرطان المعدة، وتصنيف المرضى حسب الخطر، وربما توجيه اختيار الأدوية. بينما هناك حاجة لمزيد من الاختبارات السريرية قبل اعتماده روتينياً، يبرز هذا العمل كيف أن قراءة آثار ضرر الحمض النووي عبر طبقات بيانات متعددة يمكن أن تكشف أدوات جديدة للتشخيص المبكر وعلاج أكثر تفصيلاً لسرطان المعدة.
الاستشهاد: Ma, Q., Yang, X., Sun, N. et al. Integrating multi-omics analysis identifies DNA damage-related gene CLSPN as a biomarker in gastric cancer. Sci Rep 16, 7789 (2026). https://doi.org/10.1038/s41598-026-39387-6
الكلمات المفتاحية: سرطان المعدة, ضرر الحمض النووي, CLSPN, علامة حيوية, تحليل الخلية الواحدة