Clear Sky Science · ar
علم السمية الشبكي التكاملي والدلائل التجريبية تكشف الآليات الكامنة وراء بدء وتقدم سرطان بطانة الرحم الناجم عن ثنائي إيثيل الفثالات
الكيماويات اليومية وخطر السرطان لدى النساء
ملدنات البلاستيك متغلغلة في حياتنا المعاصرة، وتظهر في التغليف ومستحضرات التجميل والأجهزة الطبية. أحد هذه المواد، ثنائي إيثيل الفثالات (DEP)، منتشر إلى حد يمكن من خلاله اكتشاف نواتجه المتحللة في بول معظم الأشخاص. في الوقت نفسه، ترتفع معدلات سرطان بطانة الرحم — وهو سرطان يصيب بطانة الرحم — على مستوى العالم. تطرح هذه الدراسة سؤالاً ذا أولوية لأي شخص يهتم بالصحة البيئية: هل يمكن أن يساهم التعرض طويل الأمد لـ DEP بهدوء في دفع خلايا الرحم نحو السرطان، وإذا كان الأمر كذلك فبأي آلية؟
كيف ربطت الدراسة التعرض بالمرض
بدأ الباحثون بتعدين قواعد بيانات عامة ضخمة تحتوي على ملفات نشاط الجينات من أنسجة سرطان بطانة الرحم والأنسجة الطبيعية لبطانة الرحم. بمقارنة آلاف الجينات دفعة واحدة، حدَّدوا أي الجينات كانت أكثر أو أقل نشاطًا بشكل متكرر في السرطان. ثم تقاطعوا مع خريطة ثانية: قائمة بالجينات البشرية التي تقترح قواعد بيانات كيميائية وأدوات تنبؤية سابقة أنها قد تتفاعل مع DEP. حيثما تداخلت الخريطتان وجدوا 19 جينًا تقع عند تقاطع التعرض لـ DEP وسرطان بطانة الرحم، مما يوحي بوجود رابط آلي بين مادة كيميائية يومية وتكون الورم.
خوارزميات ذكية لإيجاد الجينات الأكثر أهمية
يزال فرز 19 جينًا مرشحًا مهمة صعبة، لذا لجأ الفريق إلى التعلم الآلي. دربوا واختبروا أكثر من 100 نموذج تنبؤي مختلف على مجموعات بيانات مرضى مجتمعة ليروا أي مجموعات الجينات يمكنها التمييز بين نسيج السرطان والنسيج الطبيعي بأفضل شكل. باستخدام طريقة تفسيرية تُدعى SHAP، التي تكشف مقدار كل جين في دفع التنبؤ نحو حالة السرطان أو الصحية، رتّبوا المرشحين. برزت خمسة جينات — FOS وJUN وNR4A1 وADRA2C وSLC6A2 — كمحاور رئيسية، إذ أظهر كل منها قدرة قوية على فصل العينات السرطانية عن غير السرطانية بشكل منفرد، ومعًا شكّلوا بصمة للتغيرات المرتبطة بـ DEP في بطانة الرحم.
التدقيق في لقاءات المادة الكيميائية بالبروتين
للبحث فيما إذا كان DEP يمكن أن يرتبط فعليًا بالبروتينات الناجمة عن هذه الجينات، استخدم الباحثون الإرساء الجزيئي ومحاكاة حاسوبية طويلة لحركة الذرات. اقترحت هذه التحليلات أن DEP يتناسب مع جيوب على عدة من هذه البروتينات، لا سيما ADRA2C وNR4A1 وSLC6A2، مكوّنًا مركبات مستقرة عبر الزمن. لا تثبت مثل هذه التجارب الافتراضية السببية من تلقاء نفسها، لكنها تعزز الفكرة القائلة إن DEP قادر على الالتصاق مباشرة ببروتينات تحكم رئيسية داخل الخلايا الرحمية أو على سطحها، مما قد يحرّك سلوكها بطرق تفضّل نمو الورم.
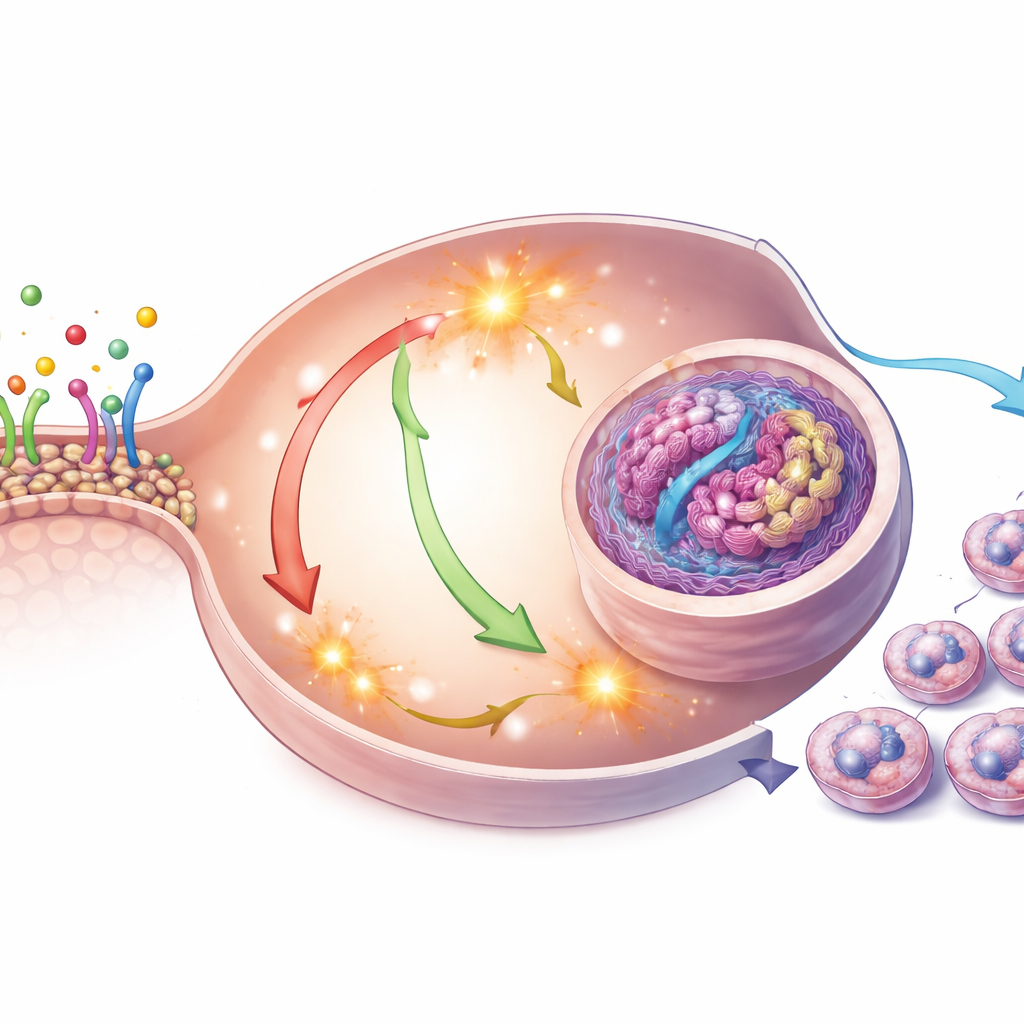
ما الذي يحدث داخل خلايا الرحم
انتقل الفريق من النماذج الحاسوبية إلى الخلايا الحية، حيث عرضوا سلسلتي خلية بشريتين سرطانيتين لبطانة الرحم لـ DEP بجرعات اختيرت لتكون حيوية الفعالية دون أن تكون سامة فورًا. وجدوا أن الخلايا المعالجة بـ DEP تكلّمت أسرع ودخلت طور نسخ الحمض النووي في دورة الخلية بسهولة أكبر. داخل هذه الخلايا ارتفعت مستويات أنواع الأكسجين التفاعلية — وهي أشكال أكسجينية ذات نشاط كيميائي عالٍ — بينما انخفض إنزيم مضاد للأكسدة طبيعي. في الوقت نفسه، ازدادت نشاطات مسارات التحكم بالنمو داخل الخلية، المعروفة غالبًا باسم MAPK/ERK وPI3K/AKT. تزامن هذا التنشيط مع زيادة في Cyclin D1 وCDK4، وهما بروتينان يعملان كحراس بوابات يدفعان الخلايا من حالة السكون إلى الانقسام النشط.
مغزى ذلك في الحياة اليومية
بالتجميع، ترسم الدراسة صورة متعددة الطبقات: يمكن أن يرتبط DEP ببروتينات خلوية محددة، ويطلق الإجهاد التأكسدي، ويشغّل دوائر إشارات تُعزّز النمو، ويسرّع دورة الخلية في خلايا سرطان بطانة الرحم. للقراء غير المتخصصين، الرسالة أن مادة مضافة شائعة للبلاستيك لديها القدرة على جعل بطانة الرحم أكثر «أرضًا خصبة» للسرطان، خاصة في جسد يتأثر بالفعل بالهرمونات وعوامل الخطر الأخرى. مع أن العمل أُجري في نماذج خلوية ويحتاج إلى تأكيد في حيوانات وبشر، إلا أنه يؤكد أهمية التدقيق في التعرضات الكيميائية الروتينية ويدعم الجهود الرامية إلى تقليل التعرض لمواد معطلة للغدد الصماء غير الضرورية.
الاستشهاد: Chen, X., Wang, Z., Wang, F. et al. Integrative network toxicology and experimental evidence reveal mechanisms underlying diethyl phthalate-induced initiation and progression of endometrial cancer. Sci Rep 16, 8066 (2026). https://doi.org/10.1038/s41598-026-39325-6
الكلمات المفتاحية: سرطان بطانة الرحم, ثنائي إيثيل الفثالات, مُعطِلات الغدد الصماء, علم السموم البيئي, إشارة خلوية