Clear Sky Science · ar
نموذج فيزيائي بوليمري لنواة الخلية بين الطور لمحاكيات التأثيرات الإشعاعية البيولوجية
لماذا يهم شكل موطن الحمض النووي لدينا
الإشعاع سيف ذو حدين في الطب: يمكنه قتل خلايا السرطان، لكنه قد يضر أيضاً الأنسجة السليمة. في جوهر كل من المخاطر والفوائد يكمن الحمض النووي، المصفوف بإحكام داخل نواة الخلية. توضح هذه الورقة كيف أن نموذجاً ثلاثي الأبعاد مفصلاً مستوحى من الفيزياء ل"مدينة الحمض النووي" النووية يمكن أن يساعد العلماء على التنبؤ بكيفية تكسر الكروموسومات وسوء إصلاحها بعد الإشعاع، مما قد يحسن علاج السرطان وتقديرات مخاطر الإشعاع في الفضاء.
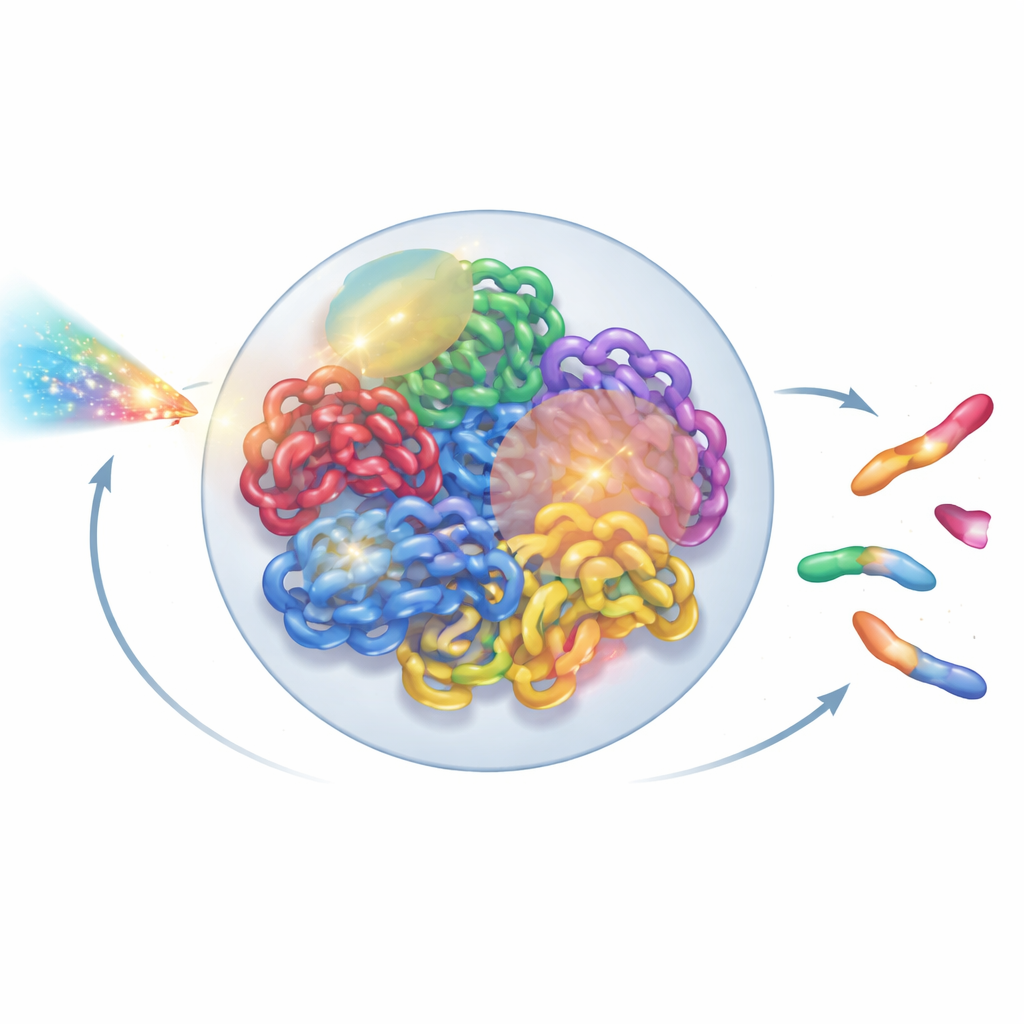
رؤية الجينوم كبنية حية
داخل كل خلية بشرية، يتم طي مترين من الحمض النووي إلى نواة صغيرة لا يتجاوز قطرها بضعة ميكرومترات. هذا الطي ليس عشوائياً: كل كروموسوم يميل إلى احتلال مناطقه الخاصة، والتي تنقسم بدورها إلى أحياء ومجالات حلقية. كشفت أدوات تجريبية جديدة، مثل المجهر فائق الدقة وخرائط اتصال Hi-C، عن هذا التوزيع ثلاثي الأبعاد بتفصيل ملحوظ. ومع ذلك، ما تزال معظم نماذج التأثير الإشعاعي تتعامل مع الحمض النووي كتشابك مبسّط من الخطوط أو حلقات مثالية، متجاهلة هذا التنظيم عالي المستوى. سعى المؤلفون لبناء نموذج لنواة كاملة يحترم ما تعلمه علماء الأحياء عن بنية الكروماتين الحقيقية، وفي الوقت نفسه يكفي أن يكون سريعاً ليعمل على حواسب المختبر الاعتيادية.
بناء نواة افتراضية باستخدام فيزياء البوليمرات
نمذج الفريق الكروموسومات كسلاسل مرنة، مستعيراً أفكاراً من فيزياء البوليمرات، وهو المجال نفسه المستخدم لفهم البلاستيك والمواد اللينة. قسموا المشكلة إلى ثلاث مراحل استرخاء للسيطرة على التكلفة الحسابية الهائلة. أولاً، وضعوا كتل بناء كبيرة تُسمى مجالات الكروماتين في أنحاء النواة، مع السماح لها بأن تتنافر مع بعضها، وتمتد على طولها، وتتجمع إلى متباينات فرعية أوسع. ثانياً، قاموا بالتكبير داخل كل مجال لتمديد ألياف الكروماتين الأرفع، بما في ذلك المناطق الحلقيّة المرتبطة بواسطة بروتينات ربط. ثالثاً، سمحوا لجميع الألياف بالتفاعل بحرية مرة أخرى داخل حدود النواة للوصول إلى تكوين نهائي واقعي. بتقسيم العملية بهذه الطريقة وإضافة بحث هرمي وحيل الحوسبة الموازية، خفضوا زمن التشغيل من أربعة أشهر غير عمليين إلى حوالي ثلاث ساعات لكل نواة افتراضية على محطة عمل ذات 64 نواة معالجة.
من مسارات الإشعاع إلى كسور وإصلاحات الحمض النووي
بمجرد بناء النواة الافتراضية، وضع المؤلفون فوقها مسارات إشعاعية مفصلة مُولَّدة بواسطة محاكيات Geant4-DNA. استخدموا بحثاً هرمياً لإيجاد، لكل حدث تأين، أي مجال كروماتين وأي مقطع ليفي، وفي النهاية أي نوكليوتيد كان الأقرب، دون تخزين مواقع جميع النوكليوتيدات العشرة مليار في الذاكرة. بدلاً من ذلك، احتفظوا بقالب كروماتين قابل لإعادة الاستخدام وطبقوا تحولات إحداثيات ذكية أثناء التنفيذ. عاملوا التأينات في العمود الفقري للحمض النووي على أنها كسور سلسلة، والكسور القريبة على الشعيرات المقابلة اعتُبرت كسوراً مزدوجة الشريط. لمحاكاة آلية إصلاح الخلية، أدخل المؤلفون قاعدة إعادة ربط مبنية على المسافة: النهايات الحرة للحمض النووي التي تقع بالقرب من بعضها أكثر عرضة لأن تعاد ربطها. اتُخذت قرارات الربط خطوة بخطوة حتى تُزاوج كل النهايات أو تُترك غير مُصلَحة، مما أعاد تكوين كل من الإصلاحات الصحيحة والشظايا الملتصقة بشكل خاطئ.
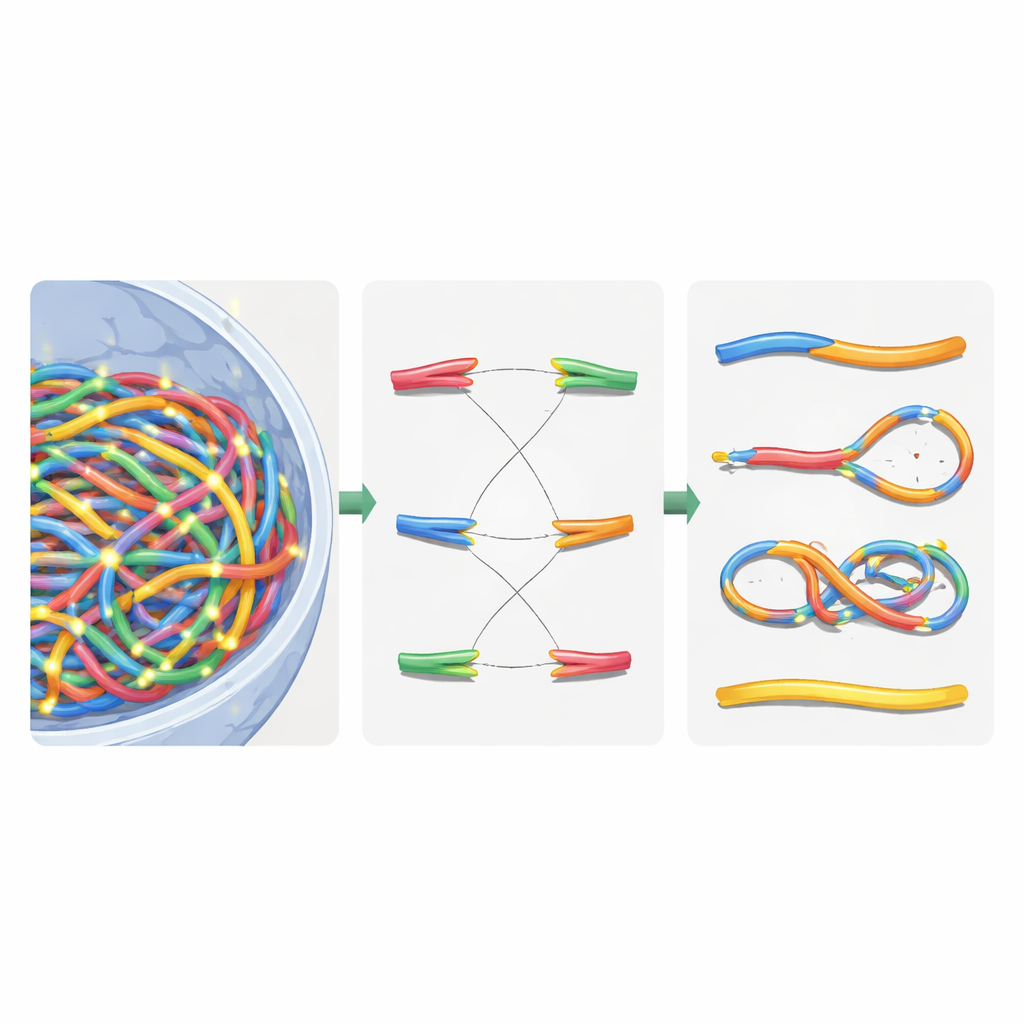
فرز الكروموسومات المكسورة بمنطق الشبكات
بعد هذا الإصلاح الافتراضي، احتوت النواة على مزيج من كروموسومات أعيد تركيبها وقطع متبقية. لتصنيف ما حدث، حول المؤلفون الجينوم المُصلَح إلى رسم بياني غير موجه: أصبحت مقاطع الكروموسوم حواف، وأصبحت نهاياتها ونقاط الكسر عقداً. باستخدام خوارزمية المكونات المتصلة القياسية، استطاعوا استرجاع كل كيان جديد شبيه بالكروموسوم تلقائياً وحساب خصائص رئيسية مثل عدد السنتروميرات (نقاط الارتباط في انقسام الخلية) والتيلوميرات (النهايات الطبيعية). من ذلك، حددوا الثنائي السنترومير (كروموسومات ذات سنتروميرين)، والحلقات، والحذوفات. ثم قارنوا محاكياتهم بتجارب كلاسيكية في خلايا جلد بشرية تعرضت لأشعة غاما وجسيمات ألفا، فوجدوا أن إجمالي تشوهات الكروموسومات تُعاد تكوينها ضمن حوالي 20% من القيم المقاسة، وهو تحسّن كبير مقارنة بالنماذج السابقة.
ماذا يعني هذا للمرضى ورواد الفضاء
بعبارة بسيطة، تُظهر هذه الدراسة أن "مكان" وجود الحمض النووي داخل النواة و"طريقة" طيه تؤثران بشدة على كيفية تراكم أضرار الإشعاع إلى تغييرات كروموسومية خطرة. بدمج هندسة جينوم ثلاثية الأبعاد واقعية، ومحاكاة فيزيائية فعالة، وقراءة مبنية على الرسوم البيانية للكروموسومات المكسورة، يقدّم المؤلفون جسراً قوياً بين بيولوجيا البنية والبيولوجيا الإشعاعية. ويقترحون أن تحسينات مستقبلية—مثل إضافة توقيت إصلاح مفصّل واستخدام بيانات التسلسل الجينومي الكامل—قد تجعل هذا النهج أفضل في التنبؤ بالتأثير البيولوجي للجسيمات عالية الطاقة المستخدمة في علاج السرطان أو المَرْصُودَة في الفضاء العميق. في نهاية المطاف، قد تساعد نماذج أفضل لموطن الحمض النووي داخل خلايانا على تصميم علاجات إشعاعية أكثر أماناً وفعالية وصقل فهمنا لمخاطر الإشعاع على المدى الطويل.
الاستشهاد: Zhao, M., Huang, G., Xu, Z. et al. A polymer physics model of the interphase cell nucleus for radiobiological simulations. Sci Rep 16, 7913 (2026). https://doi.org/10.1038/s41598-026-39234-8
الكلمات المفتاحية: الضرر الجيني الناتج عن الإشعاع, العمارة ثلاثية الأبعاد للكروماتين, تشوهات الكروموسومات, نمذجة فيزياء البوليمرات, علاج بالجسيمات