Clear Sky Science · ar
زيادة تصلب الشرايين وتعبير الـ "inflammarafts" في خلايا البلعميات الرغوية في الفئران المعيبة في AIBP.
لماذا تسد الشرايين أكثر من كونها مجرد دهون زائدة
تصلب الشرايين — الانسداد والتيبس البطيء للأوعية الدموية — هو سبب رئيسي للنوبات القلبية والسكتات الدماغية. نميل لتصويره ببساطة كترسب للدهون في الأوعية، لكن الصورة أعقد: الخلايا المناعية داخل جدار الوعاء يمكن أن تطفئ الالتهاب أو تشعل نيرانه. تستقصي هذه الدراسة لماذا، في بعض الحالات، تتحول هذه الخلايا من "فرق تنظيف" مخزنة للدهون إلى مهيجات خطرة تدفع اللويحات نحو مرحلة أكثر فتكا.
الخلايا المناعية التي تخزن الدهون
داخل لويحات الشرايين النامية، يأخذ نوع من خلايا الدم البيضاء تُسمى البلعميات كميات كبيرة من الكوليسترول ويتحول إلى ما يسمى «خلية رغوية» — خلية منتفخة محشوة بـقطرات زيتية. أظهرت أعمال سابقة في الفئران أن هذه الخلايا الرغوية، رغم مظهرها غير الصحي، تخفت الاستجابة الالتهابية إلى حد ما، بينما البلعميات الأرفع المجاورة تميل لإنتاج إشارات التهابية أكثر. يسأل البحث الجديد ماذا يحدث إذا افتقد الجسم بروتينًا اسمه AIBP، الذي يساعد عادة على إزالة الكوليسترول من سطح الخلايا ويحافظ على تحكم ببعض "البقع الساخنة" في الغشاء الخلوي.
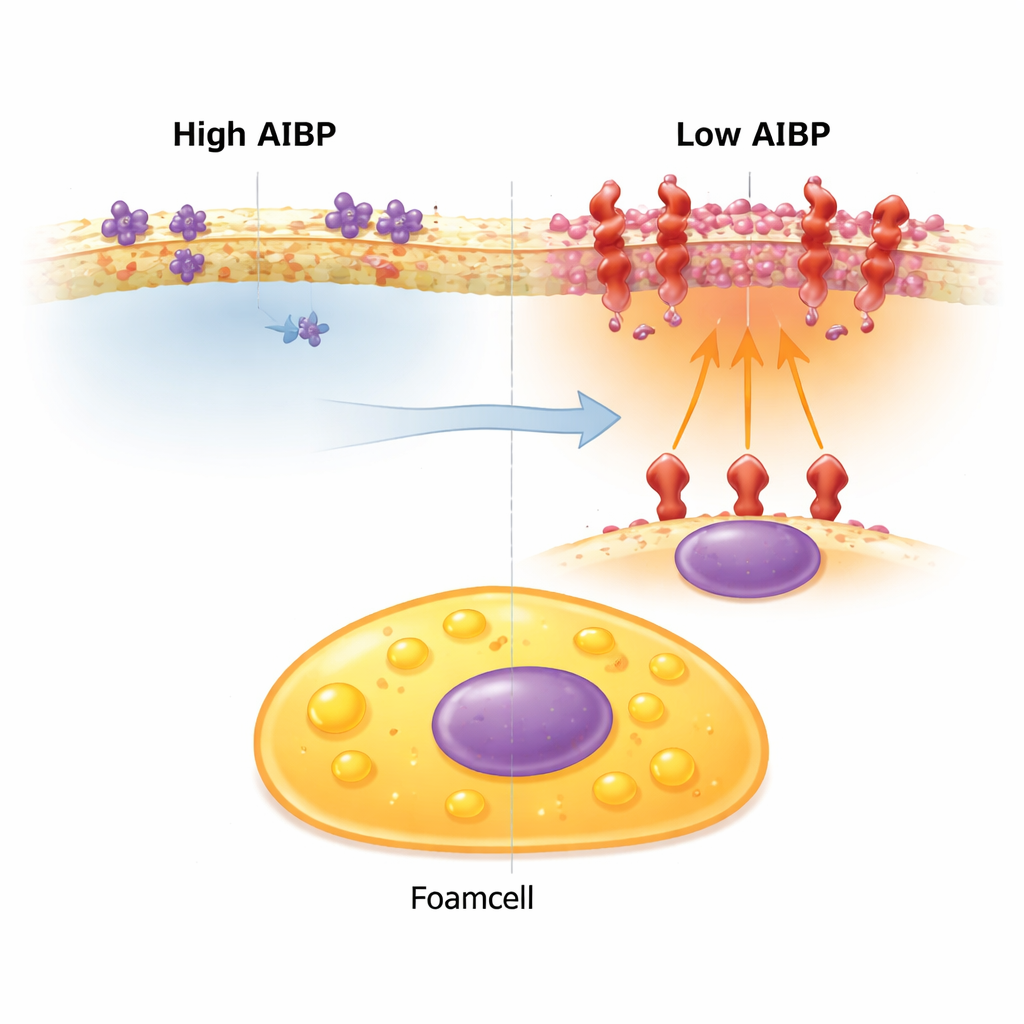
بقع غشائية تضخم إشارات الإنذار
سطح الخلية ليس متجانسًا. يتجمع الكوليسترول وبعض الدهون في منصات صغيرة حيث يمكن لمستقبلات استشعار الخطر أن تتقارب. عندما تتوسع هذه المنصات وتحتشد فيها المستقبلات الالتهابية، يسميها المؤلفون "inflammarafts". أحد هذه المستقبلات، TLR4، يساعد الخلايا على كشف المخاطر لكنه يمكن أن يدفع الالتهاب المزمن إذا فرط تنشيطه. في الفئران العادية المعرضة لارتفاع الكوليسترول، عادة ما تحمل البلعميات غير الرغوية المزيد من هذه inflammarafts، بينما تبقى الخلايا الرغوية منخفضة فيها — وهو سبب جعل الخلايا الرغوية تُعتبر أقل التهابية.
عندما تتحول الخلايا المحشوة بالدهون إلى خلايا ملتهبة
قارن الفريق بين فئران تفتقد كلًا من AIBP ومستقبل رئيسي لإزالة الكوليسترول (مما يجعلها عرضة بشدة لأمراض الشرايين) وفئران ضابطة تفتقد فقط ذلك المستقبل. بعد 16 أسبوعًا على نظام غذائي عالي الدسم، أظهرت الفئران المعيبة في AIBP لويحات تحتوي على المزيد من الخلايا الرغوية، كل منها محشو بمزيد من الدهون المحايدة. والأهم أن هذه الخلايا الرغوية أظهرت مستويات عالية من أزواج TLR4 وبقع غشائية غنية بالكوليسترول — سمات inflammarafts — مما جعلها النوع الخلوي الالتهابي الرئيسي داخل اللوحة بدلاً من الخلايا الأكثر هدوءًا والمخزنة التي كانت تُرى سابقًا. في الأطباق المختبرية، أبدت البلعميات من الفئران المعيبة في AIBP والتي حُولت إلى خلايا رغوية باستخدام كوليسترول مؤكسد تشغيلًا لجينات مرتبطة بالالتهاب وتفكك الأنسجة وإعادة تشكيل الأوعية، وأظهرت مزيدًا من الإجهاد التأكسدي ودوائر ميتوكوندرية متوترة.
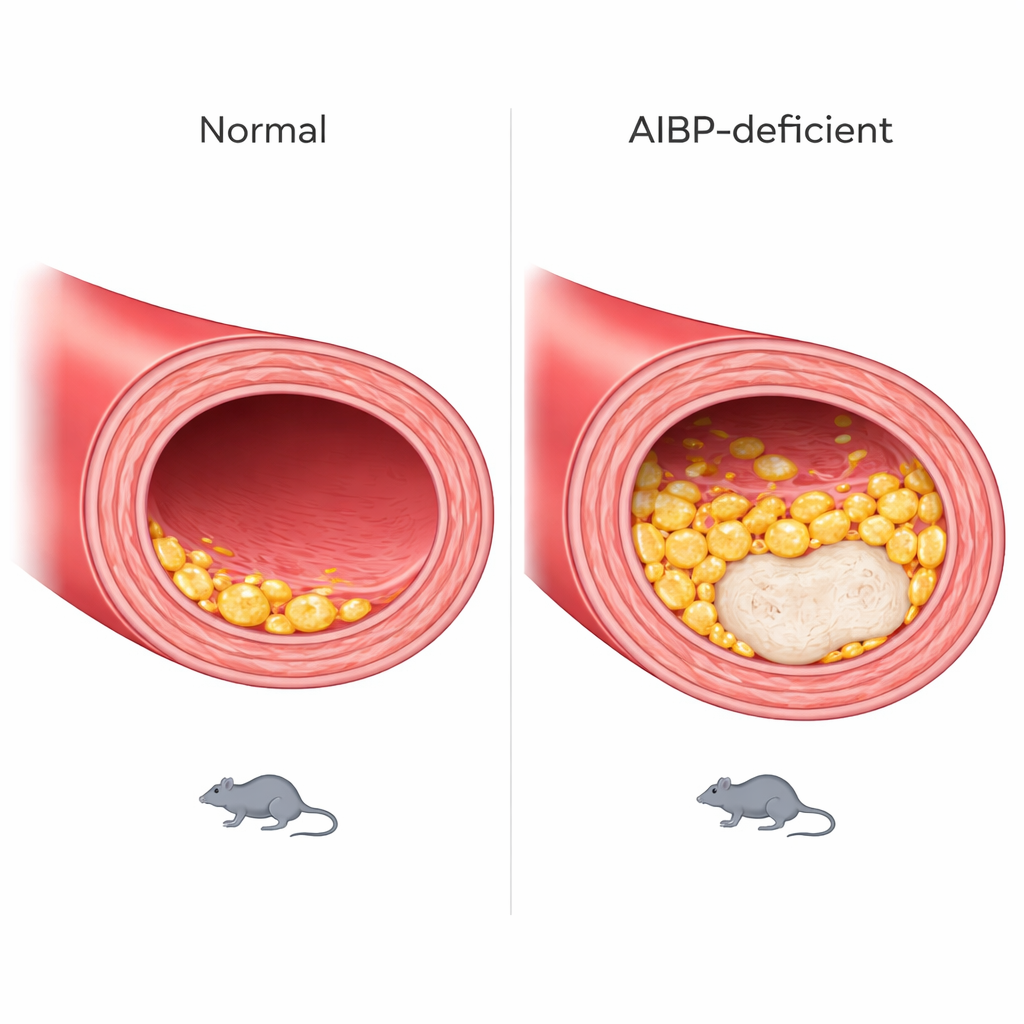
لويحات نامية وغير مستقرة في جدار الوعاء
انعكست هذه التغيرات الخلوية بمرض أكثر شدة في الشرايين. كشوف مقطعية للشريان الرئيسي الخارج من القلب كشفت أن الفئران المعيبة في AIBP طورت لويحات أكبر، والأهم من ذلك نوى نخرية أكبر — مناطق ميتة داخل اللوحة مرتبطة بآفات "قابلة للانفجار" عرضة للتمزق. تأثرت كل من الفئران الذكور والإناث، مع اختلاف نمط المكان على طول الوعاء حيث ظهر الأسوأ بين الجنسين. كما اكتسبت الحيوانات وزنًا بسرعة أكبر وكان لديها مستويات ثلاثي الغليسريد في الدم أعلى، ما يشير إلى اضطرابات أوسع في تعامل الجسم مع الدهون.
ماذا قد يعني ذلك للعلاجات المستقبلية
لغير المتخصص، الرسالة الأساسية أن ليست كل الخلايا المحملة بالكوليسترول في اللوحة متشابهة. عندما يكون AIBP حاضرًا، تميل الخلايا الرغوية إلى العمل كوحدات تخزين، تحجز الدهون الزائدة بهدوء. عندما يغيب AIBP، تعيد تلك الخلايا تشكيل أسطحها، تبني inflammarafts، وتبدأ بإرسال إشارات التهابية عالية تساعد في دفع اللويحات نحو مراحل متقدمة وخطيرة. وعلى الرغم من أن العمل أُجري في الفئران، إلا أنه يبرز AIBP والتحكم في هذه البقع الغشائية كأهداف محتملة لعلاجات مستقبلية تهدف إلى منع لويحات الشرايين من أن تصبح غير مستقرة ومهددة للحياة.
الاستشهاد: Li, S., Nazarenkov, N., Alekseeva, E. et al. Increased atherosclerosis and expression of inflammarafts in macrophage foam cells in AIBP-deficient mice.. Sci Rep 16, 7645 (2026). https://doi.org/10.1038/s41598-026-39113-2
الكلمات المفتاحية: تصلب الشرايين, خلايا البلعميات الرغوية, الالتهاب, استقلاب الكوليسترول, AIBP