Clear Sky Science · ar
نقص Dlgap2 يعطل التوازن المشبكي عبر تعزيز تحلل Itsn1 المعتمد على اليوبكويتين في نموذج يشبه التوحّد ناتج عن حمض الفالبرويك
لماذا يهم دواء شائع وتوصيل الدوائر العصبية
حمض الفالبرويك دواء مستخدم منذ فترة طويلة لعلاج الصرع واضطرابات المزاج، لكن تناوله أثناء الحمل ارتبط بارتفاع مخاطر التوحّد لدى الأطفال. تطرح هذه الدراسة سؤالاً مهماً للأسر والأطباء: ماذا يفعل هذا الدواء تحديداً لأسلاك الدماغ النامية؟ من خلال تتبّع التغيّرات وصولاً إلى جزيئات محددة عند المشابك — نقاط التواصل بين الخلايا العصبية — يكشف الباحثون عن سلسلة أحداث جديدة قد تفسّر السلوكات الشبيهة بالتوحّد وتشير إلى استراتيجيات علاجية مستقبلية. 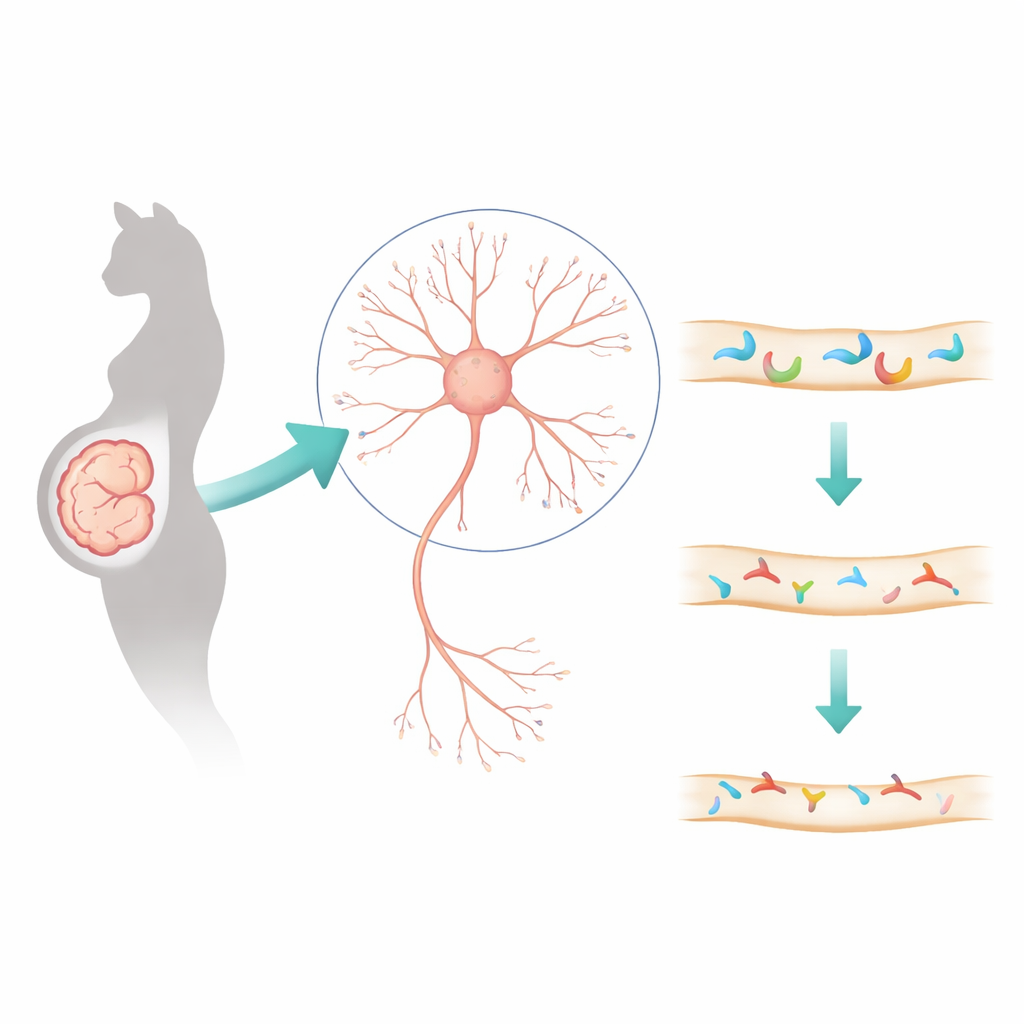
البحث عبر الأنواع عن نقاط ضعف مشتركة
للعثور على دلائل موثوقة، لم يكتفِ الفريق بنموذج حيواني واحد. قارنوا أدمغة أو أنسجة شبيهة بالدماغ من العضلات البشرية القشرية، والقرود، والجرذان، والفئران التي تعرّضت لحمض الفالبرويك قبل الولادة. باستخدام دراسات واسعة النطاق للجينات والبروتينات، حدّدوا مجموعة صغيرة من الجينات التي تغيّرت في كل هذه الأنظمة والتي كانت مرتبطة بالمشابك وعزل المحاور العصبية. من بينها برز جين واحد: Dlgap2، وهو بروتين هيكلي يساعد في تنظيم الجانب البعدي للمشابك المثيرة. في الفئران التي أعطيت حمض الفالبرويك قبل الولادة، انخفضت مستويات Dlgap2 في القشرة العصبية وبشكل أكثر تحديداً داخل مقصورات المشابك الدقيقة، ما يوحي بأن هذا الجزيء الحافظ للبنية هو ضحية رئيسية للتعرّض للدواء.
من التحولات الجزيئية إلى تغيّرات السلوك
سأل المؤلفون بعد ذلك ما إذا كان فقدان Dlgap2 وحده يكفي لتعكير وظيفة الدماغ. استخدموا فيروسات تحمل RNA قصير الشعر لتقليل Dlgap2 في خلايا عصبية مستزرعة من الفئران وفي فئران حديثة الولادة. في المختبر، أظهرت الخلايا العصبية ذات Dlgap2 الأقل تفرعات أقصر ونقَطاً بعدَ مشبكية أقل، وهي علامات على اتصالات أضعف. في الحيوانات الحية، أدى تثبيط Dlgap2 مستهدفًا في الدماغ إلى سلوكات شبيهة بالتوحّد: واجهت الفئران الذكور الصغيرة صعوبة في تعلّم موقع منصة مخفية في متاهة الماء وأظهرت اهتمامًا منخفضًا بشركاء اجتماعيين والجدة الاجتماعية في اختبار الغرفة الثلاثية. تحاكي هذه التغيّرات العجز في التعلّم والاجتماع الذي يُرى في الحيوانات المعرضة لحمض الفالبرويك قبل الولادة، مما يقوّي الحجة بأن خسارة Dlgap2 ليست مجرد أثر جانبي بل دافع لتغيّر السلوك.
إيجاد شريك هش في المشبك
لفهم كيف تتوالى آثار فقدان Dlgap2 داخل المشبك، فحص الباحثون البروتينات المرسخة في الكثافة بعد المشبكية، اللوحة الجزيئية الكثيفة التي تستقبل الإشارات الكيميائية، بتفصيل أكبر. باستخدام البروتيوميات، وجدوا أن تقليل Dlgap2 غيّر وفرة مئات البروتينات المشبكية، لا سيما تلك المشاركة في تنظيم المشابك وإعادة تدوير الحويصلات عن طريق الالتقام الخلوي. انخفض بروتين واحد، Intersectin‑1 (Itsn1)، بشكل حاد بشكل خاص. أظهرت أعمال بيوكيميائية إضافية أن Dlgap2 وItsn1 يتواجدان فعليًا في نفس مجمعات البروتين في أجزاء مخصبة بالمشابك وأن كلاهما يظهران بين الجينات المرتبطة بالتوحّد. أشار ذلك إلى شراكة تنظيمية مركّزة بين الجزيئين داخل بيئة المشبك المزدحمة. 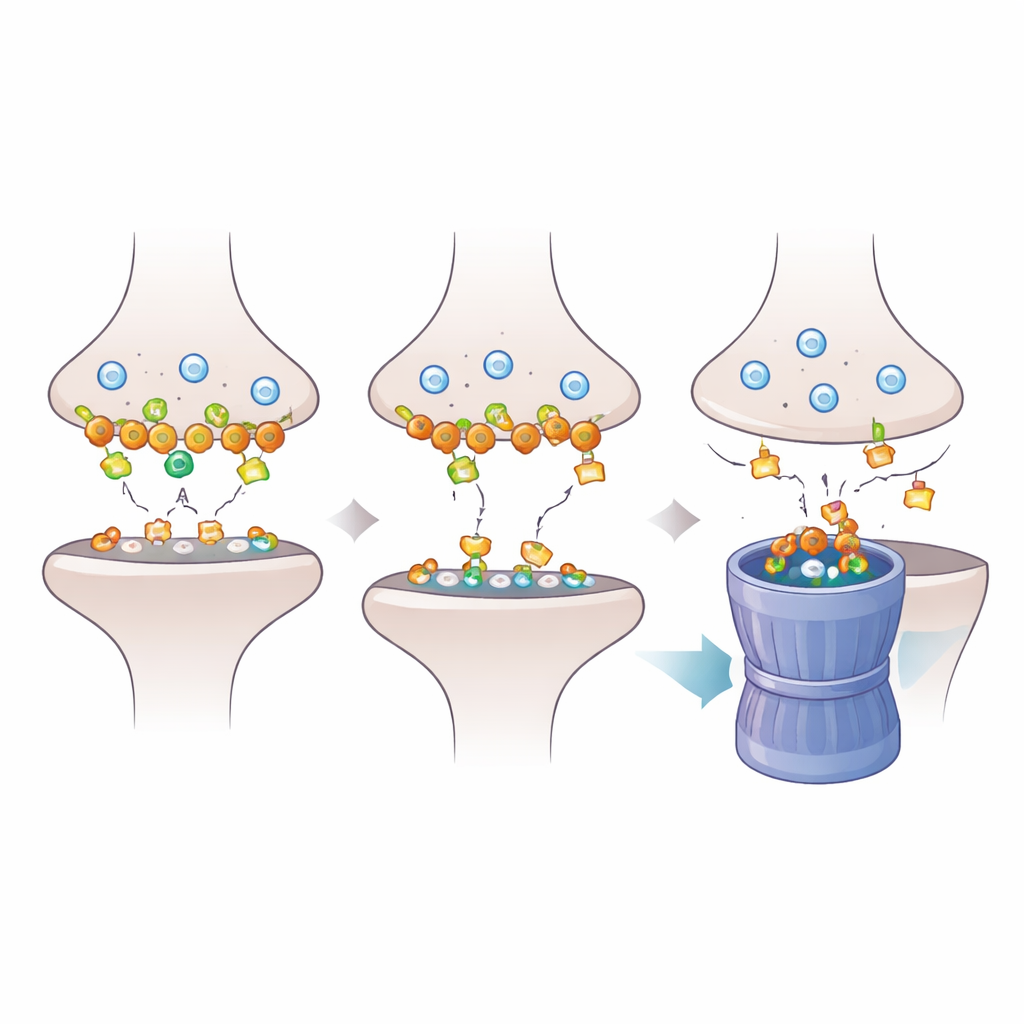
مسار إتلاف خفي يظهر إلى العلن
سأل الفريق بعد ذلك لماذا تنخفض مستويات Itsn1 عندما يختفي Dlgap2. لاحظوا أنه في مقصورات المشبك، استحث نقص Dlgap2 شكلًا من وسم البروتين يُعرف باليوبكويتين المرتبط بـK48، الذي يوسم البروتينات لتفكيكها بواسطة "المَفرِمة" البروتيازومية الخلوية. منع هذا النظام الإتلافي بعقار MG132 حال دون خسارة Itsn1، ما يدل على أن Dlgap2 عادة يحمِي Itsn1 من الوسم والتدمير. بدون Dlgap2، يُوسَم Itsn1 أكثر فأكثر، ويُدخل في البروتيازوم، وينفد من المشابك، مما يقوض إعادة التدوير بالالتقام وتوازن النشاط المشبكي. تشير النتائج إلى أن تحولات طفيفة في سرعة تبديل البروتينات الأساسية يمكن أن تزعزع استقرار المشابك أثناء تطور الدماغ.
ما معنى هذا للتوحّد والعلاجات المستقبلية
مجتمعة، تقترح الدراسة فكرة بسيطة لكنها قوية للجمهور العام: يمكن أن يُضعِف التعرض قبل الولادة لحمض الفالبرويك بروتينًا هيكليًا "دعامة" (Dlgap2) في المشابك. عندما تفقد هذه الدعامة، يصبح بروتينها الشريك (Itsn1) هدفًا مفرطًا لآليات التخلص الخلوية، مما يؤدي إلى إعادة تدوير خاطئة لمكونات المشبك وفي النهاية إلى دوائر مشبكية مشوّهة وسلوكات شبيهة بالتوحّد في الفئران. وبينما تسهم العديد من الجينات والعوامل البيئية في التوحّد، فإن محور Dlgap2–Itsn1 يوفّر سلسلة جزيئية ملموسة من التعرض الدوائي قبل الولادة إلى تغير وظيفة الدماغ. على المدى الطويل، قد تساعد استراتيجيات تحافظ على هذه الشراكة أو تضبط آليات التخلص من البروتينات في المشابك على حماية أدمغة النامية من أشكال مشابهة من الاضطراب.
الاستشهاد: Guo, X., Zhang, L. & Zhuang, K. Dlgap2 deficiency disrupts synaptic homeostasis by promoting ubiquitin-mediated Itsn1 degradation in a valproic acid-induced autism-like model. Sci Rep 16, 8305 (2026). https://doi.org/10.1038/s41598-026-39099-x
الكلمات المفتاحية: حمض الفالبرويك والحمل, بروتينات هيكلية مشبكية, آليات طيف التوحّد, مسار اليوبكويتين والبروتيازوم, نماذج الفأر للتوحد