Clear Sky Science · ar
نقل قوى الجر عبر هيدروجيل مصفوفي حيوي يعزز هجرة ظهارية جماعية بوساطة الإنتغرين
كيف تجذب الخلايا بعضها البعض للشفاء
عندما تقطع جلدك أو تتضرر أحد أعضائك، يجب أن تتحرك صفائح من الخلايا بشكل منسق لإغلاق الجرح. تطرح هذه الدراسة سؤالاً بسيطاً في الظاهر: عندما تزحف الخلايا معاً، هل تكتفي بسحب بعضها البعض، أم أنها "تتحدث" أيضاً عبر المادة اللينة تحتها؟ من خلال إعادة خلق بيئة هلامية واقعية في المختبر، يبيّن المؤلفون أن الخلايا قادرة على إرسال قوى ميكانيكية عبر هذه المصفوفة اللينة لتوجيه الحركة الجماعية، كاشفين عن طبقة مخفية من التواصل قد تكون حاسمة في التئام الجروح، إصلاح الأنسجة، وحتى انتشار السرطان.
أرضية ناعمة تنقل القوة
في أجسامنا، تستقر العديد من الخلايا على سقالة ناعمة غنية بالبروتين بدلاً من شيء صلب مثل الزجاج أو البلاستيك. لمحاكاة ذلك، نمي الباحثون خلايا ظهارية كلوية كصف مستمر على هيدروجيل حيوي مكوّن من ماتريغيل وكولاجين، وهما مكونان شائعان للأنسجة الطبيعية. ثم أنشأوا منطقة فارغة صغيرة في وسط الهلام، شبيهة بجرح صغير، ورصدوا سريان الصف الخلوي نحو الداخل لملء الفجوة. لتعقّب مدى نشاط مسار إشاري رئيسي داخل الخلايا، استخدموا حساسًا حيويًا متوهجًا يبلغ عن نشاط ERK، وهو بروتين يستجيب في كثير من الأحيان للإشارات الميكانيكية. أتاح هذا الإعداد متابعة الوقت الحقيقي لكيفية ارتباط القوى الميكانيكية في الهلام اللين بكل من حركة الخلايا والإشارات الداخلية. 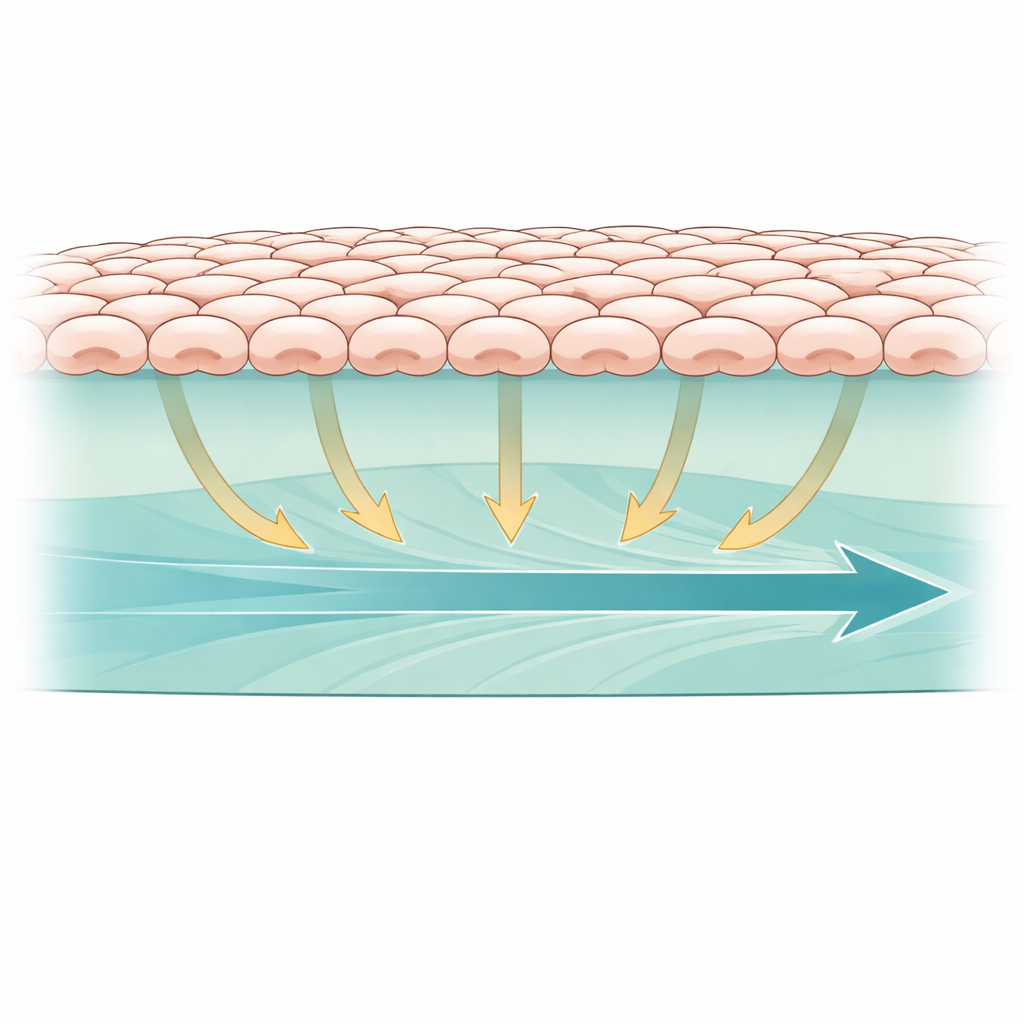
ملاحظة تحرك الأرض تحت الخلايا
لكي يحدد الفريق ما إذا كان الهلام بالفعل يتحمل وينقل القوة، مزجوا جسيمات مغناطيسية دقيقة داخل المادة وتتبعوا حركتها أثناء هجرة الخلايا. على الهلام العادي الذي يحتوي على كل من ماتريغيل وكولاجين، انزلقت الجسيمات ببطء في نفس اتجاه تقدم صف الخلايا، مما يشير إلى أن الخلايا تمسك بالمصفوفة وتسحبها تحتها. على الهلام المصنوع من ماتريغيل وحده، تحركت الجسيمات أبطأ، مما يوحي بضعف نقل القوة. عندما تم عبرنة الهلام كيميائياً بالغلوترات ألدهيد لتقويته و"قفل" الشبكة، تكاد الجسيمات لا تتحرك على الإطلاق. تحت هذه الظروف المغلقة، لا تزال الخلايا تتصلب لكن تقدمها الجماعي تباطأ بشدة، وأصبح إشارة ERK أضعف وأقل تركيزاً عند الحافة المتقدمة، مرابطين الجر القوي للمصفوفة بحركة جماعية أسرع وأكثر توجيهاً.
محركات داخلية وبوابات أيونية تقود الحركة
ثم استقصى المؤلفون ما الذي يولد هذه القوى الجاذبة داخل الخلايا وكيف يتم استشعار هذا النشاط. استخدموا أدوية لحجب انقباض قائم على الميوزين، نفس نوع الآلية الجزيئية التي تشغل العضلات. عندما تم تثبيط الانقباض، انخفض نشاط ERK وتقدم صف الخلايا أبطأ، مُتماشياً مع فكرة أن السحب الداخلي مطلوب لنقل التوتر إلى المصفوفة. كما تداخلوا مع عدة أنواع من قنوات الكالسيوم في غشاء الخلية ومخزن الكالسيوم الداخلي. أدى حجب هذه المسارات الأيونية إلى كبح نشاط ERK وإبطاء الهجرة الجماعية، مما يشير إلى سلسلة من الأحداث تتحول فيها السحبة الميكانيكية على المصفوفة إلى إشارات كالسيوم وERK تساعد في إبقاء المجموعة متحركة معاً.
توجيه الاتجاه عبر مقابض سطحية
نتيجة لافتة خصوصاً جاءت من استهداف الإنتغرينات، الجزيئات السطحية التي تعمل كمرابط صغيرة تربط الخلايا بمحيطها. عندما حجب الباحثون نوعاً رئيسياً من الإنتغرين، لم يعد الصف يتحرك للأمام كجبهة متماسكة، على الرغم من أن الخلايا الفردية كانت لا تزال تتلوى محلياً بسرعة تقارب السرعة الطبيعية. في الوقت نفسه، تكاد حركة الجسيمات في الهلام تتوقف، مما يظهر أن الإنتغرينات أساسية لنقل القوة من الخلايا المنقبضة إلى المصفوفة. بالمقابل، أدى حجب القنوات الميكانيائية الحساسة المرتبطة بـPiezo1، التي تساعد الخلايا على استشعار الضغط الفيزيائي، إلى تقليل كل من وتيرة الهجرة والجر المرصود في الهلام. معاً، ترسم هذه النتائج صورة تُولّد فيها الانقباضات القوة، وتنقلها الإنتغرينات إلى المصفوفة، وتفسر القنوات الميكانيكية الحساسة وإشارة ERK تلك القوة لتنسيق اتجاه وكفاءة الحركة الجماعية. 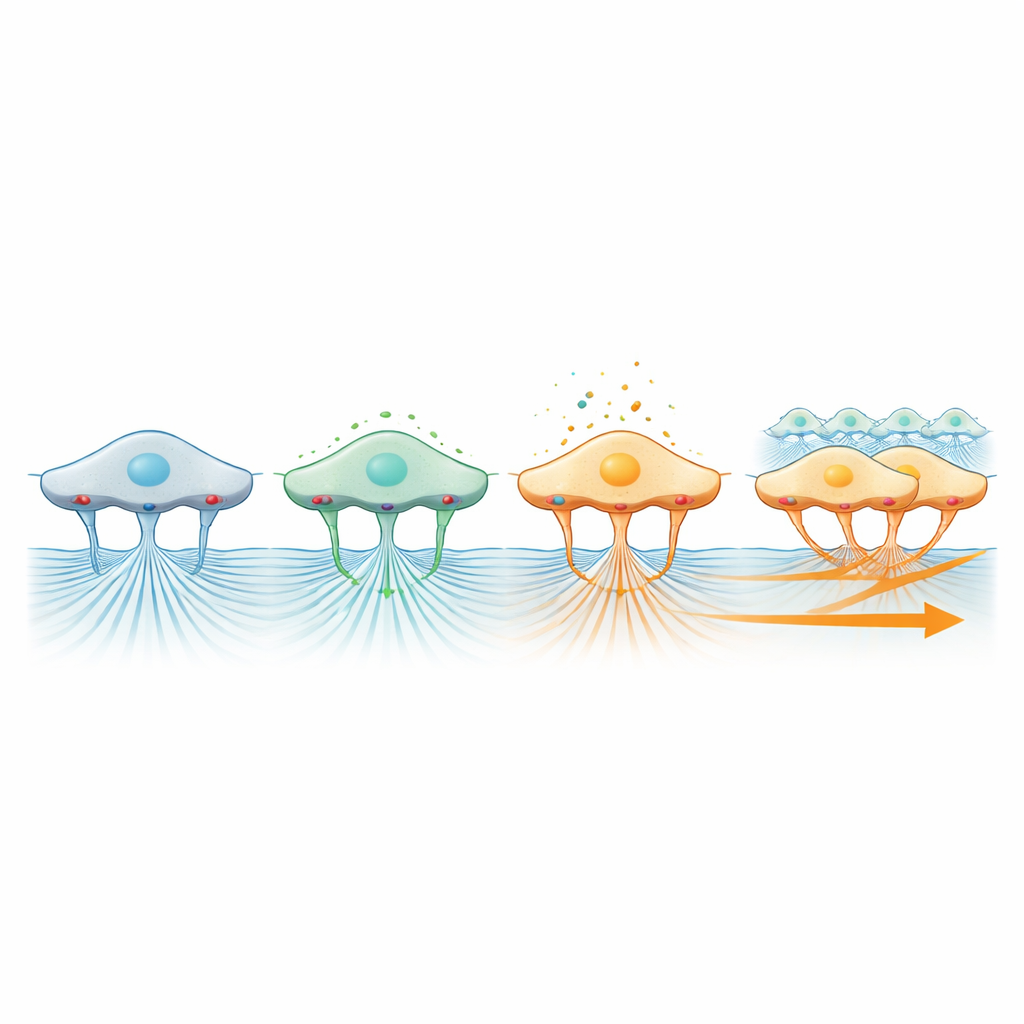
لماذا يهم هذا في الشفاء والمرض
ببساطة، تُظهر هذه الدراسة أن صفائح الخلايا لا تقتصر على سحب بعضها البعض؛ بل تسحب أيضاً المادة اللينة تحتها ومن خلالها، مستخدمة إياها كنوع من "هاتف" ميكانيكي. ترسل انقباضات الطبقة الخلوية توتراً عبر المصفوفة، وهذا التوتر، الذي يتم استشعره عبر الإنتغرينات والقنوات الأيونية ويُقرأ عبر نشاط ERK، يساعد المجموعة على التحرك بسرعة وباتجاه موحَّد. عندما تُقفل المصفوفة كيميائياً بحيث لا يمكن انتشار القوى، أو عندما تُحجب مقابض السطح والمستشعرات الأساسية، يتعثر المسير الجماعي. هذه الرؤى تُعمّق فهمنا لكيفية إغلاق الجروح، وكيف تحافظ الأنسجة على بنيتها، وكيف قد تستغل مجموعات الخلايا الغازية، مثل تلك في السرطان والتليف، المسارات الميكانيكية في محيطها للانتشار.
الاستشهاد: Ouyang, M., Cao, Y., Sheng, H. et al. Traction force transmission via bioactive matrix hydrogel promotes epithelial collective migration mediated by integrin. Sci Rep 16, 8923 (2026). https://doi.org/10.1038/s41598-026-39048-8
الكلمات المفتاحية: هجرة خلوية جماعية, الإشارة الميكانيكية, المصفوفة خارج الخلوية, إنتغرين, التئام الجروح