Clear Sky Science · ar
النمذجة القائمة على البنية تكشف الأساس الجزيئي لنشاط CYP153A6 الجديد تجاه مشتقات التولوين
تفويض المهام الكيميائية الصعبة للطبيعة
يعتمد الكيميائيون والصناعة على تفاعلات تضيف الأكسجين إلى روابط الكربون–الهيدروجين الصعبة، مثلما في تنظيف الملوثات أو صناعة مكونات للأدوية والعطور. إن القيام بذلك بشكل نقي، دون مواد كيميائية قاسية أو نفايات معادن ثقيلة، أمر صعب. تبحث هذه الدراسة في محفز طبيعي، إنزيم يدعى CYP153A6 من بكتيريا تربوية، وتطرح سؤالًا بسيطًا ذو تداعيات كبيرة: هل يمكن توجيه هذا الإنزيم ليُجري بشكل انتقائي «ترقية» لمركبات شبيهة بالتولوين — وهي مكونات شائعة للوقود والمذيبات — إلى منتجات أكثر فائدة وصديقة للبيئة؟
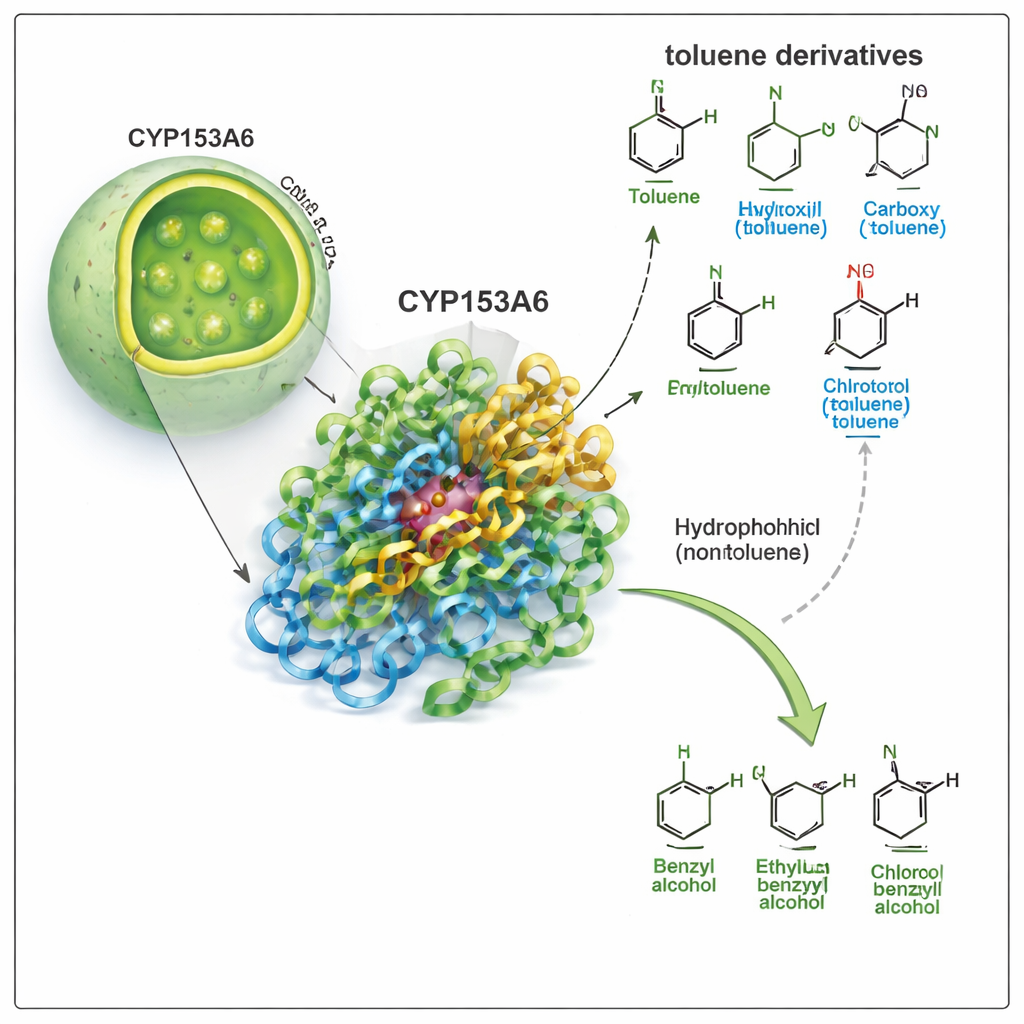
إنزيم يختار موضعًا واحدًا
ينتمي CYP153A6 إلى عائلة سايتوكروم P450 الكبيرة، المتخصصة الطبيعية في الأكسدة المتنوعة. على خلاف العديد من المحفزات الصناعية، يعمل هذا الإنزيم في الماء، عند درجات حرارة معتدلة، ويختار مواضع محددة جدًا على الجزيء. أظهرت أعمال سابقة أن CYP153A6 يضيف الأكسجين إلى نهايات سلاسل الهيدروكربون البسيطة وبعض جزيئات العطر النباتية. هنا، يسأل الباحثون ما إذا كان يمكنه أيضًا مهاجمة الموضع «البنزيلي» — السلسلة الجانبية الصغيرة المرتبطة بحلقة البنزين — في التولوين والمركبات المرتبطة به. هذا التحول يحول مشتقات التولوين إلى كحولات بنزيلية، وهي لبنات بناء قيّمة للصناعات الدوائية والنكهات والمواد الكيميائية الراقية.
اختبار أي الجزيئات يفضلها الإنزيم
أجرى الفريق أولًا تجارب تحويل حيوي باستخدام خلايا E. coli المعدلة التي تنتج CYP153A6، سواء كخلايا كاملة أو كمستخلصات خلوية. عرضوا الإنزيم لمجموعة من مشتقات التولوين، مغيرين المجموعة المرتبطة بحلقة الأروماتيك (مثل ميثيل، كلور، ميثوكسي، هيدروكسيل، أو نيترو) وموقعها (بارا، ميتا، أو أورثو). أدّى الإنزيم أداءً جيدًا جدًا مع المركبات غير القطبية أو ذات القطبية الطفيفة، مثل p‑cymene وp‑xylene وp‑methylanisole وp‑chlorotoluene، محولًا باستمرار مجموعة الميثيل البنزيلية إلى كحول بنزيلي. اللافت أنه تجاهل تمامًا المركبات الأكثر قطبية مثل p‑cresol وp‑methyl benzyl alcohol وp‑nitrotoluene، مع أن هذه مشابهة من الناحية التركيبية. أشارت هذه النمطية إلى أن جيب الإنزيم شديد الكارهة للماء ويعادي المجموعات القطبية.
بناء خريطة ثلاثية الأبعاد للآلة الجزيئية
لأن البنية ثلاثية الأبعاد لـ CYP153A6 لم تُحل تجريبيًا، بنى الباحثون نموذجًا حاسوبيًا عالي الجودة باستخدام P450 قريب ذي بنية معروفة. تحققوا من صحة هذا النموذج بفحص هندسته وتشغيل محاكاة ديناميكا جزيئية طويلة ليُلاحظوا ما إذا كان البروتين ثابتًا عبر الزمن، وهو ما حصل بالفعل. كشفت المحاكيات عن موقع نشط مدفون يتصل بالخارج عبر أنفاق ضيقة تدخل منها الركائز وتخرج منها المنتجات. تُشكَّل هذه الأنفاق وتُغلق بواسطة حلقات مرنة على سطح البروتين، مما يساعد على تفسير كيف يوجّه الإنزيم الجزيئات الكارهة للماء إلى مركز الحديد الهيم التفاعلي مع السماح للماء والمنتجات المؤكسدة بالهروب.
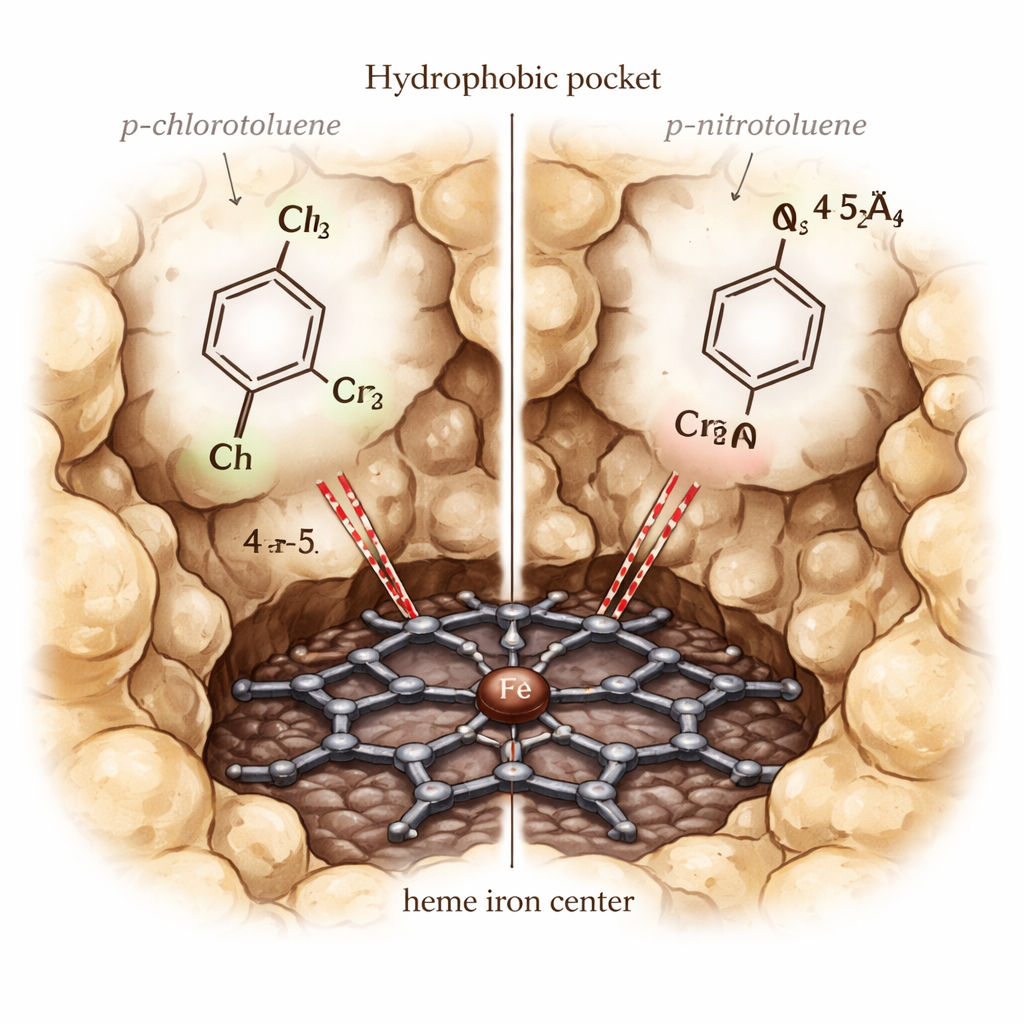
مراقبة الجزيئات وهي تترسخ وتتحرك وتتفاعل
مع وجود النموذج، حاكى المؤلفون كيف ترتبط مشتقات التولوين المختلفة داخل CYP153A6. استخدموا نهجًا يسمى docking الجماعي، جاربين العديد من أشكال البروتين المتباينة قليلًا وعدة حالات إلكترونية لحديد الهيم، لتحديد أي الإعدادات تميز الركائز الحقيقية عن غيرها. السيناريو الفائز استخدم الحديد في حالته الحديدية الساكنة (فيريك) وبدون جزيئات ماء إضافية في الجيب، وفَضّلَ بشكل صحيح الركائز المعروفة. تتبعت محاكيات المتابعة إطارًا تلو الآخر كيف جلس كل جزيء بالنسبة للهيم. بقيت الركائز الجيدة مثل p‑cymene وp‑xylene قريبة من الحديد مع توجيه مجموعة الميثيل البنزيلية نحوه، وكانت طاقات الربط المتوقعة لها مواتية بشدة. أما الركائز الضعيفة فتميل إلى الابتعاد أو اتخاذ أوضاع محرجة أو التفاعل بشكل غير مرغوب مع السلاسل الجانبية الشحمية التي تبطن الجيب.
لماذا يتفاعل شبيه واحد ولا يتفاعل آخر
برز لغز واحد: يُؤكسد p‑chlorotoluene بكفاءة بواسطة CYP153A6، بينما لا يُؤكسد p‑nitrotoluene، مع أن كلاهما يناسب الجيب ويرتبطان بقوة مماثلة في المحاكاة. لحل هذا، أجرى الباحثون حسابات مختلطة الكم/الميكانيكا الجزيئية (QM/MM) أكثر تفصيلًا على حالة الإنزيم عالية التفاعل المعروفة بـ «المركب I». أظهرت هذه الحسابات أن مجموعة النيترو تجذب كثافة إلكترونية كبيرة بعيدًا عن ذرة الكربون البنزيلية، مما يجعل أكسدتها صعبة للغاية رغم القرب الهندسي. بالمقابل، تتيح مجموعة الكلورو تواصلًا إلكترونيًا أفضل بين الهيم والركيزة، ينعكس في كثافة دوران أعلى على الحلقة العطرية ومجموعة الميثيل وميل تفاعلي أفضل لخطوة اقتطاع الهيدروجين الحاسمة.
ماذا يعني هذا لكيمياء أنظف
بعبارة بسيطة، يتصرف CYP153A6 كأنه قفاز دهني صغير يمسك بعض الجزيئات الشبيهة بالوقود بطريقة مثالية لإضافة الأكسجين عند نقطة محددة — محولًا إياها إلى منتجات أكثر قابلية للذوبان في الماء، وأكثر فائدة، وفي نهاية المطاف أسهل تحللًا بيئيًا. تُظهر الدراسة أن الإنزيم يُفضّل البدائل غير القطبية وأن الشكل وتدفق الإلكترونات يحددان ما إذا كانت مشتقة التولوين ستتحول أم لا. من خلال توضيح كيف يتعرف CYP153A6 على هذه الجزيئات ويُفعلها، تضع الدراسة مخططًا لهندسة نسخ محسنة قد تساعد في تنظيف الملوثات العطرية أو تصنيع مواد كيميائية معقدة بطريقة أكثر استدامة.
الاستشهاد: Wei, Y., Donzella, S., Foiadelli, S. et al. Structure-based modeling reveals molecular basis for CYP153A6’s novel activity toward toluene derivatives. Sci Rep 16, 7570 (2026). https://doi.org/10.1038/s41598-026-38986-7
الكلمات المفتاحية: التحفيز الحيوي, سايتوكروم P450, هيدروكسلة التولوين, هندسة الإنزيمات, الكيمياء الخضراء