Clear Sky Science · ar
مصنع حيوي في البلاستيدات لإنتاج α-لاكتالبومين البشري الوظيفي للتطبيقات الغذائية والعلاجية
تحويل النباتات إلى مصنّعات لبروتينات الحليب
تعتمد الحميات الحديثة بشكل كبير على بروتينات الحليب، لكن تربية الأبقار على نطاق عالمي تأتي بتكاليف بيئية وتساؤلات أخلاقية. تستكشف هذه الدراسة طريقة مختلفة تمامًا لإنتاج بروتين رئيسي من حليب الإنسان — عبر تعليم أوراق النباتات على تصنيعه. تُظهر النتائج أن نباتات التبغ يمكن إعادة برمجتها لصنع α‑لاكتالبومين البشري، وهو بروتين مهم لتغذية الرضع وله خصائص محتملة مضادة للسرطان، ما يفتح مسارًا نحو مكونات لصيغ الأطفال خالية من الحيوانات ومكونات غذائية جديدة مكافحة للسرطان.
لماذا يهم هذا البروتين الحليبي
حليب الأم أكثر من مجرد طعام؛ إنه خليط دقيق من البروتينات والدهون والسكريات يتغير حسب حاجة الرضيع. أحد أهم بروتيناته هو α‑لاكتالبومين، الذي يساعد في بناء اللاكتوز، السكر الرئيسي في الحليب ومصدر طاقة حاسم للرضع. α‑لاكتالبومين غني بالأحماض الأمينية الأساسية، بما في ذلك التربتوفان، وهو مادة أولية لسيروتونين المخ المرتبط بالشعور الجيد، وقد رُبط بتحسين مقاومة الإجهاد وحماية محتملة ضد بعض السرطانات. وبفضل سهولة هضمه، ومذاقه المعتدل، واستقراره على نطاق واسع من الحموضة، يُستخدم على نطاق واسع في فورمولا الأطفال والمشروبات الغذائية — والطلب عليه في ازدياد.
مشكلة الألبان التقليدية
الاعتماد على الأبقار لتوفير بروتينات الحليب له عيوب. تنتج الثروة الحيوانية حصة كبيرة من انبعاثات الغازات الدفيئة العالمية، وتتطلب عمليات الألبان الكبيرة مساحات شاسعة من الأرض وكمية كبيرة من المياه والعلف. إلى جانب ذلك، قد تُدخل إدارة المزارع مخاوف بشأن الهرمونات والمضادات الحيوية ومسببات الأمراض إلى سلسلة الحليب. غذّت هذه الضغوط الاهتمام بنُهج "الزراعة الخلوية"، حيث تُنتَج بروتينات الحليب بواسطة ميكروبات أو خلايا مُزرعة بدلاً من الحيوانات. ومع ذلك، فإن العديد من هذه الأنظمة لا تزال مكلفة أو صعبة القياس أو تنتج بروتينات ليست مطابقة تمامًا للنُسخ البشرية. تقدم النباتات، ولا سيما البلاستيدات الخضراء في الأوراق — المصانع الخضراء الصغيرة التي تشغل البناء الضوئي — منصة واعدة بديلة.
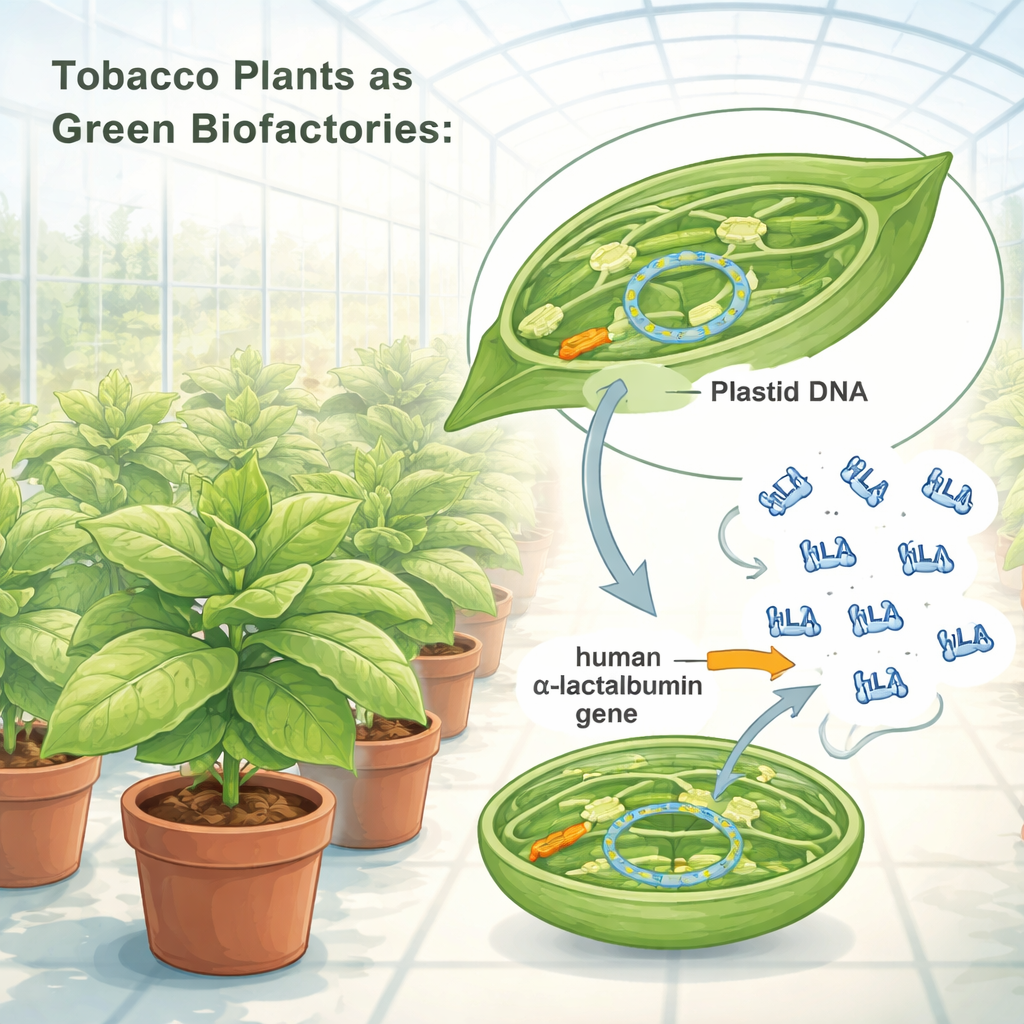
إعادة برمجة البلاستيدات كمصانع حيوية
أعاد الباحثون تصميم التعليمات الجينية الخاصة بألفا‑لاكتالبومين البشري بحيث تتمكن بلاستيدات التبغ من قراءتها بكفاءة. أدخلوا هذا الجين المحسّن في DNA البلاستيدة، مستخدمين "كاسيت جيني" مبنيا من عناصر تنظيمية نباتية قوية تعمل كمفاتيح تشغيل/إيقاف فعالة. باستخدام طريقة قذف الجسيمات، سلّموا هذا الكاسيت إلى خلايا أوراق التبغ، ثم انتقوا الشتائل التي تبنّت البلاستيدات فيها الجين الجديد بشكل كامل. أكدت الاختبارات الجينية أن جميع نسخ DNA البلاستيدة في هذه النباتات حملت الآن مخطط البروتين البشري. نمت النباتات المعدلة بشكل طبيعي في ظروف الدفيئة، منتجة بذورًا دون عقوبات مرئية على الحجم أو الشكل أو الخصوبة، ما يوحي بأن الحمولة البروتينية الإضافية لم تضر بصحة النبات.
إثبات أن البروتين المصنع في النبات يعمل
بعد ذلك سأل الفريق ما إذا كان α‑لاكتالبومين المنتج في النبات يتصرف مثل البروتين البشري الحقيقي. استخرجوا البروتينات القابلة للذوبان من الأوراق، ونقّوا α‑لاكتالبومين، وفحصوا بنية البروتين باستخدام تقنية تكشف كيف تنطوي البروتينات. كانت "البصمة" الطيفية للبروتين المشتق من النبات متداخلة تقريبًا مع تلك الخاصة بألفا‑لاكتالبومين البشري التجاري، مما يشير إلى طي مشابه. وظيفيًا، فعّل البروتين المصنع في النبات إنزيم تصنيع اللاكتوز تقريبًا بمثل كفاءة النسخة الأصلية، محركًا تشكيل اللاكتوز بنسبة نحو 93% من معدل البروتين المعياري. ومن المدهش أن α‑لاكتالبومين تراكم ليشكّل نحو 23% من إجمالي البروتين القابل للذوبان في الأوراق — وهو من أعلى المستويات المبلغ عنها للبروتينات البشرية المصنوعة في بلاستيدات النباتات — ما يشير إلى أن هذا النظام يمكن أن يوفر عوائد ملائمة للصناعة.
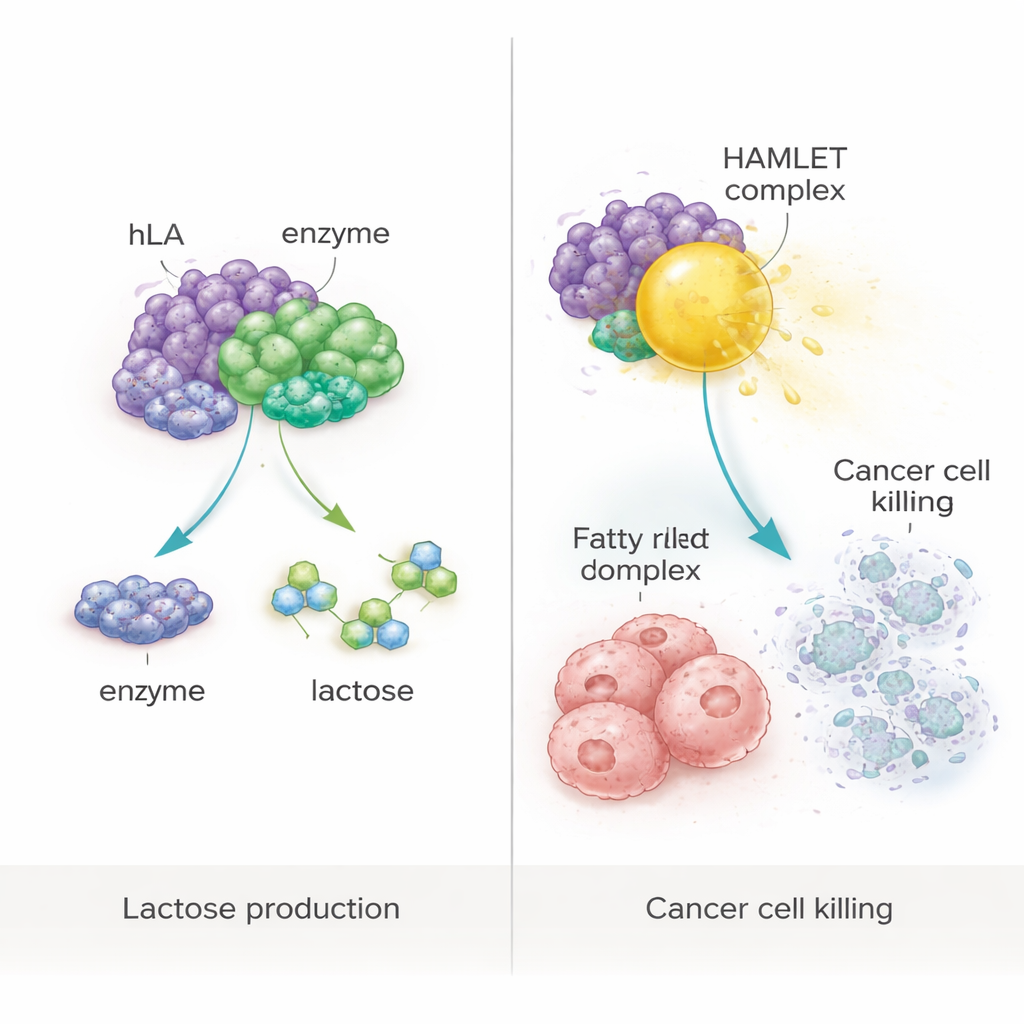
من التغذية إلى مجمعات مكافحة السرطان
اختبرت الدراسة أيضًا فكرة أكثر طموحًا: استخدام البروتين المنتج في النبات كركيزة لمجمع مضاد للسرطان معروف باسم HAMLET، يتكوّن حين يرتبط α‑لاكتالبومين بشدة مع حمض الأوليك، وهو حمض دهني شائع. عن طريق تسخين البروتين المنقّى المشتق من النبات بلطف مع حمض الأوليك تحت ظروف مسيطرة، أنشأ الباحثون مجمعًا شبيهًا بـ HAMLET. عند تطبيق هذا المجمع على خلايا سرطانية بشرية من القولون (WiDr) والثدي (MCF‑7) في الزرع الخلوي، خفّض هذا المجمع بشكل كبير بقاء الخلايا إلى أقل من 10%. أظهر التحليل المتابع أن معظم الخلايا المتأثرة كانت تخضع للموت المبرمج (الاستماتة) بدلاً من الانهيار غير المسيطر. ومن المهم أن لا البروتين وحده ولا الحمض الدهني وحده ولا مستخلصات النباتات غير المعدلة سببت موتًا خلويًا ملحوظًا، مؤكدة أن التأثير القاتل للسرطان اعتمد على تكوّن المجمع المحدد.
ماذا قد يعني هذا للأغذية والأدوية المستقبلية
تُظهر النتائج مجتمعة أن بلاستيدات النباتات يمكنها إنتاج كميات كبيرة وموثوقة من بروتين حليب بشري ذا صلة غذائية ونشاط علاجي. للمستخدم غير المتخصص، يعني هذا أن صيغ الأطفال المستقبلية أو الأطعمة الوظيفية أو المكملات قد تُنتَج يومًا ما باستخدام بروتينات مزروعة في الأوراق بدلاً من الحصاد من الأبقار، مما يقلل الأثر البيئي مع مطابقة أكثر لبيولوجيا الإنسان. في الوقت نفسه، يمكن تحويل نفس البروتين المستخرج من النبات في المختبر إلى مجمع مضاد للسرطان مستهدف، مما يلمّح إلى سلاسل إنتاج نباتية لأدوية حيوية ميسورة التكلفة. بينما هناك حاجة لمزيد من البحوث لتأكيد السلامة والأداء في الحيوانات والإنسان — ولنقل هذه التقنية إلى محاصيل صالحة للأكل — تقدم الدراسة لمحة مقنعة عن إمكانية أن تضاعف النباتات دورها كمصانع صغيرة للمغذيات والطب من الجيل القادم.
الاستشهاد: Ehsasatvatan, M., Kohnehrouz, B.B. Transplastomic biofactory for the production of functional human α-lactalbumin for nutritional and therapeutic applications. Sci Rep 16, 7359 (2026). https://doi.org/10.1038/s41598-026-38965-y
الكلمات المفتاحية: بروتينات الحليب المصنوعة من النبات, مصنع حيوي في البلاستيدات, ألفا-لاكتالبومين البشري, بدائل الألبان المستدامة, علاج السرطان HAMLET