Clear Sky Science · ar
miR-340 يحسّن فعالية العلاج الجيني بجين p53 في خلايا سرطان البروستاتا النقيلي عبر خفض تنظيم MDM2
لماذا يهم هذا البحث المرضى
بالنسبة للرجال الذين يعانون من سرطان البروستاتا المتقدم الذي انتشر ولم يعد يستجيب للعلاج الهرموني، العلاجات المتاحة اليوم قد تبطئ المرض لكنها نادراً ما تشفيه، وحوالي نصف المرضى فقط يعيشون لأكثر من خمس سنوات. تستكشف هذه الدراسة طريقة جديدة لتحسين فعالية العلاجات الحالية عبر تعزيز أحد دفاعات الجسم الطبيعية ضد السرطان — بروتين الحارس p53 — باستخدام مساعد جيني صغير يسمى miR-340.
إعادة إيقاظ حارس الورم في الجسم
تعطل العديد من السرطانات، بما في ذلك أورام البروستاتا العدوانية، وظيفة p53، البروتين الذي يوقف الخلايا المصابة عادة لإصلاحها أو يحفز تدميرها الذاتي. إحدى المقاربات، التي جُرِّبت بالفعل في مرضى أنواع أخرى من السرطان، هي العلاج الجيني بجين p53: توصيل نسخة سليمة من جين p53 إلى خلايا الورم لاستعادة استجابتها للضرر. لكن الأورام غالباً ما تنتفض عبر زيادة إنتاج MDM2، وهو بروتين يوسم p53 للتدمير. افترض المؤلفون أنه إذا أمكن خفض MDM2 في نفس الوقت الذي يضاف فيه p53، فقد يُستعاد التأثير الكامل لهذا المسار الحامي للخلايا في سرطان البروستاتا الصعب علاجه.
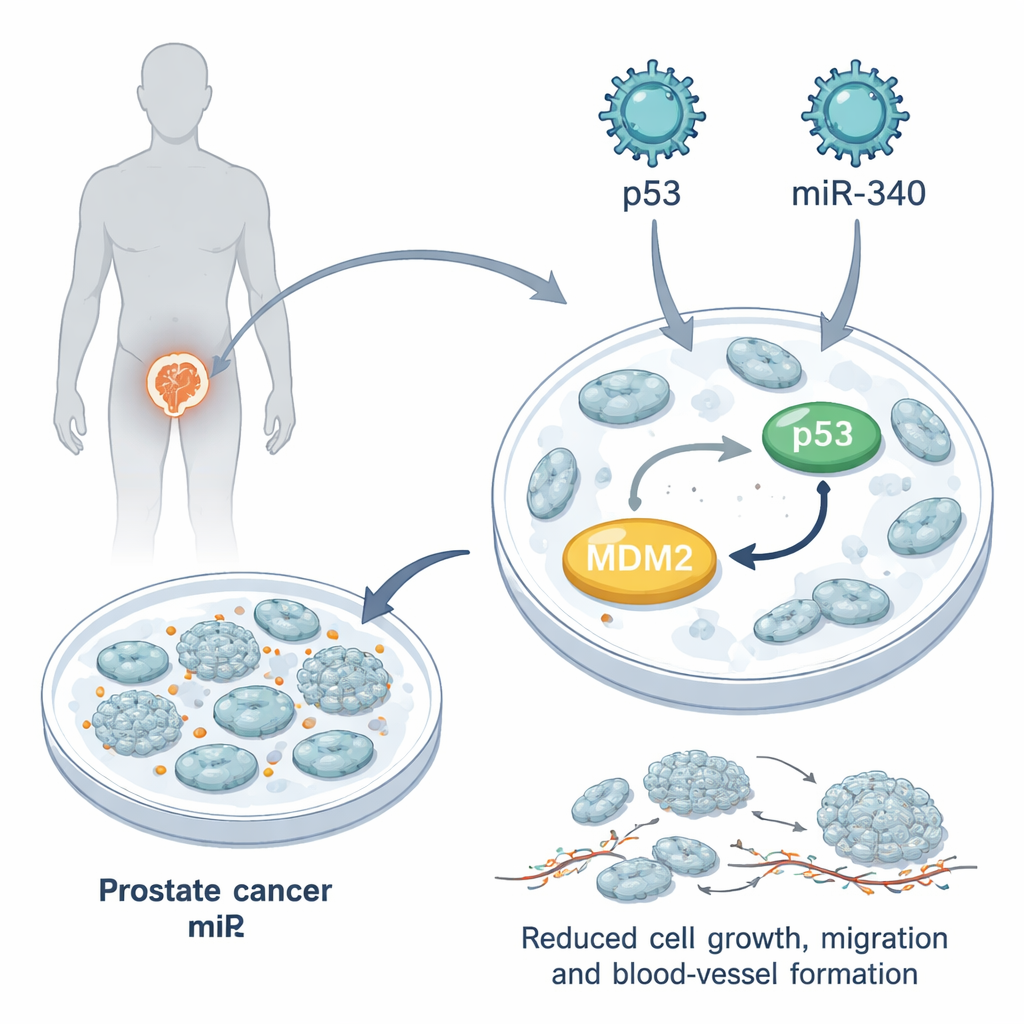
RNA صغير بتأثير كبير
ركز الفريق على miR-340، جزيء RNA صغير موجود طبيعياً في الخلايا يساعد على ضبط نشاط الجينات. أظهرت تحليلات قواعد البيانات أن مستويات miR-340 أضعف في أورام البروستاتا مقارنة بالنسيج البروستاتي السليم، وأضعف أكثر في المرض المقاوم للخصي. أشارت دراسات سابقة إلى أن miR-340 يمكن أن يرتبط بالرسالة الجينية لـMDM2 ويقلل من إنتاجه. في هذه الدراسة، استخدم الباحثون جسيمات لنتيفيروس مهندسة لإدخال miR-340 إضافي، أو p53 إضافي، أو كليهما معاً إلى خلايا سرطان البروستاتا PC3، النموذج المختبري الشائع الذي يفتقر تماماً إلى p53 الوظيفي. أكدوا أن miR-340 يخفض MDM2 بشكل قوي وأن الجمع بين miR-340 وp53 أدى إلى مستويات أعلى بكثير من الشريك الأساسي لـp53 وهو p21، وهو مهم لإيقاف انقسام الخلايا.
تبطيء نمو الخلايا السرطانية وانتشارها
بعد تعديل خلايا سرطان البروستاتا، اختبر الباحثون سرعة نموها، وحركتها، وقدرتها على دعم تكوين الأوعية الدموية — وهي كلها سمات للأورام العدوانية. p53 وحده أبطأ نمو الخلايا وتسبب في زيادة عدد الخلايا المتوقفة في طور الراحة G0/G1 من دورة الخلية. لم يؤثر miR-340 وحده تأثيراً كبيراً على النمو، لكن عند دمجه مع p53 ضاعف هذا الإبطاء بشكل كبير: استغرقت الخلايا وقتاً أطول لمضاعفة عددها وشكلت كرات ثلاثية الأبعاد شبيهة بالأورام أصغر وأضعف. في اختبارات الخدش التي تحاكي هجرة خلايا الورم، كاد miR-340 وحده لا يغير حركة الخلايا، لكنه عزز قدرة p53 على منع الخلايا من الزحف إلى الفجوة. كما قلل الجمع بينهما الإشارات التي تشجع نمو الأوعية الدموية، والسائل المأخوذ من خلايا سرطان البروستاتا المعالجة جعل خلايا الأوعية الدموية تنمو وتتحرك أقل.
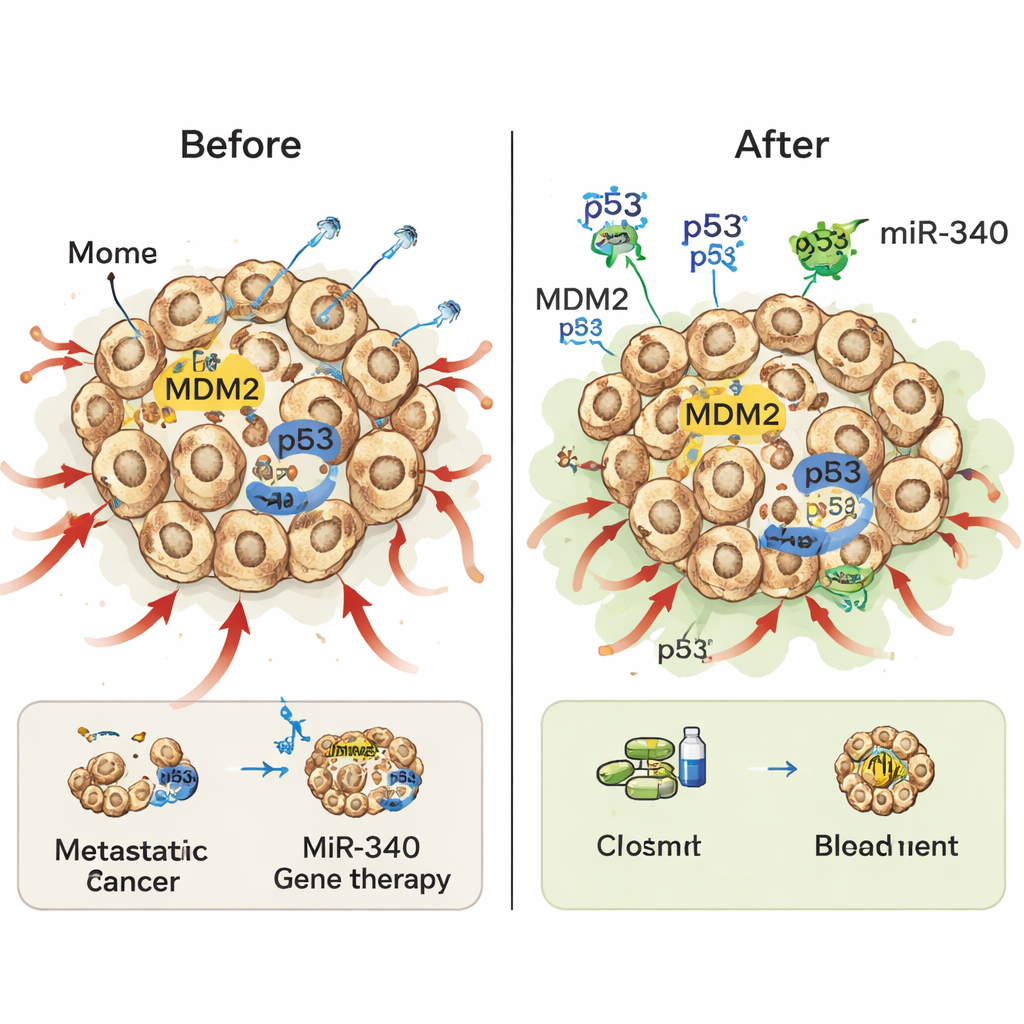
جعل الكيماوي والإشعاع أكثر فاعلية
كانت نتيجة بارزة أن العلاج الجيني المشترك miR-340/p53 جعل العلاجات القياسية أكثر قوة دون أن يكون ساماً بدرجة كبيرة بمفرده. عندما تعرضت الخلايا المعدلة لمستويات منخفضة من دواء الكيماوي دوكسيتاكسيل، أظهرت الخلايا الحاملة لكل من miR-340 وp53 ارتفاعاً حاداً في الموت المبرمج مقارنة بالخلايا التي أعطيت p53 وحده أو miR-340 وحده. وظهرت نمطية مماثلة مع أشعة X: لم يفعل miR-340 وحده كثيراً، لكن مع p53 جعل خلايا السرطان أكثر حساسية بشكل كبير، مما خفض قدرتها على تكوين مستعمرات بعد التعرض للإشعاع. في كلتا الحالتين يبدو أن miR-340 يساعد عبر تقليل MDM2، مما يسمح لـp53 المضاف بالتراكم وتفعيل برامجه المسببة للموت بالكامل بمجرد أن تلحق العلاجات الكيماوية أو الإشعاعية ضرراً بالخلايا السرطانية.
ماذا قد يعني هذا للرعاية المستقبلية
يخلص المؤلفون إلى أن إضافة miR-340 إلى علاج p53 الجيني يمكن أن يقوّي هذا النهج بشكل ذي معنى ضد سرطان البروستاتا النقيلي المقاوم للعلاج — لا سيما عند استخدامه جنباً إلى جنب مع العلاجين الكيماوي والإشعاعي الحاليين. وعلى الرغم من أن هذا العمل أُنجز في خلايا مخبرية وما يزال يواجه عقبات عملية، مثل تحسين طرق توصيل الجينات والتحقق من السلامة في الحيوانات والبشر، إلا أنه يحدد استراتيجية واضحة وقابلة للاختبار: إضعاف كوابح الورم على p53 عبر خفض MDM2، ثم السماح للعلاجات القياسية بتحفيز استجابة أقوى وموجهة. إذا أكدت دراسات لاحقة هذه الفكرة، فقد يحصل المرضى ذات يوم على جرعات أقل من الأدوية السامة مع تحقيق سيطرة أقوى على الأورام.
الاستشهاد: Deyhimfar, R., Kehtari, M., Saadatpour, F. et al. miR-340 improves the efficiency of p53 gene therapy in metastatic prostate cancer cells through downregulation of MDM2. Sci Rep 16, 7527 (2026). https://doi.org/10.1038/s41598-026-38963-0
الكلمات المفتاحية: سرطان البروستاتا, العلاج الجيني, p53, MDM2, الميكرو RNA-340