Clear Sky Science · ar
تصميم وتركيب وتقييم مضاد للأورام لجزيئات سبيروإندينوبيريدوتريازيني بيران جديدة وظيفية
لماذا تهم الأدوية الجديدة للسرطان
أنقذت علاجات السرطان حياة الكثيرين، لكنها غالبًا ما تصاحبها مشكلتان كبيرتان: قد تتوقف الأورام عن الاستجابة للأدوية، وقد تتعرض الأنسجة السليمة للضرر إلى جانب الخلايا السرطانية. يستكشف هذا البحث فئة جديدة من الجزيئات الصغيرة المصممة بدقة لتهاجم الخلايا السرطانية بفعالية مع أن تكون ألطف على الخلايا الطبيعية. من خلال بناء هذه المركبات بطريقة ذكية وكفوءة واختبارها على خلايا سرطان الثدي والبنكرياس العدوانية، يسعى الباحثون إلى إشارات مبكرة تدل على إمكانية تطوير أدوية مستقبلية أكثر أمانًا وانتقائية.
بناء أشكال دوائية أفضل
جوهر هذا العمل هو شكل كيميائي ثلاثي الأبعاد خاص يُعرف بسقالة سبيرو. يمكن تخيله كنظامين حلقويين ملتحمين عند نقطة ارتكاز واحدة، مما يجعل الجزيء بأكمله صلبًا ومضغوطًا وأكثر «كائنية» مقارنة بسلسلة رخوة. تستخدم العديد من الأدوية الحديثة هذا النوع من البُنى لأنه يساعدها على الانطباق بإحكام داخل جيوب البروتينات المعقدة داخل خلايانا. في هذا المشروع، صمم الفريق جزيئات سبيرو جديدة تجمع عدة أنواع حلقوية معروفة من دراسات سابقة بوجود إمكانات مضادة للسرطان، مدمجة كلها في بنية منظمة بإحكام.
وصفة بسيطة لجزيئات معقدة
كيميائيًا، عادةً ما يكون من الصعب ويستغرق وقتًا طويلًا تصنيع هذه المركبات السبيروية. بدلًا من ذلك، استخدم الباحثون استراتيجية أحادية الإناء ومتعددة المكونات: تُخلط ثلاث وحدات بناء بسيطة معًا وتنسكب تحت الظروف المناسبة لتتجمع ذاتيًا إلى البنية المستهدفة المعقدة. بعد اختبار مذيبات ودرجات حرارة مختلفة، كانت أفضل الشروط هي الإيثانول العادي مع تسخين لطيف، دون أي محفز مضاف. أنتج هذا النهج مكتبة صغيرة من الجزيئات ذات الصلة بعوائد عالية، والتي حللوها بعد ذلك تفصيليًا باستخدام تقنيات معيارية للتأكد من تشكل البنى المقصودة بالفعل.
اختبار المركبات الجديدة
بمجرد إرساء الجانب الكيميائي، تحول التركيز إلى البيولوجيا. عرض الفريق خطين من خلايا السرطان صعبة العلاج — خلايا بنكرياسية (Panc1) وخلايا سرطان ثدي ثلاثية السلبية (MDA‑MB‑231) — للمركبات الجديدة، جنبًا إلى جنب مع خلايا مشتقة من الجلد الطبيعية كفحص سلامة. باستخدام اختبار لوني يقيس عدد الخلايا الحية بعد المعالجة، وجدوا أن ثلاثة مركبات، الموسومة 9d و9e وخصوصًا 9f، برزت بقدرة أقوى على تثبيط النمو مقارنة بالباقي. اللافت أن جميع هذه المركبات أظهرت تأثيرًا ضئيلًا على الخلايا الطبيعية عند نفس التركيزات، مما يلمح إلى درجة من الانتقائية التي تفتقر إليها كثير من العلاجات الكيميائية الحالية.
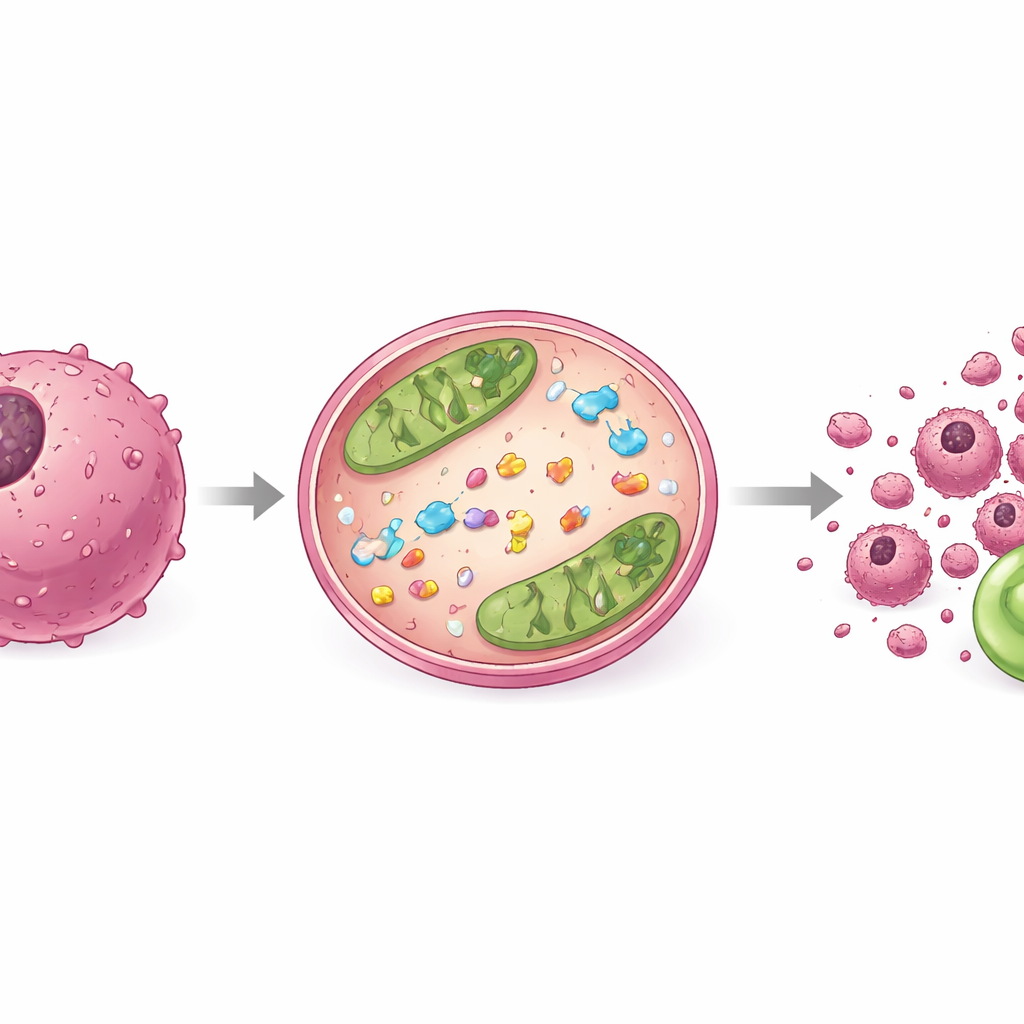
كيف تستجيب الخلايا ولماذا تهم البنية
لمعرفة ما يحدث داخل الخلايا السرطانية، صبّ الباحثون حمضها النووي وفحصوها تحت مجهر فلوري. أظهرت الخلايا المعالجة بالمركب الأكثر فعالية، 9f، نوى منكمشة ومفتتة — علامات كلاسيكية للموت الخلوي المبرمج بدلًا من التسمم البسيط. نظرت تجارب إضافية في بروتينين حارسين أساسيين يتحكمان في مفتاح موت الخلية: أحدهما يمنع الموت والآخر يعززه. قلبت المعالجة بـ9f هذا التوازن نحو الهلاك الذاتي في الخلايا السرطانية، متسقة مع دفع موجه نحو الاستماتة. من خلال مقارنة أعضاء عائلة المركبات المختلفة، لاحظ الفريق أيضًا أن تغييرات صغيرة حول قلب السبرو أحدثت تأثيرات كبيرة على القدرة الفعالة، مما يبرز كيف يمكن لكل من السحب الإلكتروني والموقع ثلاثي الأبعاد للمجموعات الفرعية أن يضبط النشاط المضاد للسرطان.
ماذا قد يعني هذا للعلاجات المستقبلية
بعبارات بسيطة، يقدم البحث طريقة عملية لصنع فئة جديدة من الجزيئات الصلبة ثلاثية الأبعاد التي يمكن أن تبطئ بقوة نمو بعض الخلايا السرطانية بينما تحافظ على سلامة الخلايا السليمة في اختبارات المختبر. كان أحد المرشحين، 9f، فعالًا بمقدار مساوي لدواء كيميائي معياري ضد خطوط الخلايا المختبرة وبدا أنه يقتلها عبر تفعيل برنامج الهلاك الذاتي الداخلي لديها. هذه النتائج مبكرة ومحدودة على خلايا مزروعة في أطباق — لا تزال الدراسات على الحيوانات، وسلوك الجرعات في الجسم، والسلامة طويلة الأمد مجهولة. ومع ذلك، تُظهر الدراسة كيف يمكن لتصميم جزيئي ذكي وطرق تركيبية فعالة أن تتعاون لإنتاج قادة واعدين لأدوية السرطان المستقبلية.
الاستشهاد: Safari, F., Bayat, M., Hosseini, H. et al. Design, synthesis, and antitumor evaluation of new functionalized spiroindenopyridotriazinepyrans. Sci Rep 16, 7917 (2026). https://doi.org/10.1038/s41598-026-38946-1
الكلمات المفتاحية: علاج السرطان, تصميم الأدوية, الجزيئات السبروية, الاستماتة, التركيب متعدد المكونات