Clear Sky Science · ar
تتفاعل A2-بانكورتيات مع Bcl-xL وWAVE1 لتعزيز مواقع تواصل الميتوكوندريا والشبكة الإندوبلازمية (MERCs) وتفاقم ارتفاع الكالسيوم الميتوكوندري لوساطة موت الخلايا في السكتة الدماغية
لماذا تهم الروابط الصغيرة في الدماغ عند المواليد
غالباً ما يُنظر إلى السكتة الدماغية كمرض يصيب البالغين، لكن عندما تحدث عند المواليد فإنها قد تُلحق أضراراً بهدوء بنمو الدماغ مسببة مشكلات تستمر مدى الحياة. تبحث هذه الدراسة فيما يحدث داخل الخلايا العصبية أثناء مثل هذه الأزمة. يركز المؤلفون على عائلة بروتينية قليلة المعرفة تُدعى بانكورتيات ويظهرون كيف أن نسختين تطوريتين تعملان كمحفزات خطرة، تشد الاتصالات بين هياكل خلوية رئيسية وتدفع سيلاناً من الكالسيوم يمكن أن يدفع الخلايا العصبية الصغيرة نحو الموت.
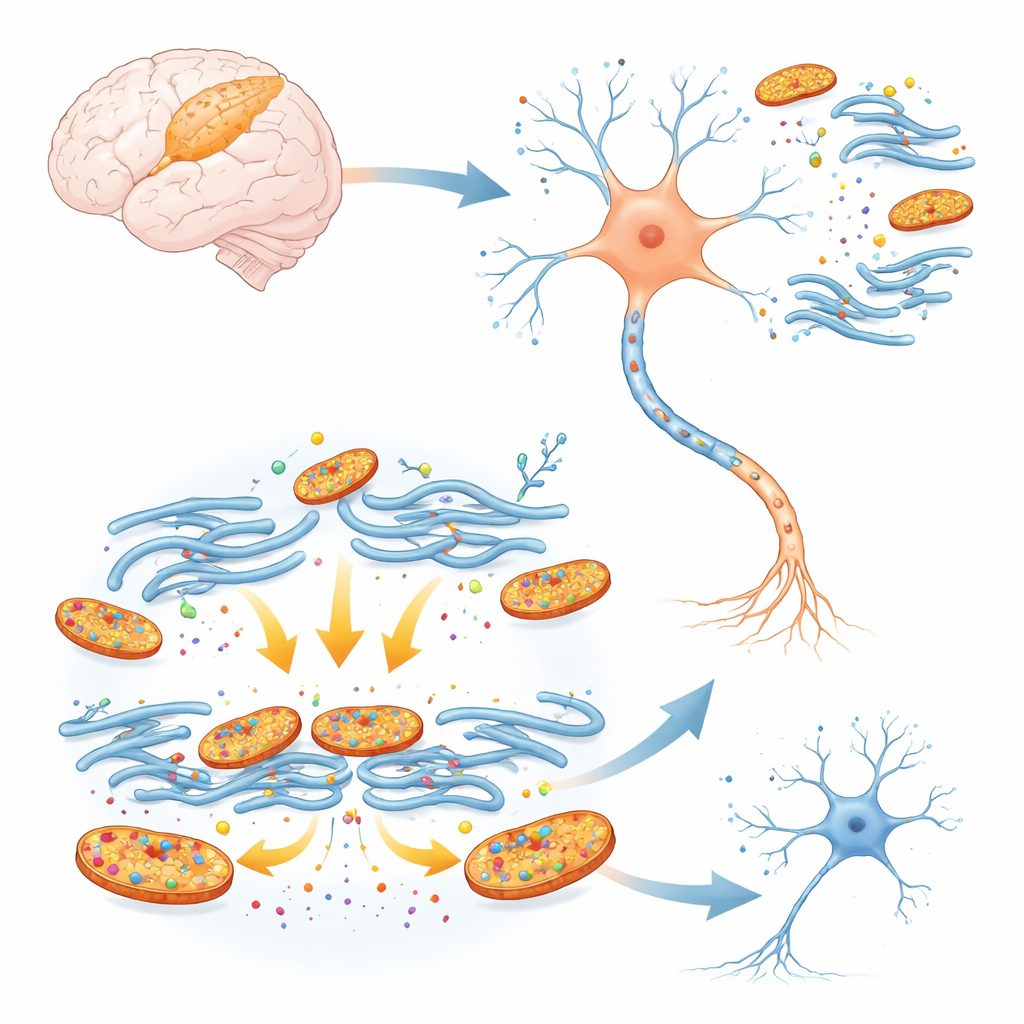
الجهات المذنبة الخفية في دماغ المواليد
البانكورتيات هي بروتينات تشبه السقالة تساعد في تشكيل الدماغ النامي. هناك شكلان، يُسمّيان A2-بانكورتيات، يكونان وفيرين خلال النمو المبكر ثم يتضاءلان مع نضوج الدماغ. وبما أن أدمغة المواليد أكثر عرضة لفقدان الأكسجين، تساءل الباحثون إن كانت هذه البروتينات المبكرة قد تفاقم الضرر عندما يُقطع تدفق الدم إلى القشر المؤقتاً كما يحدث في السكتة الوليدية. في خلايا قشر الفأر المزروعة، استخدموا أدوات جينية لتقليل مستويات كل البانكورتيات ثم عرضوا الخلايا لنقص الأكسجين والجلوكوز الذي يحاكي السكتة. كانت الخلايا العصبية ذات مستويات بانكورتين منخفضة أكثر احتمالاً للبقاء على قيد الحياة بكثير، مما يشير إلى أن هذه البروتينات، بدلاً من حماية الخلايا الصغيرة، تسهم في دفعها نحو الإصابة تحت الإجهاد.
من نماذج سكتة الفأر إلى أنسجة دماغية محمية
لمعرفة ما إذا كانت هذه الوظيفة الضارة تظهر أيضاً في دماغ حي، صمم الفريق فئراناً تفتقر تحديداً إلى أشكال A2-البانكورتين التطورية. ثم تعرّضت فئران صغيرة تبلغ أسبوعين معطلّة الجين وأشقاؤها الطبيعيون لحصار شريان دماغي رئيسي، وهو نموذج قياسي للسكتة الإقفارية. بعد يوم واحد، أظهرت المجموعتان إصابة في مناطق عميقة من الدماغ، لكن قشرة الفئران الخالية من A2-بانكورتيات كانت بها إصابة تقارب نصف ما لوحظ في الحيوانات الطبيعية. بشكل صارخ، اختفى هذا التأثير الوقائي في فئران بعمر خمسة أسابيع، عندما تسود متغيرات البانكورتين البالغة. تشير هذه النتائج المعتمدة على العمر إلى أن A2-بانكورتيات عوامل رئيسية معززة للموت في القشرة الوليدية، رابطين برنامجاً تطورياً بالحساسية للسكتة.
مناطق اتصال خطرة داخل الخلايا العصبية
داخل الخلايا، تقف الميتوكوندريا المنتجة للطاقة بالقرب من الشبكة الإندوبلازمية (ER)، وهي شبكة غشائية مطوية تخزن الكالسيوم. حيث يقترب الغشائين من بعضهما تشكل ما يُسمى مواقع تواصل الميتوكوندريا–الشبكة الإندوبلازمية أنفاقاً مجهرية يمكن أن يمرّ عبرها الكالسيوم. الانتقال المعتدل يدعم إنتاج الطاقة، لكن الزيادة الزائدة قد تُحمّل الميتوكوندريا وتؤدي إلى موت الخلية. وجد الباحثون أن A2-بانكورتيات، مع شريكين—Bcl-xL وWAVE1—تتجمع لتكوّن مركباً ثلاثي الأجزاء يوجد عند هذه المواقع. عندما أجبروا الخلايا على إنتاج كميات إضافية من A2-بانكورتيات مع هذين الشريكين، تلامست الميتوكوندريا وER بتكرار وشدة أكبر، كما أظهره مُستشعر فلوري مشتت خاص. انضم بروتين ربط يُدعى GRP75 إلى هذا المركب، مساهماً في تثبيت مناطق الاتصال.
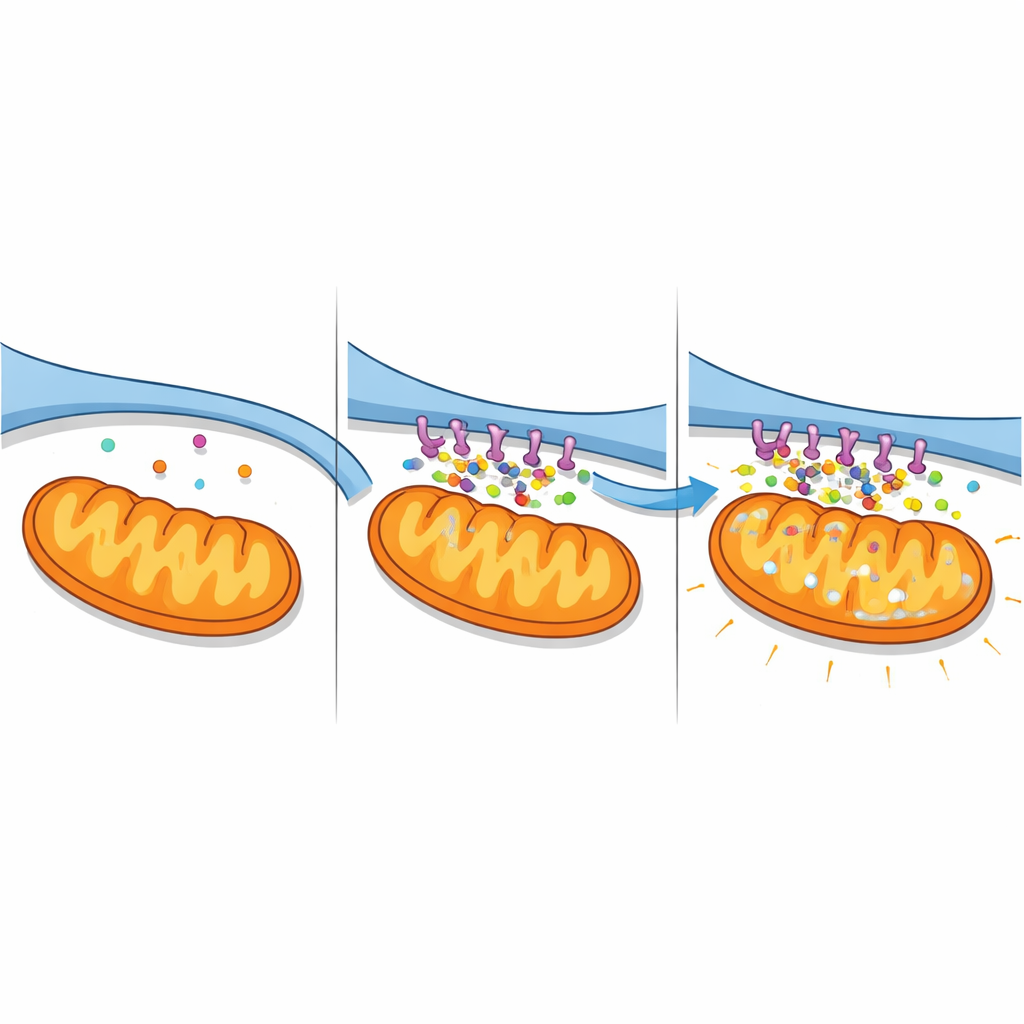
سيول الكالسيوم ومحطات الطاقة الفاشلة
كان لتقوية الاتصالات عواقب خطيرة على توازن الكالسيوم. باستخدام مؤشرات فلورية تُبلغ عن الكالسيوم في السيتوسول وER والميتوكوندريا بشكل منفصل، راقب المؤلفون تغير المستويات مع الزمن. أظهرت الخلايا التي عبرت عن مركب A2-البانكورتين ارتفاعاً مستمراً في الكالسيوم داخل الميتوكوندريا وفي السائل المحيط، مصحوباً بانخفاض في مخازن ER، وهو بصمة نقل هائل من ER إلى الميتوكوندريا. منع قناة إطلاق الكالسيوم الرئيسية على سطح ER (IP3R) حال دون هذه التغيرات إلى حد كبير، مؤكداً أن المركب يضخم مساراً محدداً من ER إلى الميتوكوندريا. في خلايا شبيهة بالعصب تعرضت لنقص الأكسجين والجلوكوز شبيه بالسكتة، أدى تثبيط البانكورتيات إلى التأثير المعاكس: خفّت حمولة الكالسيوم وتم الحفاظ على مخازن ER بشكل أفضل. تكشف هذه النتائج معاً عن A2-بانكورتيات كمنظمين لـ"طريق سريع" للكالسيوم يصبح قاتلاً تحت الإجهاد الإقفاري.
ما معنى هذا لحماية أدمغة المواليد
لغير المتخصصين، الخلاصة أن هذه الدراسة تحدد مفتاحاً جزيئياً جديداً يساعد في تقرير ما إذا كانت الخلايا العصبية الصغيرة ستنجو أو تموت بعد السكتة. عن طريق تشديد الوصلات المجهرية بين الأغشية المخزنة للكالسيوم ومحطات طاقة الخلية، تتسبب A2-بانكورتيات في اختناق الميتوكوندريا بكمية زائدة من الكالسيوم وفشلها. إزالة هذه البروتينات في الفئران الصغيرة يخفف تأثير السكتة التجريبية، مما يوحي بأن أدوية أو علاجات جينية تستهدف تعطيل مركبات A2-البانكورتين—أو إرخاء مواقع الاتصال التي تعززها—قد تقلل يوماً ما من إصابة الدماغ لدى المواليد المتأثرين. وبينما تظل مثل هذه العلاجات آفاقاً مستقبلية، ترسم الدراسة مساراً واضحاً وقابلاً للاختبار يربط بين بروتينات تطورية وحمولة الكالسيوم المفرطة وفقدان الخلايا العصبية في السكتة الوليدية.
الاستشهاد: Yang, Q., Wang, CC., Matsuyama, T. et al. A2-pancortins interact with Bcl-xL and WAVE1 to promote mitochondria-ER contact sites (MERCs) and exacerbate mitochondrial calcium elevation to mediate cell death in stroke. Sci Rep 16, 8467 (2026). https://doi.org/10.1038/s41598-026-38928-3
الكلمات المفتاحية: السكتة الدماغية الوليدية, مواقع تواصل الميتوكوندريا والشبكة الإندوبلازمية, حمولة الكالسيوم الزائدة, بروتينات بانكورتين, موت الخلايا العصبية