Clear Sky Science · ar
الكادميوم يؤدي إلى نفوق فِرُوبتوز في خلايا الحيوانات المنوية للفأر عبر تنشيط مسار ROS–TCA
لماذا يهم معدن شائع صحة الرجال
الكادميوم معدن طري يُستخدم في البطاريات والأصباغ ومنتجات صناعية أخرى. يمكن أن يتراكم في التربة والمياه والغذاء، ويدخل أجسامنا تدريجياً بصمت. ربطت دراسات عديدة التعرض للكادميوم بانخفاض عدد الحيوانات المنوية وتردي جودتها لدى الرجال، لكن الآلية الدقيقة التي يُصيب بها الخلايا المولِّدة للحيوانات المنوية ظلت غير واضحة. تركز هذه الدراسة على المشكلة، كاشفةً كيف يدفع الكادميوم خلايا تكوين الحيوانات المنوية في الفأر نحو مسار موت خلوي محدد مرتبط بالحديد ونظام طاقة متوتر داخل الميتوكوندريا، وهي محطات طاقة الخلية.
من التلوث إلى خلايا منوية معرضة للخطر
يُعد الكادميوم مضرًّا معروفًا للجهاز التناسلي الذكري في البيئة. الرجال المعرضون له في العمل أو الساكنون في مناطق ملوثة يظهرون غالباً انخفاضاً في عدد الحيوانات المنوية وحركتها وشكلها الطبيعي، وحتى تلفاً في الحمض النووي للحيوانات المنوية. تؤكد دراسات على الحيوانات هذه النتائج، مع انكماش الخصيتين وتسريب الحواجز الواقية وانخفاض التستوستيرون وفقدان واسع للخلايا الجرثومية. لاحظ المؤلفون سابقًا أن الكادميوم قد يثير نوعًا غير معتاد من الموت الخلوي المعتمد على الحديد يُسمى الفتحروبْتوس في نسيج الخصية. في العمل الحالي، ركّزوا على الخلايا المنوية في مرحلة التحول إلى حيوانات منوية (spermatocytes) لدى الفأر ليروا بالضبط كيف يضرها الكادميوم وما إن كان هذا المسار المعتمد على الحديد متورطًا.
حمولة حديدية زائدة ونوع خاص من الموت الخلوي
للتحقيق، زرع الفريق سلالة خلايا منوية فأرية في أطباق وعرض الخلايا للكادميوم، مع أو من دون أدوية معروفة بقدرتها على حجب الفتحروبْتوس. خفّض الكادميوم بقاء الخلايا بنحو النصف وأبطأ انقسامها. داخل الخلايا ارتفعت مستويات الحديد الحر ومؤشر تلف الدهون المسمى المالونديألدهيد بشدة، بينما انخفض إنزيم وقائي رئيسي هو GPX4. كما زادت بروتينات أخرى مشاركة في تخزين الحديد وتصديره، مما يشير إلى اضطراب شديد في معالجة الحديد. عندما أضاف الباحثون مثبطات الفتحروبْتوس — مركب مخلّب للحديد وجزيء يحمي الدهون — خفتت كثير من هذه التغيرات الضارة وتحسّن بقاء الخلايا. معًا، تتوافق هذه التبدلات مع بصمة الفتحروبْتوس، مما يشير إلى أن الكادميوم لا يقتل الخلايا بشكل غامض فحسب، بل يدفعها نحو هذا البرنامج المحدد للموت المعتمد على الحديد والدهون.
الميتوكندريا تحت الحصار
تعقدت القصة عندما وجه العلماء انتباههم إلى الميتوكوندريا، مراكز الطاقة التي تولد أيضًا الجذور الحرة التفاعلية (ROS) كمنتجات ثانوية. تحت المجهر، أظهرت الخلايا المنوية السليمة ميتوكوندريا طويلة خيطية، بينما ظهرت الخلايا المعرضة للكادميوم بميتوكوندريا قصيرة ومجزأة، علامة على تلفٍ بنيوي. أكدت القياسات ارتفاع ROS الميتوكوندريا، بينما انخفض الشحنة الكهربائية عبر غشاء الميتوكوندريا — مؤشر رئيسي للوظيفة. استجابت الخلايا برفع نظم الدفاع الداخلية، بما في ذلك بروتينات تتحكم بها مستشعر الإجهاد Nrf2، لكن هذه الدفاعات لم تكن كافية. ومن الأهمية أن أدوية حجب الفتحروبْتوس خففت من ROS الميتوكوندريا وأعادت الصحة الميتوكوندرية جزئيًا، رابطين بذلك محطات الطاقة المتضررة مباشرة بمسار الموت المعتمد على الحديد.
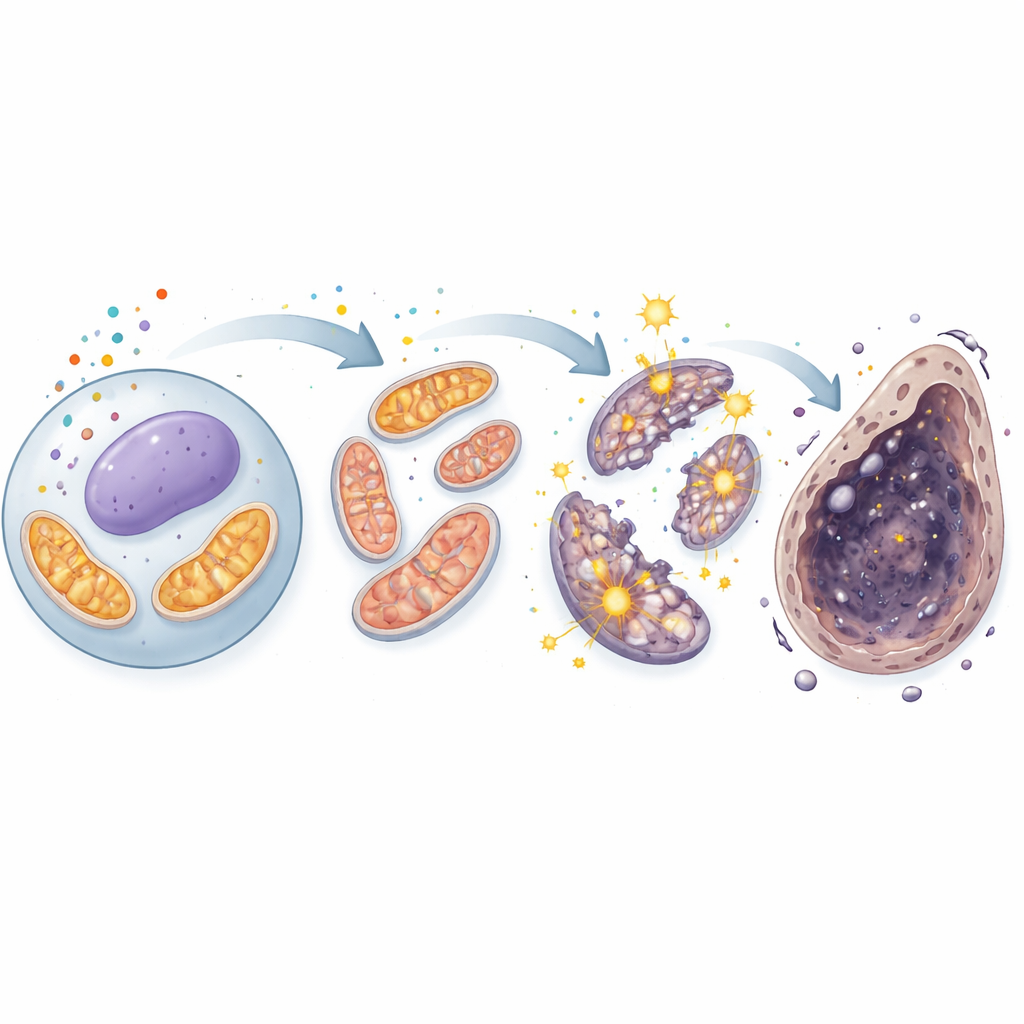
دورة شرّ داخل محطة طاقة الخلية
باستخدام مزيج من تصوير نشاط الجينات وقياسات المستقلبات، رأى الباحثون أن الكادميوم لم يقتصر على إتلاف الميتوكوندريا فحسب — بل بدا أنه يستولي على دورتها الأساسية للطاقة، دورة ثلاثي الكربوكسيل (TCA). ارتفعت مستويات متوسطين مركزيين في دورة TCA، ألفا‑كيتوجلوتارات والسكسينات، بشكل كبير، وزادت نشاطية إنزيم كاربوكسيلاز البيروفات الذي يمد الدورة بالوقود الطازج. وهذا يقترح أن دورة TCA أصبحت مفرطة النشاط بشكل متناقض في الخلايا المتضررة، مما يُجبر المزيد من الإلكترونات على المرور عبر سلسلة التنفس ويسبب تسربًا أكبر للجذور الحرة في العملية. ثم أعادت هذه الـROS الإضافية تغذية كيمياء الحديد وتلف الأغشية، معززةً الفتحروبْتوس. مرة أخرى، خفضت مثبطات الفتحروبْتوس هذه الاضطرابات الأيضية، مما يؤكد الصلة الوثيقة بين الكادميوم، فرط نشاط الميتوكوندريا، والموت الخلوي المعتمد على الحديد.
ماذا يعني هذا للخصوبة والبحوث المستقبلية
بعبارة مبسطة، تُظهر الدراسة أن الكادميوم يهاجم خلايا تكوين الحيوانات المنوية بإتلاف الميتوكوندريا مباشرة ودفع دورة الطاقة لديها نحو فرط نشاط ضار. يجمع هذا المزيج الخلايا بجزيئات أكسجين تفاعلية ويعطل توازن الحديد، ويدفعها نحو الفتحروبْتوس. وبما أن الخلايا المنوية (spermatocytes) ضرورية لإنتاج حيوانات منوية صحية، فإن خسارتها تساهم في تفسير الارتباط القوي بين التعرض للكادميوم وتناقص خصوبة الذكور. على الرغم من أن هذه التجارب أُجريت في خلايا فأرية في طبق، إلا أنها تقدم خريطة آلية واضحة يمكن للاختبارات الحيوانية والسريرية المستقبلية أن تتحقق منها. كما تبرز الدراسة استراتيجيات وقائية محتملة: أدوية أو مغذيات تُقلل إجهاد الميتوكوندريا، تضبط دورة TCA بدقة، أو تمنع تلف الأغشية المدفوع بالحديد قد تساعد في حماية الجهاز التناسلي الذكري من معادن بيئية مثل الكادميوم.
الاستشهاد: Xiong, L., Yi, L., Zeng, X. et al. Cadmium induces ferroptosis in mouse spermatocytes by activating the ROS–TCA pathway. Sci Rep 16, 8449 (2026). https://doi.org/10.1038/s41598-026-38827-7
الكلمات المفتاحية: سُميّة الكادميوم, خصوبة الذكور, إجهاد الميتوكوندريا, الفتروبْتوس, الجذور الحرة التفاعلية