Clear Sky Science · ar
العوامل على مستوى الأحماض الأمينية لاستقرار الحرارة في الإندوليزين المتطرف Ts2631
لماذا تهمّنا الفيروسات المحبة للحرارة لمضادات حيوية مستقبلية
مع تزايد مقاومة المضادات الحيوية، يتسابق العلماء لإيجاد طرق جديدة لقتل البكتيريا الخطرة. نهج واعد يستعير أسلحة من الفيروسات التي تصيب البكتيريا، المسماة العاثيات. تنتج هذه الفيروسات إنزيمات تُعرف بالإندوليزينات، التي تثقب جدران الخلايا البكتيرية. الدراسة هنا تركز على إندوليزين مقاوم للحرارة بشكل ملحوظ، Ts2631، من فيروس يعيش في ينابيع ساخنة في أيسلندا. من خلال الكشف عن أي وحدات بناء فردية في هذا البروتين تجعله مستقرًا عند درجات حرارة تكاد تغلي، يأمل الباحثون في تصميم إنزيمات مضادة للبكتيريا أكثر متانة وطول عمر للاستخدام الطبي والبيوتكنولوجي. 
أداة فيروسية مصقولة في ينابيع ساخنة تغلي
يأتي Ts2631 من عاثية تصيب البكتيريا المحبة للحرارة Thermus scotoductus، التي تزدهر في مياه تصل حرارتها إلى ما يزيد بكثير عن 60 °م. يقوم إنزيم Ts2631 بقطع رابطة محددة في الببتيدوجليكان، الشبكة القوية التي تحيط بالخلايا البكتيرية. ما يميز Ts2631 هو ثباته الحراري الشديد: يبقى مطويًا حتى نحو 100–105 °م، حسب الوسط. هذا أعلى بكثير من درجات الحرارة التي تنهار عندها معظم البروتينات. قارن المؤلفون Ts2631 بأقرب قريبه المدروس من فيروس يعيش في درجات حرارة معتدلة، لايزوزيم T7، لمعرفة الحيل الهيكلية التي استخدمتها الطبيعة للحفاظ على سلامة Ts2631 في ظل هذه الظروف القاسية.
حلقات أقصر ومزيج مختلف من وحدات البناء
البروتينات سلاسل من 20 نوعًا من الأحماض الأمينية، مطوية إلى أشكال معقدة. عندما وضع الباحثون هياكل Ts2631 وT7 ثلاثية الأبعاد فوق بعضها، وجدوا أن البنية العامة متشابهة جدًا: كلاهما له نواة مدمجة من الحلزونات والشرائط. يكمن الاختلاف الرئيسي في مناطق الحلقات المرنة التي تربط هذه العناصر. في Ts2631، هذه الحلقات أقصر وتظهر مرونة أقل، بينما لدى لايزوزيم T7 حلقات أطول وأكثر ارتخاءً. يحمل Ts2631 أيضًا المزيد من بعض الأحماض الأمينية المرتبطة غالبًا بمقاومة الحرارة: البرولين الصلب؛ البقايا العطرية مثل التيروسين والتريبتوفان؛ والأرجينين موجب الشحنة. في الوقت نفسه، يحتوي على عدد أقل من السيرين وحمض الأسبارتيك والحمض الغلوتامي، التي قد تجعل البروتينات أكثر عرضة عند درجات حرارة عالية. ينطبق هذا النمط ليس فقط مقابل لايزوزيم T7 بل أيضًا عند مقارنة Ts2631 بمئات الآلاف من البروتينات الفيروسية وملايين البروتينات البكتيرية.
تبديل أحماض أمينية مفردة لاختبار أهميتها
للانتقال من الارتباطات إلى السببية، استبدلت الفرقة بشكل منهجي 55 حمضًا أمينيًا فرديًا في Ts2631 وقيست كيف أثر كل طفرة على درجة انصهار البروتين (Tm) وعلى قدرة الإنزيم على تكسير جدران الخلايا البكتيرية. كانت بعض التغيرات حول موقع الفعالية المحتوي على الزنك مدمرة بشكل خاص. عندما غيّروا ثلاث وحدات منسقة للزنك (H30 وH131 وC139)، انخفضت Tm للبروتين بما يصل إلى نحو 20 °م وفُقد النشاط. ساهم اثنان من التيروسينات المحفوظة (Y60 وY69) أيضًا في الاستقرار. ومن المفاجئ أن إزالة رابطة ثنائية الكبريت—نوع من الروابط التساهمية بين السيستئين C80 وC90—رفعت بالفعل درجة الانصهار، رغم أنها دمرت النشاط. هذا يبيّن أن كون البروتين مستقرًا جدًا في أنبوب الاختبار لا يعني دائمًا أنه سيعمل بشكل أفضل في الظروف الحقيقية. 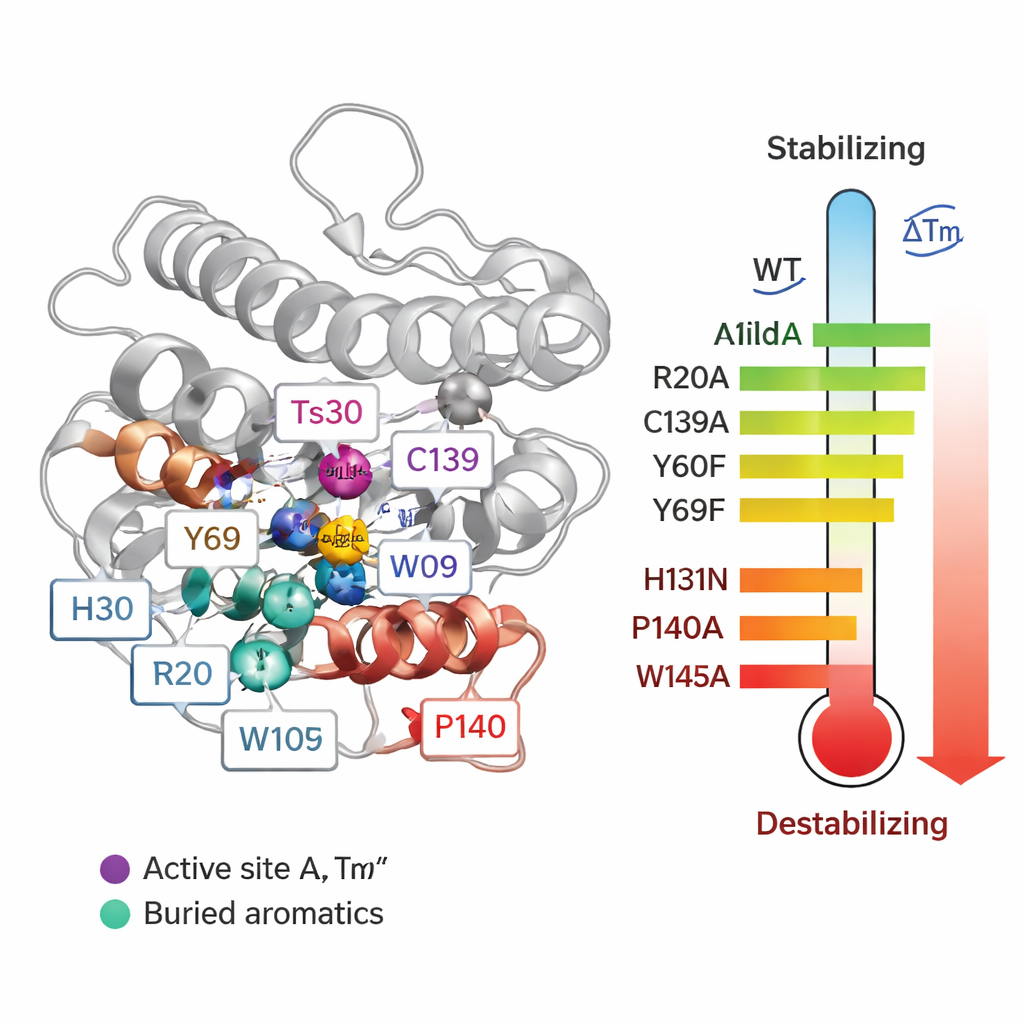
"مرابط" عطرية خفية وقبضة أساسية على جدار البكتيريا
أبرز النتائج جاءت من تبديل بقايا البرولين والتريبتوفان. أدى تغيير برولين واحد (P140)، الواقع بجانب ربط الزنك C139، إلى خفض Tm بأكثر من 21 °م وأضعف النشاط بعد التسخين، لأن الطفرة أزعجت هندسة رابطة خاصة لازمة لربط المعدن بشكل صحيح. كما ثبت أن عدة تريبتوفانات مدفونة بعمق (W102 وW109 وخاصة W145) حاسمة: استبدالها بالألانين تسبب في انخفاضات Tm بمقدار 14–24 °م وجعل الإنزيم أكثر حساسية للحرارة أثناء اختبارات النشاط. تعمل هذه البقايا العطرية كمرابط داخلية تؤمن نواة البروتين في مكانها. من بين الأرجينينات، كان لمعظمها تأثير ضئيل على الاستقرار، لكن R20 تبين أنه أساسي للإمساك بالببتيدوجليكان. عندما استبدل R20، ربط الإنزيم جدار الخلية البكتيرية ضعيفًا وفقد نشاطه عند التسخين، مما يظهر أن بعض الأحماض الأمينية تسهم أكثر في الوظيفة من مجرد الصلابة الحرارية.
من إنزيمات الينابيع الساخنة إلى مضادات بكتيرية أكثر صلابة
تُظهر الدراسة مجتمعة أن مقاومة Ts2631 الحرارية الاستثنائية تعتمد على عدد قليل من الأحماض الأمينية الموضوعة في مواقع حاسمة بدلًا من تقوية موحدة لبنية البروتين بأكملها. تشكل بقايا رابطة الزنك، وبرولين محفوظ قرب موقع الفعالية، وجوانب عطرية مدفونة نواة مُثبّتة، بينما تبدو بعض ميزات الاستقرار التقليدية، مثل روابط ثنائية الكبريت أو الجسور الملحية، أقل أهمية هنا مما كان متوقعًا. للمجال الأوسع، تشير هذه العمل إلى أن الإندوليزينات الميسوفيلية (المعتدلة الحرارة) يمكن جعلها أكثر متانة من خلال تبديل مواضع مختارة بحرص إلى تريبتوفان أو برولين دون التضحية بالنشاط المضاد للبكتيريا. بعبارة أخرى، عبر تعلم كيف تبني الطبيعة إنزيمات تتجاهل درجات الحرارة القريبة من الغليان، يحصل العلماء على مخطط عملي لهندسة مضادات حيوية بروتينية أكثر موثوقية وطويلة العمر.
الاستشهاد: Cieminska, K., Kaczorowska, AK., Kozlowski, L.P. et al. Residue-level determinants of the thermal stability of the extremophilic Ts2631 endolysin. Sci Rep 16, 7630 (2026). https://doi.org/10.1038/s41598-026-38786-z
الكلمات المفتاحية: إندوليزين مقاوم للحرارة, إنزيمات العاثيات البكتيرية, ثباتية البروتين الحرارية, مقاومة المضادات الحيوية, هندسة البروتين