Clear Sky Science · ar
دراسة حول مؤشرات حيوية لتحول الخلايا العضلية الملساء الوعائية إلى خلايا رغوية بسبب الهوموسيستين
لماذا تبدأ الشرايين المسدودة بتغيرات خلوية صغيرة
تصلب الشرايين — الانسداد والتصلب البطيءان للشرايين — هو سبب رئيسي للنوبات القلبية والسكتات الدماغية. نسمع عادة عن الكوليسترول والنظام الغذائي، لكن أقل ما يُقال عن كيفية تغير الخلايا الفردية في جدار الوعاء مع تطور المرض. تدرس هذه الدراسة عن كثب أحد المحفزات من هذا النوع، وهو جزيء دموي يُسمى الهوموسيستين، وتوضح كيف يمكنه دفع خلايا العضلات الوعائية التي تتصرف عادةً بشكل طبيعي إلى تخزين الدهون والتحول إلى ما يُسمى بالخلايا الرغوية، وهي لبنات بناء اللويحات الخطرة.
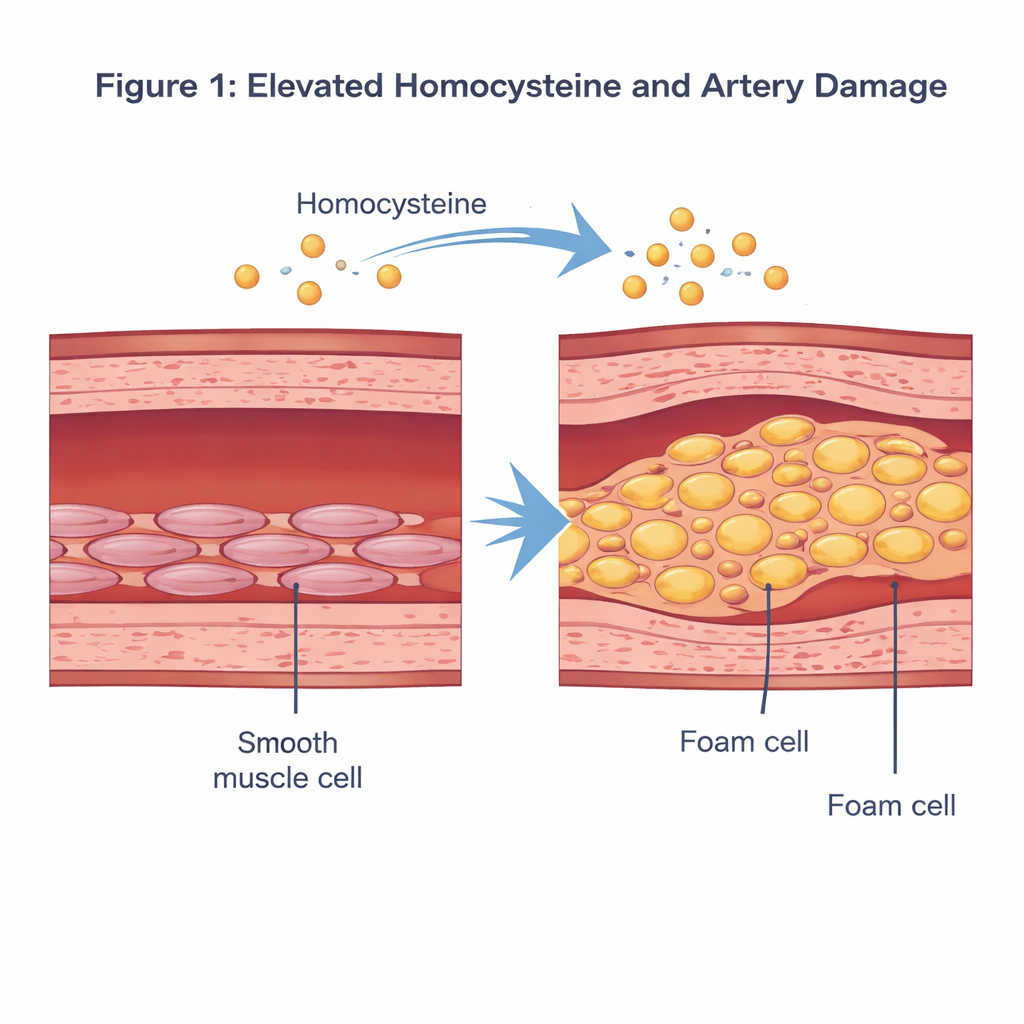
الحمض الأميني المسبب للمشكلات في مجرى الدم
الهوموسيستين هو حمض أميني يحتوي على الكبريت ينتج عندما يعالج الجسم المغذّي الغذائي ميثيونين. في الظروف الطبيعية يكون مستواه في الدم منخفضًا. عندما يرتفع فوق حوالي 15 ميكرومول لكل لتر — حالة تُسمى فرط هوموسيستينية — ربطت دراسات وبائية ذلك بزيادة خطر الأمراض القلبية الوعائية. أشارت أبحاث سابقة إلى أن فائض الهوموسيستين يمكن أن يضر البطانة الداخلية للشرايين، ويثير الالتهاب، ويغير سلوك الخلايا العضلية الملساء الوعائية، التي تقع في الطبقة الوسطى لجدار الوعاء وتساعد في تنظيم ضغط الدم عن طريق الانقباض والاسترخاء.
كيف تتحول خلايا العضلات الشريانية إلى خلايا رغوية محملة بالدهون
ركز الباحثون على كيفية إعادة تشكيل الهوموسيستين لهذه الخلايا الملساء. في أطباق المختبر، عرّضوا خلايا عضلية ملساء وعائية بشرية لجرعة من الهوموسيستين تهدف إلى محاكاة حالة تشبه المرض وقارنوها بالخلايا غير المعالجة. باستخدام صبغات واختبارات كيميائية حيوية قياسية، لاحظوا أن الخلايا المعالجة بالهوموسيستين امتلأت بقطرات دهنية ملونة باللون الأحمر، وارتفعت مستويات الكوليسترول والدهون الثلاثية لديها بشكل حاد. وفي الوقت نفسه، انخفضت مؤشرات البروتين لهويتها «الانقباضية» المعتادة، بينما ازدادت مؤشرات لحالة أكثر تركيبية ومشكلة للويحات. مجتمعة، تُظهر هذه التغيرات أن الهوموسيستين يمكن أن يدفع الخلايا العضلية الملساء بعيدًا عن دورها الطبيعي ونحو حالة شبيهة بالخلايا الرغوية المحملة بالدهون التي تسهم مباشرة في تكوّن اللويحات.
البحث عن بصمات جزيئية داخل الخلايا
لفهم أي البروتينات تتغير أثناء هذا التحول، لجأ الفريق إلى علم البروتيومات الحديث، وهي تقنية يمكنها قياس آلاف البروتينات دفعة واحدة. قارنوا مستويات البروتين في الخلايا المعالجة بالهوموسيستين مقابل الضوابط وكمَّدوا بشكل موثوق ما يقرب من 4800 بروتين. من بينها، برز 54 بروتينًا كمتعَرّضين لتغيير مهم: 13 منها زادت و41 انخفضت. العديد من البروتينات المتغيرة متورطة في التعامل مع الدهون، وبقاء الخلايا، والإجهاد التأكسدي، وإعادة تشكيل البنية الخلوية. ثم استخدم المؤلفون أدوات المعلوماتية الحيوية لتجميع هذه البروتينات في مسارات وظيفية ولرسم كيفية تفاعلها مع بعضها البعض، مبرزين شبكات مرتبطة باستقلاب الكوليسترول واستجابات الإجهاد في جدار الوعاء.
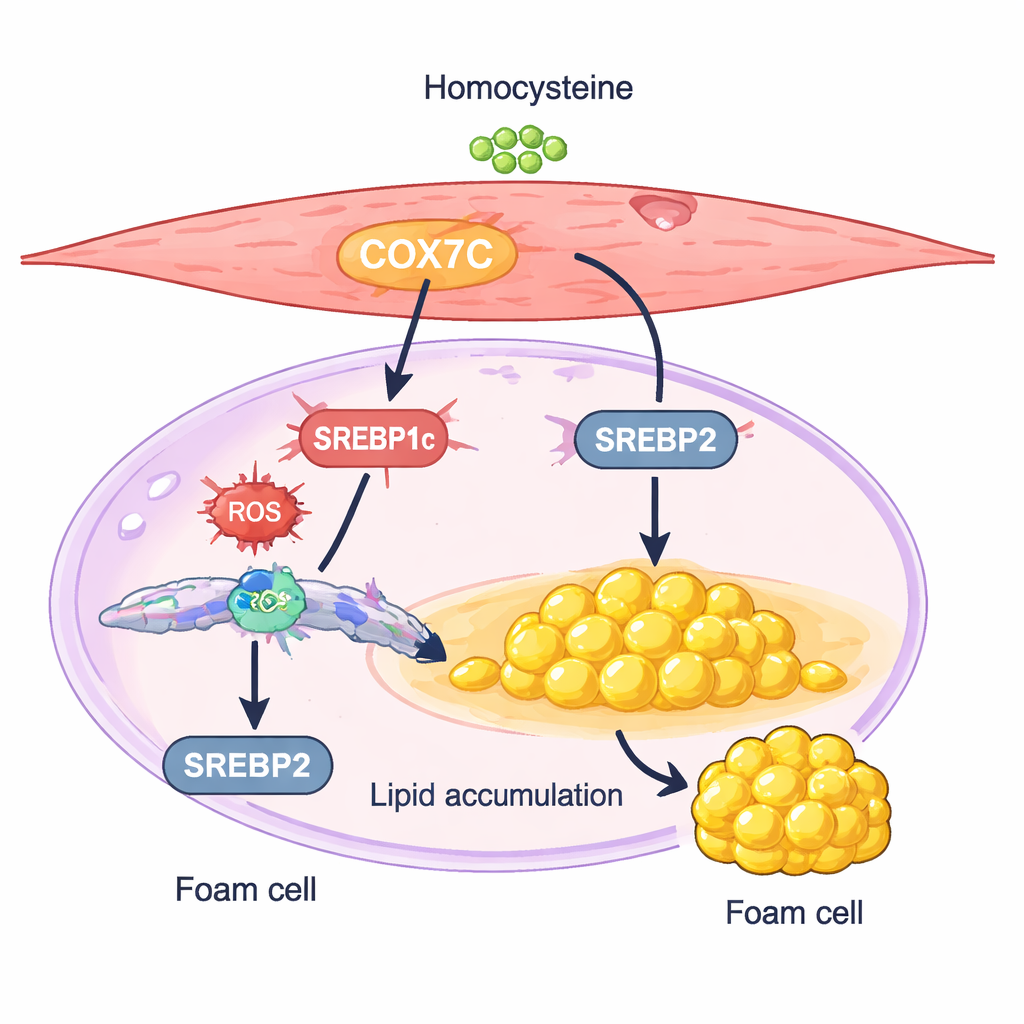
مفتاح ميتوكوندري يدفع الخلايا لتخزين الدهون
برز بروتين واحد، يُدعى COX7C، كمشتبه به الأكثر إثارة للاهتمام. COX7C هو مكوّن من مصنع الطاقة الخلوي، الميتوكوندريا، حيث يساعد في إدارة إنتاج الطاقة. في خلايا العضلات الملساء المعالجة بالهوموسيستين، كانت مستويات COX7C أعلى مقارنةً بالضوابط. أظهر الباحثون أن زيادة COX7C أكثر دفعت الخلايا إلى تراكم مزيد من الدهون والتعبير بمستويات أعلى عن منظِّمين رئيسيين لإنتاج الدهون، SREBP1c وSREBP2. أما كبت COX7C فكان له التأثير المعاكس: قلل من نشاط SREBP، وخفّض تراكم الكوليسترول والدهون الثلاثية، وقلّل التغيرات الشبيهة بالخلايا الرغوية. تؤيد هذه النتائج نموذجًا تقوم فيه زيادة الهوموسيستين برفع COX7C في الميتوكوندريا، مما يعزّز إشارات الإجهاد الخلوية، والتي بدورها تنشط تخليق الدهون المدفوع بواسطة SREBP، ملمحة بذلك إلى تحول الخلايا العضلية الملساء إلى حالة مخزّنة للدهون.
ماذا يعني هذا لصحة القلب والعلاجات المستقبلية
هذا العمل لا يثبت بعد ما يحدث في شرايين البشر، وقد أُجري في خلايا مزروعة في المختبر بدلاً من المرضى. ومع ذلك، يقدم نظرة مفصّلة على كيفية مساهمة ارتفاع الهوموسيستين في تحويل خلايا العضلات المفيدة في الشريان إلى خلايا رغوية ضارة، ويحدّد COX7C والبروتينات ذات الصلة كمؤشرات حيوية محتملة أو أهداف دوائية. بالنسبة للقارئ العام، الرسالة الأساسية هي أنه إلى جانب «الكوليسترول الجيد» و«الضار»، يمكن لتحولات صغيرة في كيمياء الدم — مثل فرط الهوموسيستينية — أن تعيد برمجة جدار الوعاء من الداخل. من خلال تحديد اللاعبين الجزيئيين مثل COX7C ومسار SREBP، تمهد هذه الدراسة الطريق لاستراتيجيات مستقبلية تهدف إلى إيقاف تكون اللويحات قبل ظهورها، عن طريق منع خلايا الشرايين من التحول إلى مخازن صغيرة للدهون.
الاستشهاد: Wang, X., Ma, X., Zhang, X. et al. Study on biomarkers of homocysteine-induced transformation of vascular smooth muscle cells into foam cells. Sci Rep 16, 7411 (2026). https://doi.org/10.1038/s41598-026-38763-6
الكلمات المفتاحية: تصلب الشرايين, الهوموسيستين, الخلايا الرغوية, الخلايا العضلية الملساء الوعائية, COX7C