Clear Sky Science · ar
PTGDS هو علامة محتملة لسرطان الغدة الرئوية تم تحديدها في تحليل شامل عبر السرطانات
لماذا قد تكون إنزيم قليل الشهرة مهمة لمرضى السرطان
معظم الناس لم يسمعوا قط عن PTGDS، إنزيم يساعد أجسامنا على إنتاج جزيئات شبيهة بالهرمونات تسمى البروستاجلاندينات. ومع ذلك قد يحمل هذا العامل الهادئ دلائل مهمة حول كيفية نمو السرطانات، وكيف تتفاعل مع جهاز المناعة، ولماذا تتصرف بعض أورام الرئة بحدة أكبر من غيرها. في هذه الدراسة، قام الباحثون بتفحص قواعد بيانات ضخمة للسرطان وأجروا تجارب مخبرية ليروا كيف يتصرف PTGDS عبر أنواع أورام متعددة، وهل يمكن أن يكون بمثابة ضوء تحذير — أو حتى مكبح — للسرطان، لا سيما سرطان الغدة الرئوية، وهو الشكل الأكثر شيوعًا لسرطان الرئة لدى غير المدخنين.
نظرة عبر سرطانات متعددة في آن واحد
لفهم PTGDS في سياق واسع، أجرى الفريق ما يسمى «التحليل الشامل عبر السرطانات» (pan‑cancer)، حيث فحصوا نشاطه في 33 نوعًا مختلفًا من السرطان باستخدام مصادر عامة كبيرة مثل أطلس جينوم السرطان وبيانات متعددة الأوميات التي تتتبع الحمض النووي الريبي والبروتين والتغيرات في الحمض النووي والمزيد. وجدوا أن مستويات PTGDS كانت منخفضة بشكل غير طبيعي في معظم السرطانات عند مقارنتها بالأنسجة السليمة، على مستويي الجين والبروتين. قليل من أنواع الأورام فقط، مثل سرطانات المبيض والبنكرياس، أظهرت مستويات أعلى. أشارت هذه الأنماط إلى أن PTGDS، في كثير من الحالات، قد يعمل أكثر كمدافع منه كمُحرك للسرطان. 
دلائل من بقاء المرضى وُتركيب حمض نووي الورم
ثم تساءل الباحثون عما إذا كانت مستويات PTGDS مرتبطة بمدة بقاء المرضى على قيد الحياة أو بسرعة تقدم مرضهم. في عدة سرطانات، بما في ذلك سرطان الغدة الرئوية وبعض أورام الدماغ، ارتبطت المستويات الأعلى من PTGDS ببقاء أفضل، بينما في بعض سرطانات الكلى ارتبطت بنتائج أسوأ، ما يوحي بأن دوره يعتمد بشدة على نسيج و«سياق» المرض. كما درسوا مدى تكرار تغيرات جين PTGDS في حمض نووي الورم وكيف يرتبط بمقاييس عدم الاستقرار الجيني في الورم، مثل عبء الطفرات الورمية وعدم استقرار الأقمار الدقيقة (microsatellite instability). في كثير من السرطانات، صاحبت مستويات PTGDS الأعلى عددًا أقل من الطفرات وصفات أقل «تشابهًا بالجذور»، وهي ميزات غالبًا ما تشير إلى مرض أقل عدوانية.
حيّ الورم ونظام المناعة
السرطان لا ينمو في عزلة — فهو يتفاعل باستمرار مع الخلايا الداعمة المحيطة وخلايا الجهاز المناعي. باستخدام أدوات حسابية تستنتج وجود خلايا مناعية انطلاقًا من نشاط الجينات، وجد الفريق أن مستويات PTGDS مرتبطة بقوة بعدد الخلايا المناعية وخلايا النسيج الضام الموجودة داخل الأورام. في سرطان الغدة الرئوية وعدة سرطانات أخرى، ارتبطت المستويات الأعلى من PTGDS بزيادة اختراق لاعبي المناعة الرئيسيين مثل الخلايا التائية والخلايا البائية والبلعميات والخلايا القاتلة الطبيعية. أظهرت مجموعات بيانات الخلية المفردة، التي تُحلل الخلايا فردًا فردًا، أن PTGDS نشط بشكل خاص في الخلايا الليفية (الخلايا البنائية)، وخلايا الأوعية الدموية، وعدة أنواع من الخلايا المناعية في نسيج الرئة الطبيعي. يدعم هذا الفكرة أن PTGDS يساهم في تشكيل «الحيّ» حول الورم، مما قد يؤثر على قدرة الجهاز المناعي على التعرف على الخلايا السرطانية والسيطرة عليها.
التعمق في سرطان الرئة: آليات داخل الخلية
نظرًا لأن الأنماط في سرطان الغدة الرئوية كانت بارزة بشكل خاص، أجرى الباحثون فحصًا أدق لهذا السرطان في المختبر. غيّروا مستويات PTGDS في خطي خلايا بشرية لسرطان الرئة، A549 وH1975. عندما أجبروا الخلايا على إنتاج مزيد من PTGDS، نمت الخلايا ببطء أكبر وكونت مستعمرات أقل، مما يشير إلى سلوك أقل ورمية. وعند تقليل PTGDS حدث العكس: تضاعفت الخلايا أسرع. أظهرت اختبارات إضافية أن زيادة PTGDS غيرت كيفية تعامل الخلايا مع الوقود القائم على الدهون، مع تعزيز تحلل الأحماض الدهنية وتخفيض المسارات التي تدعم النمو السريع. كما أزعجت الدورة الخلوية الطبيعية، مما تسبب في توقف الخلايا لفترة أطول قبل الانقسام مجددًا. ومن المثير للاهتمام أنه على الرغم من أن بعض البروتينات المرتبطة بالموت زادت، إلا أن الوفاة الخلوية الإجمالية لم ترتفع كثيرًا، ما يشير إلى أن PTGDS يبطئ النمو أساسًا بدلاً من قتل الخلايا ببساطة. 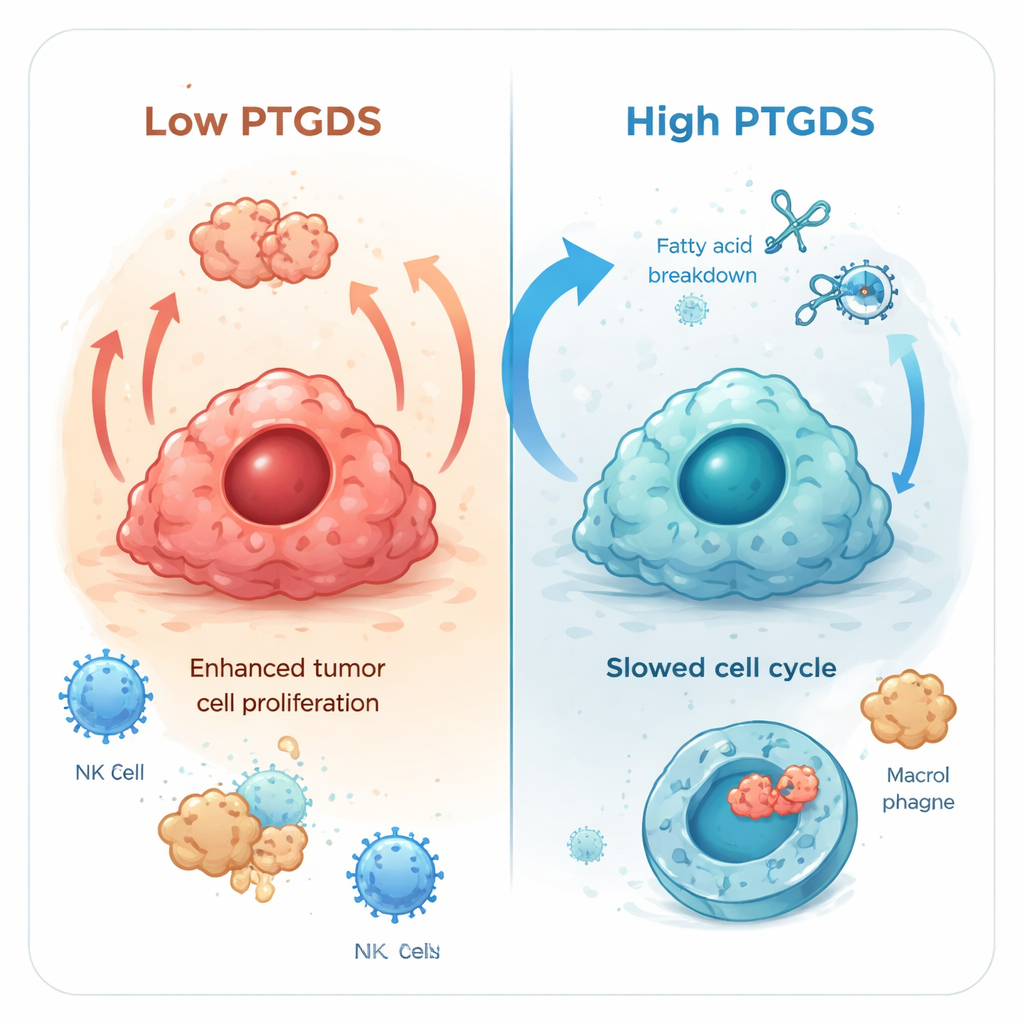
مفاتيح فوقية وُضوابط الميكروRNA
استكشف البحث أيضًا كيف يتم تنظيم PTGDS نفسه. وجد الفريق أن بعض العلامات الكيميائية على الحمض النووي، المعروفة بالمثيلة، كانت أكثر شيوعًا في منطقة جين PTGDS في أورام الرئة مقارنة بالنسيج الرئوي الطبيعي، وكانت عدة من هذه العلامات مرتبطة بمقدار إنتاج PTGDS. يوحي هذا بأن الأورام قد تخفت PTGDS عبر مفاتيح فوقية (epigenetic switches). بالإضافة إلى ذلك، ومن خلال فحص أنماط جزيئات صغيرة من الحمض النووي الريبي التنظيمية تُدعى الميكروRNA، سلطوا الضوء على مرشح واحد، miR‑3944، الذي يكون أكثر وفرة في أورام الرئة ومرتبطًا سلبًا بمستويات PTGDS. مجتمعة تشير هذه النتائج إلى طبقات تنظيمية متعددة قد تستخدمها الأورام لرفع أو خفض PTGDS.
ماذا قد يعني ذلك للمرضى في المستقبل
للغير متخصصين، الرسالة الرئيسية هي أن PTGDS يظهر نمطًا ثابتًا من الانخفاض في العديد من السرطانات، وفي سرطان الغدة الرئوية على وجه الخصوص يبدو أنه يعمل كمكبح طبيعي لنمو الورم. ترتبط مستوياته ليس فقط بكيفية نمو الأورام وانقسامها، بل أيضًا بكيفية تفاعلها مع دفاعات الجسم المناعية وكيفية استخدامهم للوقود. بينما هناك حاجة لمزيد من الأبحاث — بما في ذلك دراسات على الحيوانات وتجارب سريرية — قد يساعد PTGDS في نهاية المطاف الأطباء على التنبؤ بنتائج المرض بشكل أفضل، وتحديد من قد يستفيد من علاجات مناعية معينة، وربما يلهم علاجات جديدة تُعيد أو تُحاكي تأثيراته المقيّدة للورم.
الاستشهاد: Wang, R., Shao, F., Liu, D. et al. PTGDS is a potential marker for lung adenocarcinoma identified in a pancancer analysis. Sci Rep 16, 7611 (2026). https://doi.org/10.1038/s41598-026-38688-0
الكلمات المفتاحية: سرطان الغدة الرئوية, علامة حيوية للسرطان, البيئة المجهرية للورم, استقلاب الأحماض الدهنية, سينثاز البروستاجلاندين D2